Was du auf dieser Seite lernst
Am Beispiel des Ammoniumchlorids lernst du, was eine umkehrbare Reaktion ist: NH₃ und HCl bilden NH₄Cl (Hinreaktion), und beim Erhitzen zerfällt NH₄Cl wieder in NH₃ und HCl (Rückreaktion). Das Protolysenschema zeigt, welche Stoffe als Säure und welche als Base wirken – und warum Protonenübertragungen immer „bergab" verlaufen.
Grundlagen aus der 9. Klasse
Die Brønsted-Definition von Säuren und Basen sowie korrespondierende Paare kennst du bereits aus der 9. Klasse: → Säure-Base-Definition nach Brønsted · → Reaktion HCl + NH₃ (Kl. 9)
1 Umkehrbare Reaktionen
1.1 Beispiel: Ammoniumchlorid
a) Bildung von Ammoniumchlorid
Über ein geöffnetes Schnappdeckelglas mit konzentriertem Ammoniak stellt man ein umgekehrtes Becherglas, in dessen Innenwand sich mit konzentrierter Salzsäure getränktes Filterpapier befindet.
↑ Zum Vergrößern klicken
✕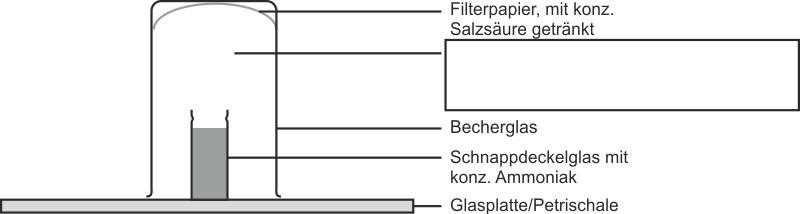
Beobachtung: Im Raum zwischen Schnappdeckelglas und Filterpapier bildet sich weißer Rauch. Auf der Glasplatte entsteht eine Schicht mit einem kristallinen weißen Feststoff.
Auswertung:
↑ Zum Vergrößern klicken
✕
↑ Zum Vergrößern klicken
✕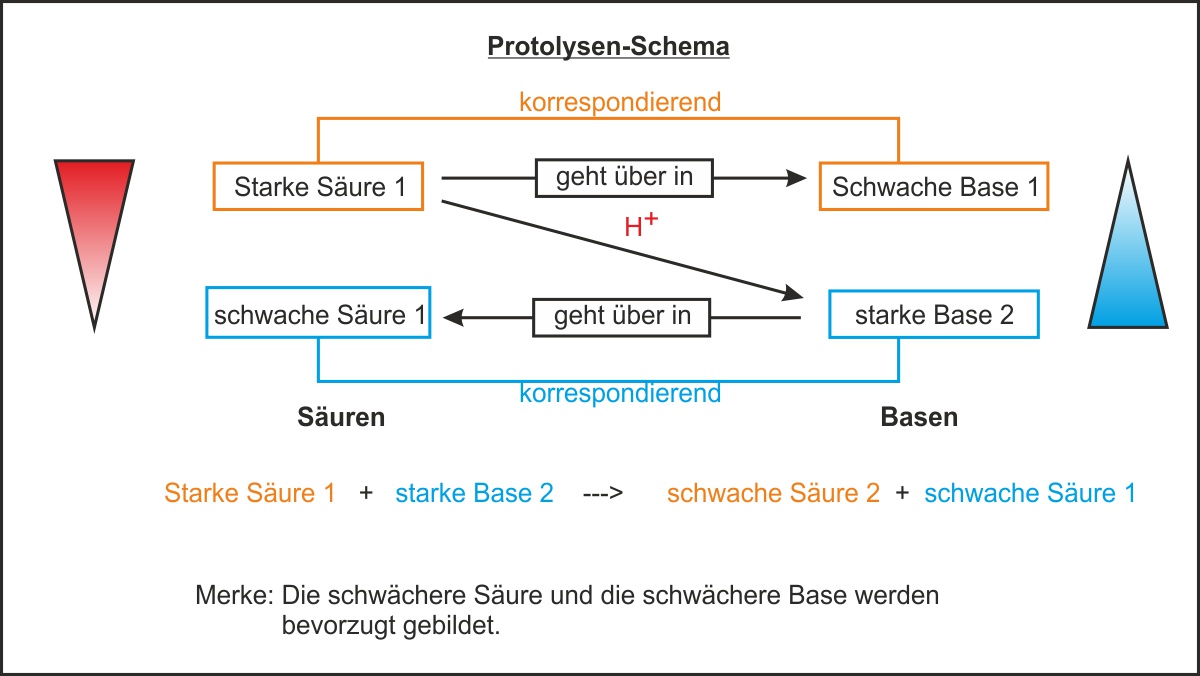
⚠️ Korrektur zum Tafelbild (untere Zeile):
Die untere Zeile des obigen Schemas enthält einen Druckfehler. Richtig lautet sie:
Starke Säure 1
+
starke Base 2
→
schwache Base 1
+
schwache Säure 2
(Dank an Fiona Ulrich für die Korrektur.)
↑ Zum Vergrößern klicken
✕
Bergab-Reaktion: Die Protolyse verläuft freiwillig von der stärkeren Säure zur schwächeren Säure – also „bergab" im Protolyseschema (vom großen roten Dreieck zum kleinen Dreieck).
b) Zerlegung von Ammoniumchlorid (Thermolyse)
Experiment: Man erhitzt in einem senkrecht eingespannten Reagenzglas festes Ammoniumchlorid.
↑ Zum Vergrößern klicken
✕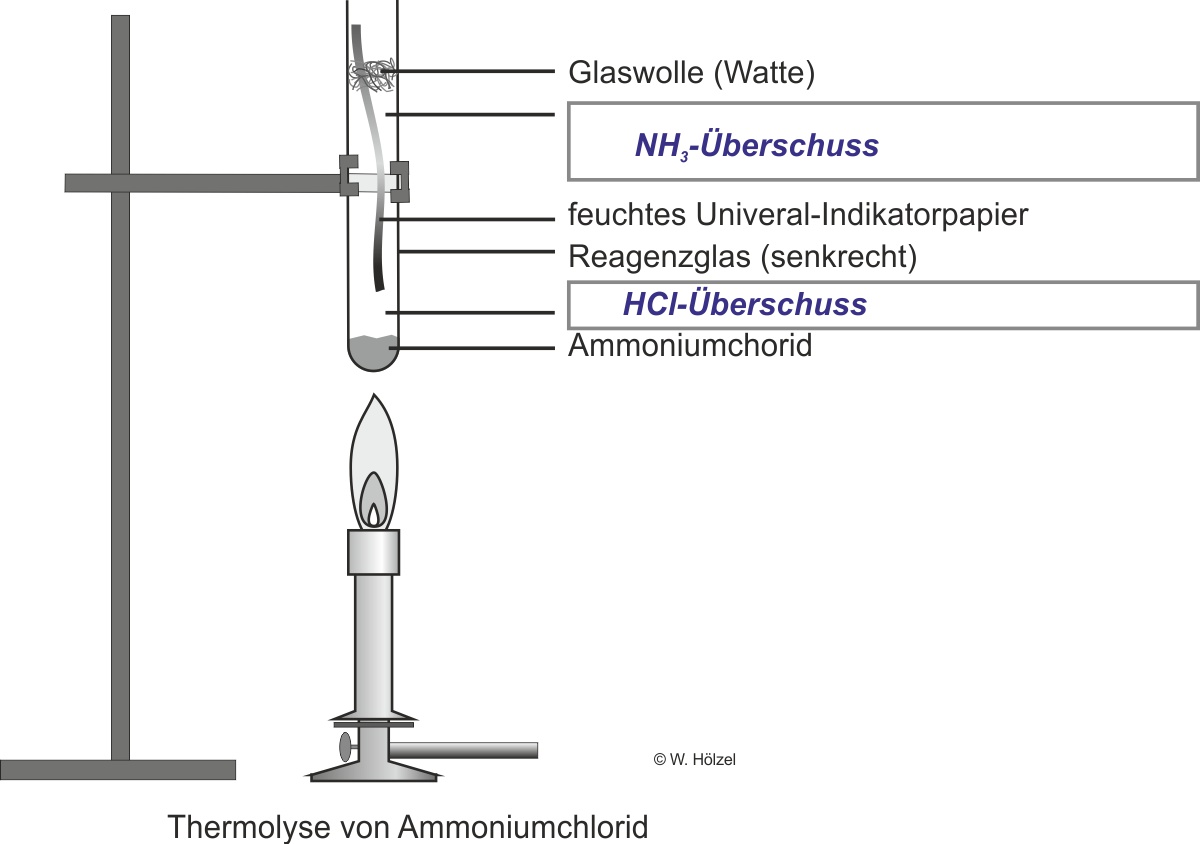
Beobachtung: Das feuchte pH-Papier färbt sich sowohl rot (Hinweis auf eine Säure – HCl-Überschuss unten) als auch blau (Hinweis auf eine Base – NH₃-Überschuss oben).
Erklärung: NH₃ diffundiert schneller (leichteres Molekül) und sammelt sich oben im Rohr, während HCl sich am Boden anreichert. Beide Gase entstehen gleichzeitig durch die Thermolyse.
Auswertung:
↑ Zum Vergrößern klicken
✕
↑ Zum Vergrößern klicken
✕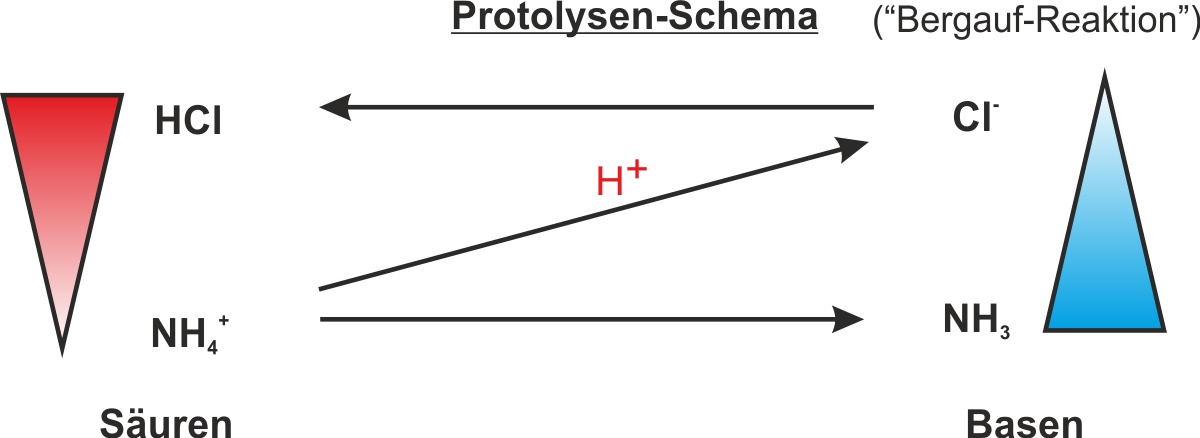
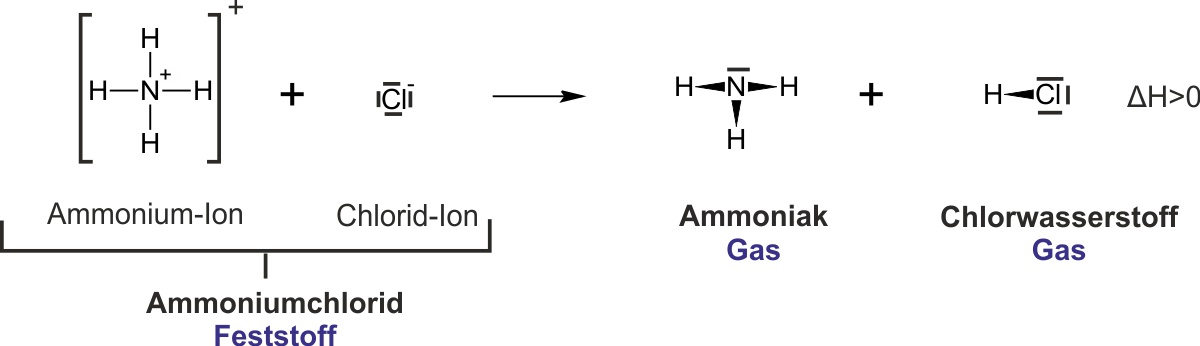
Bergauf-Reaktion: Die Thermolyse (Rückreaktion) verläuft erzwungen von der schwächeren Säure NH₄+ zur stärkeren Säure HCl – also „bergauf" im Protolyseschema. Sie benötigt Energie (ΔH > 0, endotherm).
c) Bildung und Zerlegung von Ammoniumchlorid – Zusammenfassung
Ammoniak + Chlorwasserstoff ⇌ Ammoniumchlorid
Der Doppelpfeil ⇌ zeigt: Es handelt sich um eine umkehrbare Reaktion, die in beide Richtungen ablaufen kann.
Hinweis – Reaktionen auf dem feuchten Indikatorpapier:
HCl + H2O → H3O+ + Cl−
(sauer → rot)
NH3 + H2O → NH4+ + OH−
(basisch → blau)
Auf einen Blick – die wichtigsten Aussagen
Umkehrbare Reaktion
NH₃ + HCl ⇌ NH₄Cl
Hin- und Rückreaktion sind möglich → ⇌-Pfeil
Bergab = freiwillig
Starke Säure + starke Base →
schwache Base + schwache Säure
ΔH < 0 (exotherm)
Bergauf = erzwungen
Schwache Säure + schwache Base →
starke Base + starke Säure
ΔH > 0 (endotherm) – braucht Energie
Korrespondierendes Paar
HCl / Cl⁻ und NH₄⁺ / NH₃ sind je ein korrespondierendes Säure-Base-Paar
Häufige Fragen – Umkehrbare Reaktionen / Ammoniumchlorid
Warum bildet sich beim Versuch weißer Rauch?
Gasförmiges Ammoniak (NH₃) aus dem Schnappdeckelglas und gasförmiger Chlorwasserstoff (HCl) aus dem Filterpapier treffen in der Luft aufeinander. Sie reagieren unmittelbar zu festem Ammoniumchlorid (NH₄Cl), das als winzige weiße Kristalle sichtbar wird – das nennt man weißen Rauch. Diese Reaktion ist exotherm (ΔH < 0) und verläuft freiwillig (→ Bergab-Reaktion im Protolyseschema).
Was bedeutet „Bergab-Reaktion" im Protolyseschema?
Im Protolyseschema werden Säuren von oben nach unten nach ihrer Stärke geordnet (starke Säure oben = großes umgekehrtes Dreieck). Eine Protolyse verläuft freiwillig immer von der stärkeren Säure zur schwächeren Säure – also „bergab". Im Beispiel HCl + NH₃: HCl (stärkere Säure, oben) überträgt H⁺ auf NH₃ (stärkere Base, oben) → Produkte Cl⁻ und NH₄⁺ befinden sich auf niedrigerem Niveau → Bergab-Reaktion, freiwillig. Mehr dazu: Brønsted-Definition (Kl. 9).
Warum färbt sich das Indikatorpapier sowohl rot als auch blau?
Beim Erhitzen von NH₄Cl entstehen gleichzeitig NH₃ (Gas, basisch) und HCl (Gas, sauer). Da NH₃ als leichteres Molekül schneller diffundiert, sammelt es sich im oberen Teil des Reagenzglases und färbt das Indikatorpapier dort blau (basisch). HCl reichert sich im unteren Teil an und färbt es rot (sauer). Das Indikatorpapier muss feucht sein, damit die Gase reagieren können: HCl + H₂O → H₃O⁺ + Cl⁻ und NH₃ + H₂O → NH₄⁺ + OH⁻.
Was ist der Unterschied zwischen NH₃ und NH₄⁺?
NH₃ (Ammoniak) ist eine schwache Base: Es nimmt ein Proton auf → NH₄⁺ (Ammonium-Ion, schwache Säure). NH₃ und NH₄⁺ bilden ein korrespondierendes Säure-Base-Paar. NH₃ hat keine Ladung und ist gasförmig, NH₄⁺ ist ein Ion und liegt in Salzen wie NH₄Cl als Feststoff vor.
Warum ist die Zerlegung von NH₄Cl eine „Bergauf-Reaktion"?
Die Thermolyse NH₄Cl → NH₃ + HCl läuft von der schwächeren Säure NH₄⁺ zur stärkeren Säure HCl – also „bergauf" im Protolyseschema. Sie verläuft nicht freiwillig, sondern muss durch Wärmezufuhr erzwungen werden (ΔH > 0, endotherm). Das ist möglich, weil beide Produkte gasförmig sind und das Gleichgewicht durch Entweichen der Gase auf die Produktseite gezogen wird.
Lernkarten – Umkehrbare Reaktionen
Klicke auf eine Karte, um die Antwort zu sehen.
Was beobachtet man, wenn NH₃ und HCl-Gas aufeinandertreffen?
Bildung von weißem Rauch (festes NH₄Cl): NH₃ + HCl → NH₄Cl (exotherm, ΔH < 0)
Was bedeutet ⇌ in einer Reaktionsgleichung?
Die Reaktion ist umkehrbar – sie kann sowohl in Hin- als auch in Rückrichtung ablaufen.
Was ist das korrespondierende Paar zur Säure HCl?
HCl (Säure) / Cl⁻ (konjugierte Base)
HCl gibt H⁺ ab → Cl⁻ entsteht.
Warum verläuft die Bildung von NH₄Cl „bergab"?
HCl ist eine stärkere Säure als NH₄⁺.
Protolyse läuft freiwillig von stärkerer → schwächerer Säure,
d. h. „bergab" im Protolyseschema.
Aufgabe: Ordne zu – Bergab oder Bergauf?
a) NH₄Cl → NH₃ + HCl (Thermolyse)
b) HCl + NH₃ → NH₄Cl (Bildung)
a) Bergauf (erzwungen, endotherm, ΔH > 0)
b) Bergab (freiwillig, exotherm, ΔH < 0)
Weiter im Kapitel Gleichgewichtsreaktionen
← Übersicht Gleichgewichtsreaktionen → 1.2 Beispiel: Calciumhydroxid
🔁 Grundlagen (Kl. 9): Brønsted-Definition · Reaktion HCl + NH₃
📌 Weiterführend: Prinzip von Le Chatelier · Massenwirkungsgesetz
