Was du auf dieser Seite lernst
Butan (C₄H₁₀) ist das erste Alkan, das in zwei verschiedenen Strukturen vorkommt. Du lernst den zentralen Begriff der Konstitutionsisomerie kennen, verstehst warum n-Butan und Isobutan verschiedene Siedepunkte haben, und übst die Halbstrukturformel als platzsparende Schreibweise.
Grundlagen aus 1.1 Methan
Summenformel, Strukturformel und Lewis-Formel hast du am Beispiel Methan kennengelernt: → 1.1 Methan · → Lewis-Formeln (Kl. 9)
Hinweis: 1.2 Ethan und 1.3 Propan werden nur bei ausreichend Zeit besprochen. Da sie ähnlich aufgebaut sind, wird auf einen eigenen Heftaufschrieb verzichtet (vgl. 1.5 Homologe Reihe).
1.4.1 Vorkommen
Im Erdgas; fällt an bei der Benzingewinnung.
1.4.2 Eigenschaften
Farbloses Gas · größere Dichte als Luft · brennbar (Verbrennungsprodukte bei vollständiger Verbrennung: CO2 und H2O) · unter Druck leicht verflüssigbar.
1.4.3 Ermittlung der Summenformel und Strukturformel
a) Qualitative Analyse (Elementaranalyse)
↑ Zum Vergrößern klicken
✕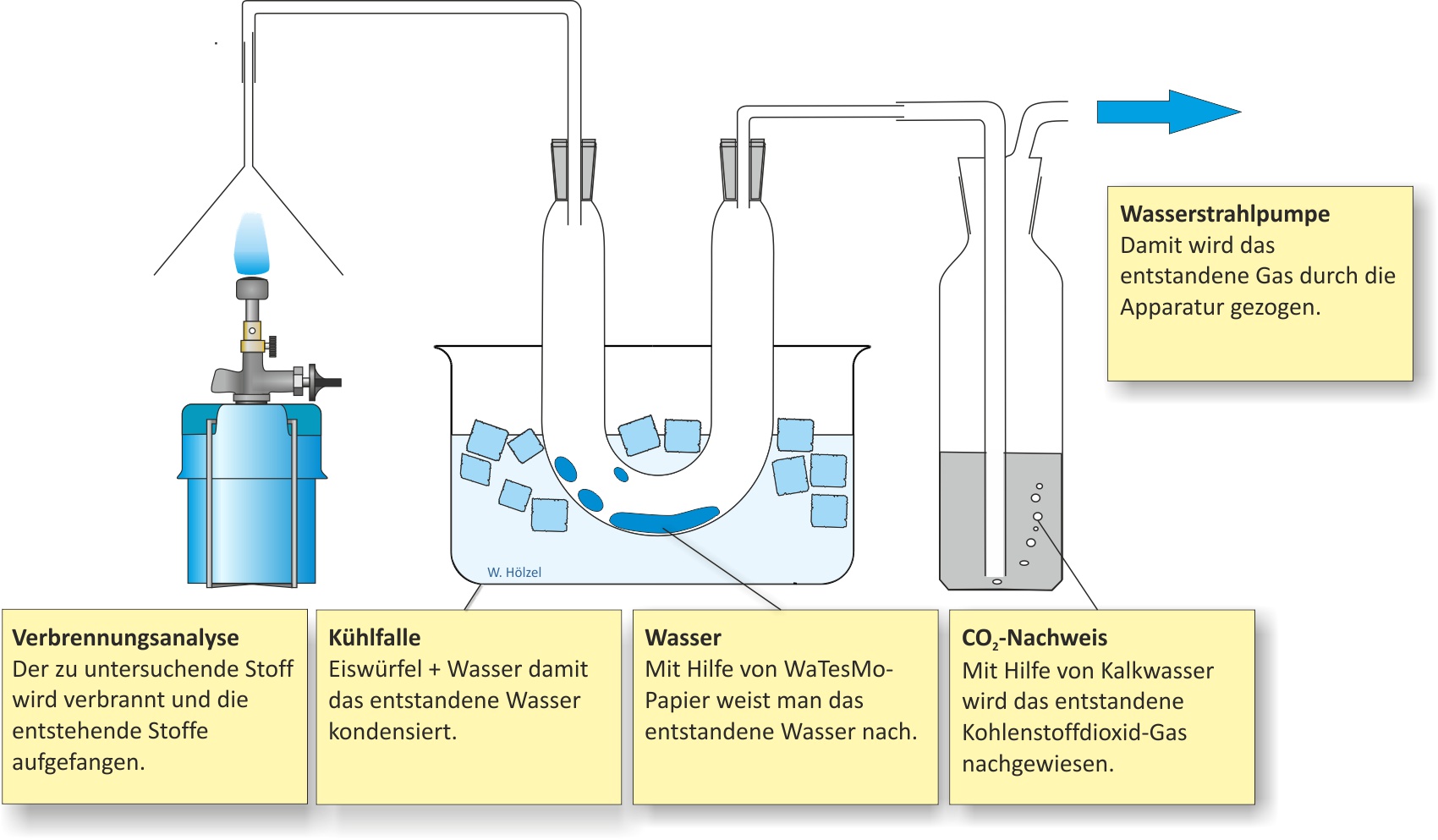
Die Verbrennungsprodukte (Wasser, Kohlenstoffdioxid) zeigen, dass Butan Kohlenstoff, Wasserstoff und eventuell Sauerstoff enthält.
b) Bau und Formeln
1. Molare Masse = 58,12 g/mol · Molekülmasse = 58,12 u
2. Summenformel: C4H10
3. Strukturformel – zwei Möglichkeiten:
✕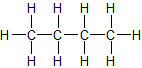 ✕
✕
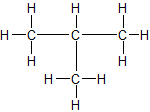
ZMK: nur Van-der-Waals-Kräfte. Bei n-Butan können sich die Moleküle dichter zusammenlagern → stärkere ZMK → etwas höhere Siedetemperatur als Isobutan.
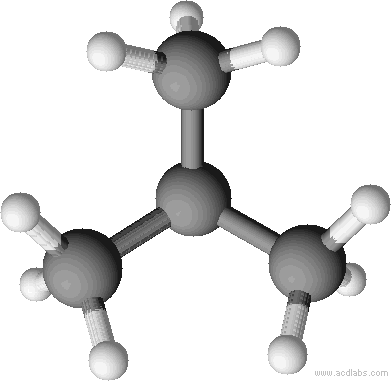
Räumliche Strukturen im Kugelstabmodell (versuche, die Abbildungen n-Butan oder Isobutan zuzuordnen):
✕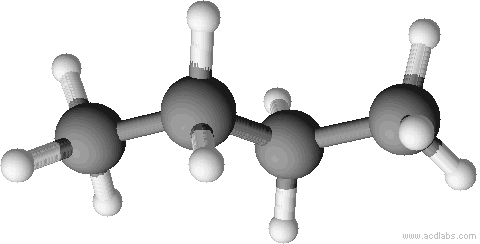 ✕
✕
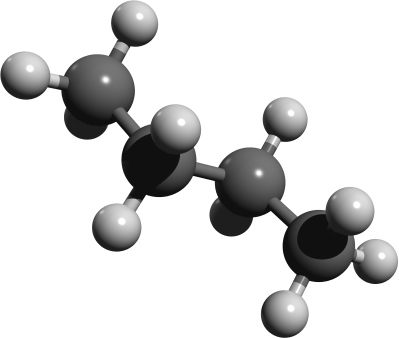
Renderbild n-Butan als Kugelstabmodell:
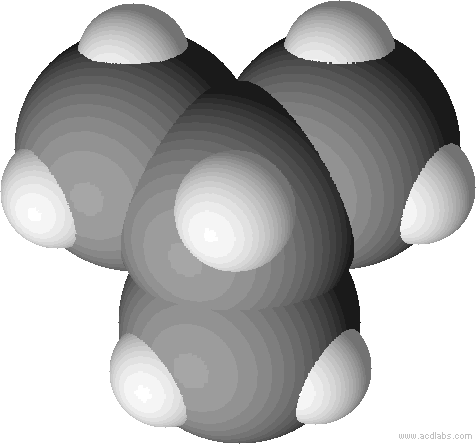
Kalottenmodell von 2-Methylpropan (= Isobutan) – bei Kalottenmodellen wird die Raumfüllung der Atome sichtbar:
Da Strukturformeln bei größeren Molekülen zu aufwendig sind, nutzt man die Halbstrukturformel: Die Wasserstoffatome werden als Summe direkt hinter das jeweilige C-Atom geschrieben. Man ermittelt zunächst, wie viele Bindungen ein C-Atom bereits hat, und ergänzt H-Atome bis zur Vierbindigkeit. Hier am Beispiel Isobutan:
↑ Zum Vergrößern klicken
✕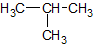
1.4.4 Verwendung
Heizgas („blaue Gaskartuschen") · Kältemittel (Ersatz für FCKW) · Treibgas in Sprays · Feuerzeuggas (häufig zusammen mit Propan).
1.4.5 Isomerie
(isos (griech.) = gleich; meros (griech.) = Teil)
Definition – Konstitutionsisomerie
Verbindungen, deren Moleküle bei gleicher Summenformel unterschiedliche Strukturformeln besitzen, bezeichnet man als Isomere. Isomere unterscheiden sich vor allem in ihren physikalischen Eigenschaften (Schmelz- und Siedepunkt) und wenig in ihren chemischen Reaktionen.
1.4.6 Vollständige Verbrennung (Oxidation)
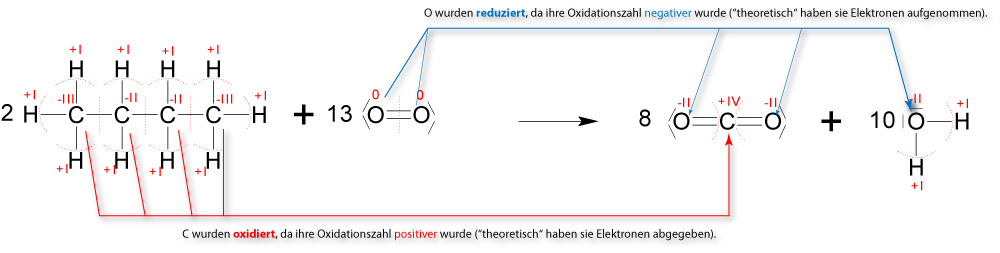
Wenn Butan vollständig verbrannt wird, entstehen ausschließlich Kohlenstoffdioxid und Wasser:
↑ Zum Vergrößern klicken
✕
Auf einen Blick – Butan
Summenformel
C4H10 · molare Masse 58,12 g/mol · stimmt mit der allg. Formel CₙH₂ₙ₊₂ überein (n = 4 → 4·2+2 = 10 H).
Konstitutionsisomerie
n-Butan (Sdp. −0,5 °C) und Isobutan = 2-Methylpropan (Sdp. −12 °C) haben die gleiche Summenformel C₄H₁₀, aber verschiedene Strukturformeln.
ZMK und Siedepunkt
Nur Van-der-Waals-Kräfte. n-Butan lagert sich dichter zusammen → stärkere ZMK → höherer Siedepunkt als das verzweigte Isobutan.
Halbstrukturformel
H-Atome als Summe hinter das C schreiben. n-Butan: CH₃–CH₂–CH₂–CH₃ · Isobutan: CH₃–CH(CH₃)–CH₃ · Vierbindigkeit von C muss stets erfüllt sein.
Häufige Fragen – Butan
Was versteht man unter Konstitutionsisomerie?
Konstitutionsisomere sind Verbindungen mit gleicher Summenformel, aber unterschiedlicher Verknüpfung der Atome. Bei C₄H₁₀ gibt es zwei Isomere: n-Butan (unverzweigte Kette) und 2-Methylpropan (Isobutan) (verzweigte Kette). Sie unterscheiden sich in physikalischen Eigenschaften wie dem Siedepunkt, kaum aber in chemischen Reaktionen. Mit steigender C-Zahl nimmt die Zahl möglicher Isomere stark zu (C₅: 3, C₁₀: 75).
Warum hat n-Butan einen höheren Siedepunkt als Isobutan?
Beide Isomere sind unpolar und besitzen nur Van-der-Waals-Kräfte als Wechselwirkung zwischen den Molekülen. Die gestreckte Kette von n-Butan ermöglicht eine größere Kontaktfläche zwischen benachbarten Molekülen als die kompaktere, kugelförmigere Gestalt von Isobutan. Größere Kontaktfläche → stärkere Van-der-Waals-Kräfte → höherer Siedepunkt (n-Butan: −0,5 °C; Isobutan: −12 °C).
Was ist der Unterschied zwischen Strukturformel, Halbstrukturformel und Summenformel?
Die Summenformel gibt nur die Anzahl der Atome an (C₄H₁₀), nicht deren Anordnung. Die Strukturformel zeigt alle Bindungsstriche explizit – anschaulich, aber bei großen Molekülen aufwendig. Die Halbstrukturformel ist ein Kompromiss: Das C-Gerüst wird ausgeschrieben, H-Atome werden als Anzahl hinter das jeweilige C-Atom gesetzt. Isobutan: CH₃–CH(CH₃)–CH₃ · n-Butan: CH₃–CH₂–CH₂–CH₃.
Wofür wird Butan im Alltag verwendet?
Butan wird wegen seiner leichten Verflüssigbarkeit unter Druck vielfältig eingesetzt: als Heizgas in Gaskartuschen beim Camping, als Kältemittel (FCKW-Ersatz in Kühlschränken), als Treibgas in Sprühdosen und als Feuerzeuggas (oft zusammen mit Propan).
Wie lautet die ausgeglichene Verbrennungsgleichung für n-Butan?
Vollständige Verbrennung:
2 C₄H₁₀ + 13 O₂ → 8 CO₂ + 10 H₂O
Kontrolle: C: 8 = 8 ✓ · H: 20 = 20 ✓ · O: 26 = 26 ✓
Die Reaktion ist stark exotherm – deshalb wird Butan als Brennstoff genutzt.
Lernkarten – Butan
Klicke auf eine Karte, um die Antwort zu sehen.
Gib Summenformel und molare Masse von Butan an. Prüfe die allg. Alkan-Formel.
Summenformel: C₄H₁₀
Molare Masse: 58,12 g/mol
Formel CₙH₂ₙ₊₂ mit n=4: 2·4+2 = 10 H ✓
Was sind Konstitutionsisomere? Nenne die beiden C₄H₁₀-Isomere mit Siedepunkten.
Gleiche Summenformel, verschiedene Struktur:
n-Butan: unverzweigt · Sdp. −0,5 °C
2-Methylpropan (Isobutan): verzweigt · Sdp. −12 °C
Schreibe n-Butan und Isobutan als Halbstrukturformel.
n-Butan:
CH₃–CH₂–CH₂–CH₃
Isobutan (2-Methylpropan):
CH₃–CH(CH₃)–CH₃
Warum hat n-Butan einen höheren Siedepunkt als Isobutan, obwohl beide C₄H₁₀ sind?
Nur Van-der-Waals-Kräfte vorhanden.
n-Butan: gestreckte Kette → größere Kontaktfläche
→ stärkere VdW-Kräfte → höherer Siedepunkt
Isobutan: kompaktere Form → weniger Kontakt
Stelle die ausgeglichene Verbrennungsgleichung für n-Butan auf.
2 C₄H₁₀ + 13 O₂ → 8 CO₂ + 10 H₂O
Kontrolle:
C: 2·4 = 8 | 8·1 = 8 ✓
H: 2·10 = 20 | 10·2 = 20 ✓
O: 13·2 = 26 | 8·2+10 = 26 ✓
Weiter im Kapitel Alkane
← 1.1 Methan → 1.5 Homologe Reihe → 1.6 Nomenklatur
🔁 Grundlagen:
1.1 Methan ·
Lewis-Formeln (Kl. 9)
📚 Vertiefung:
Isomerie bei Alkenen ·
Isomerie (Kursstufe)
