Was du auf dieser Seite lernst
Methan (CH₄) ist das einfachste Alkan und gleichzeitig der Einstieg in die Organische Chemie. Du lernst, wie man über die qualitative Elementaranalyse auf die Summenformel schließt, wie die Strukturformel und der Bindungswinkel aussehen, und warum die Verbrennung von Methan eine Redoxreaktion ist.
Grundlagen aus der 9. Klasse
Lewis-Formeln, Atombindung und Oxidationszahlen hast du in der 9. Klasse kennengelernt: → Lewis-Formeln (Kl. 9) · → Oxidationszahlen (Kl. 9)
1.1.1 Vorkommen
Methan kommt vor in: Erdgas, Sumpfgas, Biogas, Grubengas.
1.1.2 Eigenschaften
- farb- und geruchloses Gas
- geringere Dichte als Luft
- brennbar
1.1.3 Ermittlung der Summenformel (Molekülformel) und Strukturformel
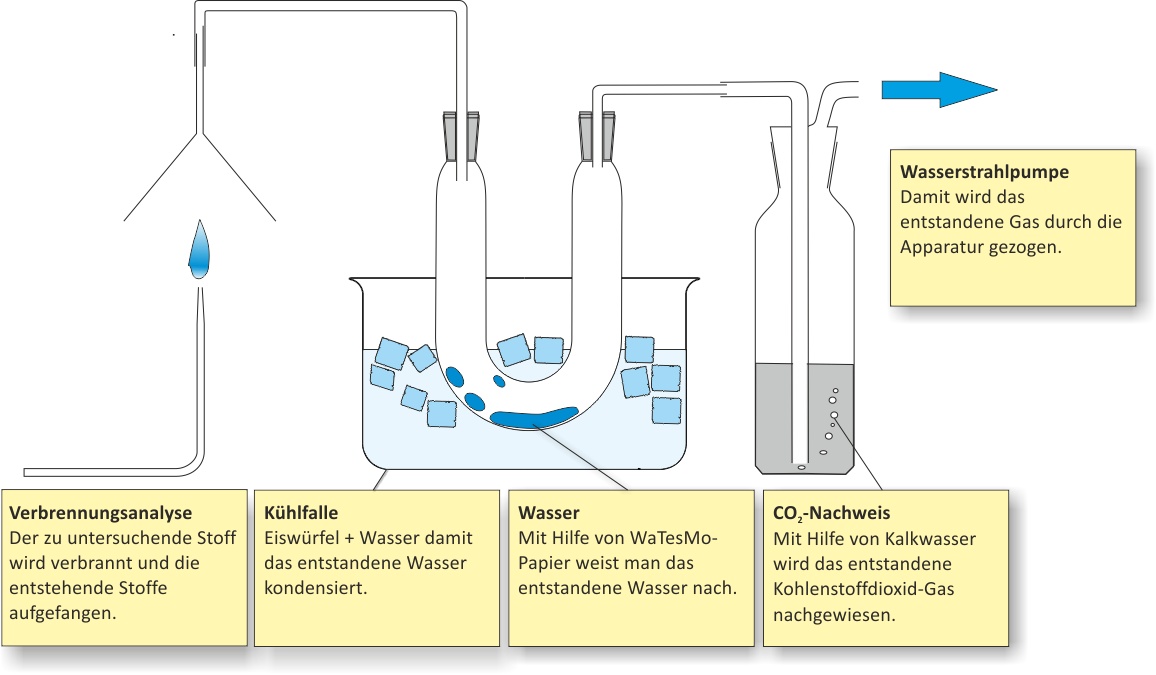
a) Qualitative Analyse (Elementaranalyse)
Hierfür wird der zu untersuchende Stoff verbrannt und die Verbrennungsprodukte bestimmt.
Bildet sich Wasser, ist Wasserstoff als Element vorhanden.
Kohlenstoff lässt sich als Ruß (unvollständige Verbrennung)
oder als Kohlenstoffdioxid nachweisen.
Der CO₂-Nachweis erfolgt mit der Kalkwasserprobe:
Das entstandene Gas wird in Kalkwasser eingeleitet –
eine Trübung zeigt CO₂ an.
↑ Zum Vergrößern klicken
✕
- Nachweis von Wasserstoff → Bildung von Wasser → WaTesMo-Papier oder wasserfreies Kupfersulfat.
- Nachweis von C → Bildung von CO2 → Nachweis als CaCO3:
Ca(OH)2 (aq) + CO2 (g) → CaCO3 (s) + H2O (l)
Die Verbrennungsprodukte (Wasser, Kohlenstoffdioxid) zeigen, dass Methan Kohlenstoff, Wasserstoff und eventuell Sauerstoff enthält.
b) Bestimmung der molaren Masse
Mit der Gaswägung lässt sich die molare Masse von Methan bestimmen:
M(Methan) = 16 g/mol · Molekülmasse 16 u.
c) Summenformel: CH4
d) Strukturformel
Man zeichnet Methan meist mit einem Winkel von 90°. Dieser Winkel entspricht nicht
dem tatsächlichen Bindungswinkel (vgl. unten). Man kann sich aber vorstellen, dass man
direkt auf das Molekül blickt.
↑ Zum Vergrößern klicken
✕ ✕
✕
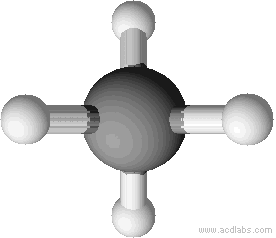
Tetraedrische Anordnung der Wasserstoffatome um das Kohlenstoffatom (Bindungswinkel 109,5°). Erklärung: größtmögliche Entfernung der Wasserstoffatome.
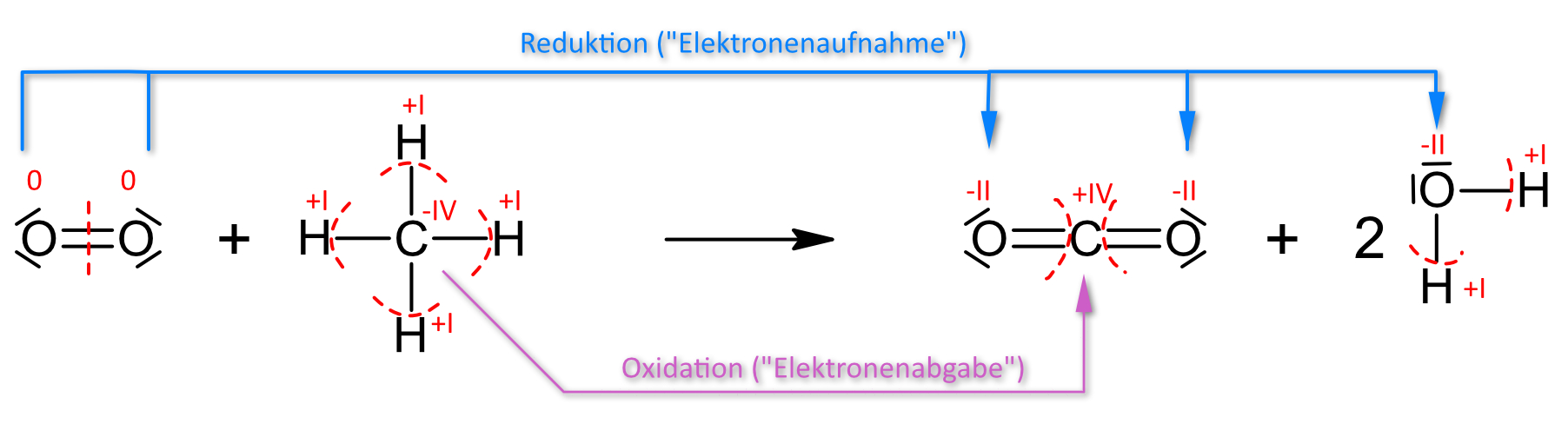
1.1.4 Vollständige Verbrennung
0 −IV +I +IV −II +I −II
2 O2 + CH4 → CO2 + 2 H2O ΔH = −888 kJ/mol
↑ Zum Vergrößern klicken
✕
Hinweis: Wenn die Ermittlung der Oxidationszahlen Schwierigkeiten macht, kann man es hier nochmals nachlesen.
1 l Methan benötigt zur vollständigen Verbrennung 10 Liter Luft (2 l Sauerstoff).
Auf einen Blick – Methan
Summenformel
Methan: CH₄ · molare Masse 16 g/mol · einfachstes Alkan · allg. Formel der Alkane: CₙH₂ₙ₊₂ (hier n = 1).
Tetraeder
Die vier H-Atome ordnen sich tetraedrisch um das C-Atom an. Bindungswinkel: 109,5° (größtmögliche Abstoßung der Bindungselektronenpaare).
Elementaranalyse
Verbrennung → H₂O (Wassernachweis: WaTesMo) + CO₂ (Kalkwasserprobe: Trübung durch CaCO₃) → Methan enthält C und H.
Verbrennung
CH₄ + 2 O₂ → CO₂ + 2 H₂O · ΔH = −888 kJ/mol (exotherm). C wird von −IV auf +IV oxidiert; O von 0 auf −II reduziert.
Häufige Fragen – Methan
Wie weist man experimentell nach, dass Methan Kohlenstoff und Wasserstoff enthält?
Methan wird vollständig verbrannt. Die entstehenden Gase und Dämpfe werden durch zwei Nachweisreagenzien geleitet: Wassernachweis mit wasserfreiem Kupfersulfat (wird blau) oder WaTesMo-Papier (Blaufärbung zeigt Wasser an) → Methan enthält Wasserstoff. CO₂-Nachweis mit Kalkwasser Ca(OH)₂: Trübung durch CaCO₃-Bildung → Methan enthält Kohlenstoff.
Warum ist der Bindungswinkel in Methan 109,5° und nicht 90°?
Die vier bindenden Elektronenpaare stoßen sich gemäß dem VSEPR-Modell (Valence Shell Electron Pair Repulsion) so weit wie möglich ab. Maximale Abstoßung ergibt eine tetraedrische Anordnung mit einem Bindungswinkel von 109,5°. In der vereinfachten Strukturformel zeichnet man 90°-Winkel, weil man so tut, als würde man von oben auf das Molekül blicken.
Warum ist die Verbrennung von Methan eine Redoxreaktion?
Bei der Verbrennung ändert sich die Oxidationszahl des Kohlenstoffs von −IV (in CH₄) auf +IV (in CO₂) → Oxidation. Der Sauerstoff wird von 0 (O₂) auf −II (in CO₂ und H₂O) reduziert → Reduktion. Es findet also ein Elektronenübergang statt: Methan ist das Reduktionsmittel, Sauerstoff das Oxidationsmittel. → Oxidationszahlen (Kl. 9)
Was bedeutet ΔH = −888 kJ/mol bei der Verbrennung?
Das negative Vorzeichen zeigt, dass Energie abgegeben wird – die Reaktion ist exotherm. Pro Mol verbranntem Methan (= 16 g) werden 888 kJ Wärmeenergie freigesetzt. Das erklärt, warum Methan (Erdgas) als Energieträger zum Heizen und Kochen eingesetzt wird. Mehr zur Reaktionsenthalpie: → Enthalpie (Kursstufe)
Wo kommt Methan natürlich vor und warum ist es klimarelevant?
Methan kommt natürlich in Erdgas (Hauptbestandteil), Sumpfgas (Zersetzung organischer Stoffe unter Wasser), Biogas (Gärung) und Grubengas (Steinkohlebergbau) vor. Als Treibhausgas ist CH₄ etwa 25-mal klimawirksamer als CO₂ (bezogen auf 100 Jahre), weil es Infrarotstrahlung besonders effektiv absorbiert.
Lernkarten – Methan
Klicke auf eine Karte, um die Antwort zu sehen.
Gib Summenformel, molare Masse und Bindungswinkel von Methan an.
Summenformel: CH₄
Molare Masse: 16 g/mol
Bindungswinkel: 109,5° (Tetraeder)
Struktur: 4 H-Atome tetraedrisch um C
Wie weist man bei der Elementaranalyse Kohlenstoff und Wasserstoff nach?
H-Nachweis:
WaTesMo-Papier oder CuSO₄ (wasserfrei) → Blaufärbung = H₂O vorhanden
C-Nachweis:
Kalkwasser Ca(OH)₂ → Trübung = CO₂ vorhanden
Stelle die vollständige Verbrennungsgleichung von Methan auf.
CH₄ + 2 O₂ → CO₂ + 2 H₂O
ΔH = −888 kJ/mol (exotherm)
Kontrolle: C: 1=1 ✓ · H: 4=4 ✓ · O: 4=4 ✓
Welche Oxidationszahlen hat Kohlenstoff in CH₄ und in CO₂? Was folgt daraus?
CH₄: C hat Oxidationszahl −IV
CO₂: C hat Oxidationszahl +IV
→ Oxidationszahl steigt → C wird oxidiert
→ Methan = Reduktionsmittel
Wieviel Liter Luft benötigt 1 l Methan zur vollständigen Verbrennung, und warum?
10 Liter Luft (≈ 2 l O₂, da Luft ≈ 21 % O₂)
CH₄ + 2 O₂ → … · Stöchiometrie: 1 Vol. CH₄ : 2 Vol. O₂
Luft enthält ~20 % O₂ → 2 l O₂ stecken in 10 l Luft
Weiter im Kapitel Alkane
← 1 Alkane – Übersicht → 1.4 Butan → 1.5 Homologe Reihe
🔁 Grundlagen (Kl. 9):
Lewis-Formeln ·
Oxidationszahlen
📚 Vertiefung Kursstufe:
Enthalpie ΔH
