Was du auf dieser Seite übst
Hier übst du die Genfer Nomenklatur an allen 9 Konstitutionsisomeren der Summenformel C7H16. Schau dir die Halbstrukturformel an, überlege den systematischen Namen – und klappe dann die Lösung auf.
Grundlagen – Genfer Nomenklatur
Die 7 Nomenklaturregeln hast du auf der vorherigen Seite kennengelernt: → 1.6 Genfer Nomenklatur der Alkane
1.6.3 Isomere der Summenformel C7H16
Entwickle zur Übung die Halbstrukturformeln der Isomeren der Summenformel C7H16 und benenne die Verbindungen mit ihrem systematischen Namen. Beachte: Es gibt 9 verschiedene Konstitutionsisomere.
Schau dir jede Halbstrukturformel an, überlege den Namen – und klappe dann die Lösung auf.
Isomer 1 von 9
Lösung anzeigen
Name: n-Heptan
Isomer 2 von 9
Lösung anzeigen
Name: 2-Methylhexan
Isomer 3 von 9
Lösung anzeigen
Name: 3-Methylhexan
Isomer 4 von 9

Lösung anzeigen
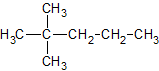
Name: 2,2-Dimethylpentan
Isomer 5 von 9
Lösung anzeigen
Name: 2,3-Dimethylpentan
Isomer 6 von 9
Lösung anzeigen
Name: 2,4-Dimethylpentan
Isomer 7 von 9

Lösung anzeigen

Name: 3,3-Dimethylpentan
Isomer 8 von 9

Lösung anzeigen
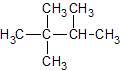
Name: 2,2,3-Trimethylbutan
Isomer 9 von 9

Lösung anzeigen

Name: 3-Ethylpentan
Lösung: Alle 9 Isomere im Überblick
1 unverzweigtes Isomer: n-Heptan
2 einfach verzweigte: 2-Methylhexan · 3-Methylhexan
5 zweifach verzweigte: 2,2- · 2,3- · 2,4- · 3,3-Dimethylpentan · 3-Ethylpentan
1 dreifach verzweigtes: 2,2,3-Trimethylbutan
Auf einen Blick – die wichtigsten Aussagen
KONSTITUTIONSISOMERE
Isomere haben die gleiche Summenformel, aber eine verschiedene Verknüpfung der Atome (→ verschiedene Strukturformeln).
ANZAHL
C7H16 hat 9 Konstitutionsisomere. Mit steigender Kettenlänge wächst die Isomerenzahl stark an.
SYSTEMATISCH VORGEHEN
Erst die längste Kette (unverzweigt), dann schrittweise kürzer mit mehr Verzweigungen – so findet man alle Isomere.
EIGENSCHAFTEN
Stärker verzweigte Isomere haben niedrigere Siedepunkte, weil die van-der-Waals-Kräfte bei kompakterer Gestalt schwächer sind.
Häufige Fragen – Isomere und Nomenklaturübungen
Was sind Konstitutionsisomere?
Konstitutionsisomere (auch Strukturisomere) sind Verbindungen mit gleicher Summenformel, aber verschiedener Verknüpfung der Atome. Sie sind vollständig verschiedene chemische Verbindungen mit eigenen Eigenschaften (Siedepunkt, Schmelzpunkt, Dichte). Alle 9 Isomere von C7H16 gehören zur Gruppe der Konstitutionsisomere.
Wie findet man systematisch alle Isomere einer Summenformel?
Man geht nach folgendem Schema vor: (1) Längste unverzweigte Kette (hier: n-Heptan, 7 C). (2) Hauptkette um 1 kürzen und eine Methylgruppe anbringen – dabei alle unterschiedlichen Positionen prüfen (→ 2-Methylhexan, 3-Methylhexan). (3) Hauptkette nochmals kürzen, zwei Seitenketten anbringen usw. Wichtig: Immer prüfen, ob ein neues Gebilde wirklich verschieden von bereits gefundenen ist.
Was unterscheidet 2-Methylhexan von 3-Methylhexan?
Beide haben eine 6 C-Atome lange Hauptkette (Hexan) und eine Methylgruppe als Seitenkette – aber an verschiedenen Positionen: Bei 2-Methylhexan sitzt die Methylgruppe an C-2, bei 3-Methylhexan an C-3. Gleiche Summenformel, verschiedene Struktur → verschiedene Eigenschaften.
Warum hat 2,2,3-Trimethylbutan einen niedrigeren Siedepunkt als n-Heptan?
Je stärker verzweigt ein Alkan ist, desto kugelförmiger (kompakter) ist das Molekül – die Oberfläche ist kleiner. Damit werden die van-der-Waals-Kräfte zwischen den Molekülen schwächer. Weniger Anziehungskräfte bedeuten: Das Molekül lässt sich leichter aus dem flüssigen Zustand herauslösen → niedrigerer Siedepunkt. Mehr dazu auf der nächsten Seite: → Eigenschaften der Alkane.
Wie viele Isomere hat C₅H₁₂?
C5H12 (Pentan) hat 3 Konstitutionsisomere: n-Pentan (5 C unverzweigt), 2-Methylbutan (4 C-Kette + 1 Methylgruppe an C-2) und 2,2-Dimethylpropan (3 C-Kette + 2 Methylgruppen an C-2, auch „Neopentan" genannt). Zum Vergleich: C4H10 hat 2 Isomere, C6H14 hat 5 Isomere.
Lernkarten – Isomere und Nomenklatur
Klicke auf eine Karte, um die Antwort zu sehen.
Was sind Konstitutionsisomere? Nenne ein Kriterium.
Gleiche Summenformel, aber verschiedene Verknüpfung der Atome (→ verschiedene Strukturformel und verschiedene Eigenschaften).
Wie viele Konstitutionsisomere hat C7H16?
9 Isomere: n-Heptan · 2- und 3-Methylhexan · 2,2- / 2,3- / 2,4- / 3,3-Dimethylpentan · 3-Ethylpentan · 2,2,3-Trimethylbutan.
Wie viele Isomere hat C5H12? Nenne alle Namen.
3 Isomere: n-Pentan · 2-Methylbutan · 2,2-Dimethylpropan (Neopentan).
Warum sinkt der Siedepunkt mit steigendem Verzweigungsgrad?
Stärkere Verzweigung → kompakteres Molekül → kleinere Oberfläche → schwächere van-der-Waals-Kräfte → niedrigerer Siedepunkt.
Benenne: C-Kette mit 4 Atomen, je eine Methylgruppe an C-2 und C-3.
2,3-Dimethylbutan
(Butan = 4 C; zwei Methylgruppen an C-2 und C-3 → 2,3-Dimethyl; Summenformel: C6H14).
Weiter im Kapitel Alkane
← 1.6 Genfer Nomenklatur → 1.7 Eigenschaften der Alkane
🔁 Weiter in der Organik: Isomerien der Alkene (Kl. 10)
