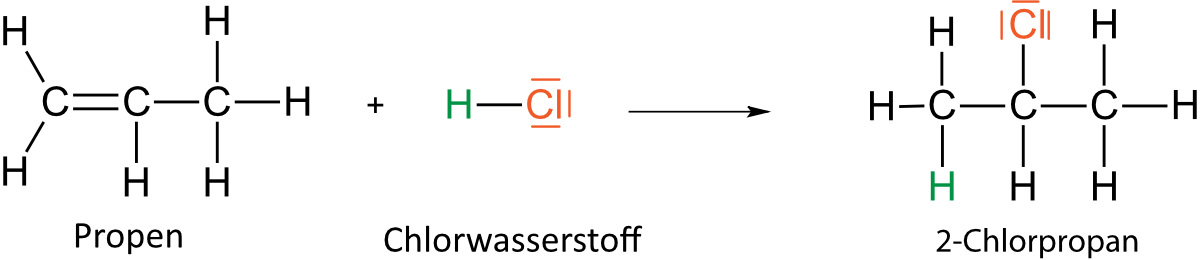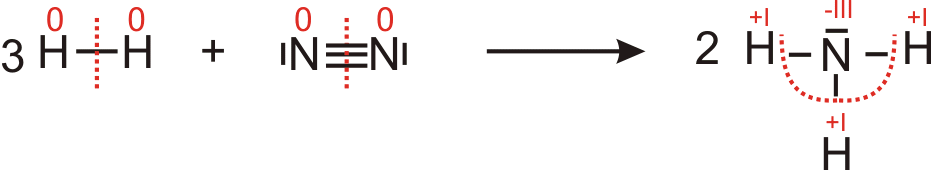Oxidationszahl
-
01.1 Methan
Was du auf dieser Seite lernst
Methan (CH₄) ist das einfachste Alkan und gleichzeitig der Einstieg in die Organische Chemie. Du lernst, wie man über die qualitative Elementaranalyse auf die Summenformel schließt, wie die Strukturformel und der Bindungswinkel aussehen, und warum die Verbrennung von Methan eine Redoxreaktion ist.
Grundlagen aus der 9. Klasse
Lewis-Formeln, Atombindung und Oxidationszahlen hast du in der 9. Klasse kennengelernt: → Lewis-Formeln (Kl. 9) · → Oxidationszahlen (Kl. 9)
1.1.1 Vorkommen
Methan kommt vor in: Erdgas, Sumpfgas, Biogas, Grubengas.
1.1.2 Eigenschaften
- farb- und geruchloses Gas
- geringere Dichte als Luft
- brennbar
1.1.3 Ermittlung der Summenformel (Molekülformel) und Strukturformel
a) Qualitative Analyse (Elementaranalyse)
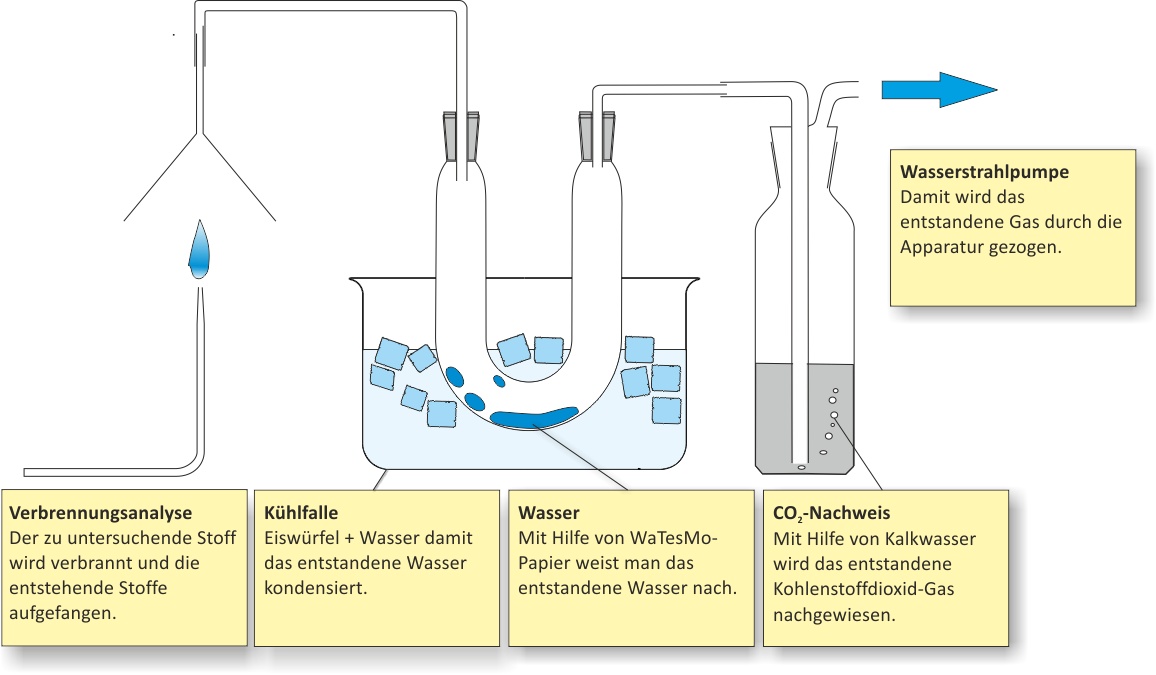
Hierfür wird der zu untersuchende Stoff verbrannt und die Verbrennungsprodukte bestimmt.
Bildet sich Wasser, ist Wasserstoff als Element vorhanden.
Kohlenstoff lässt sich als Ruß (unvollständige Verbrennung) oder als Kohlenstoffdioxid nachweisen. Der CO₂-Nachweis erfolgt mit der Kalkwasserprobe: Das entstandene Gas wird in Kalkwasser eingeleitet – eine Trübung zeigt CO₂ an.↑ Zum Vergrößern klicken
✕
- Nachweis von Wasserstoff → Bildung von Wasser → WaTesMo-Papier oder wasserfreies Kupfersulfat.
- Nachweis von C → Bildung von CO2 → Nachweis als CaCO3:
Ca(OH)2 (aq) + CO2 (g) → CaCO3 (s) + H2O (l)
Die Verbrennungsprodukte (Wasser, Kohlenstoffdioxid) zeigen, dass Methan Kohlenstoff, Wasserstoff und eventuell Sauerstoff enthält.
b) Bestimmung der molaren Masse
Mit der Gaswägung lässt sich die molare Masse von Methan bestimmen: M(Methan) = 16 g/mol · Molekülmasse 16 u.c) Summenformel: CH4
d) Strukturformel
Man zeichnet Methan meist mit einem Winkel von 90°. Dieser Winkel entspricht nicht dem tatsächlichen Bindungswinkel (vgl. unten). Man kann sich aber vorstellen, dass man direkt auf das Molekül blickt.↑ Zum Vergrößern klicken
✕ ✕
✕
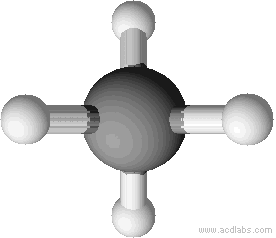
Tetraedrische Anordnung der Wasserstoffatome um das Kohlenstoffatom (Bindungswinkel 109,5°). Erklärung: größtmögliche Entfernung der Wasserstoffatome.
1.1.4 Vollständige Verbrennung
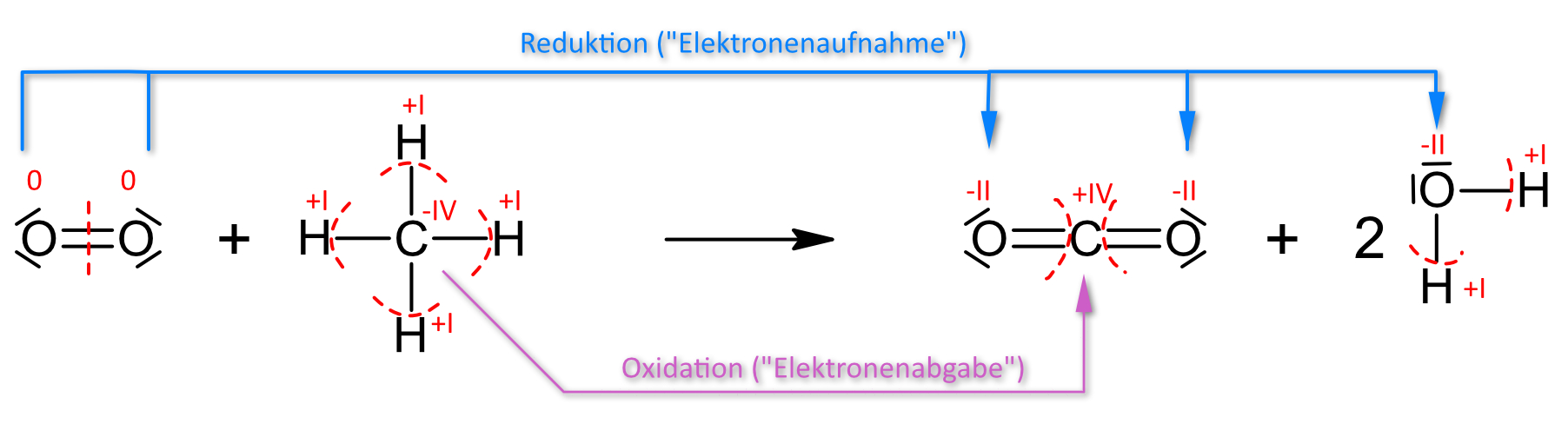
0 −IV +I +IV −II +I −II
2 O2 + CH4 → CO2 + 2 H2O ΔH = −888 kJ/mol↑ Zum Vergrößern klicken
✕
Hinweis: Wenn die Ermittlung der Oxidationszahlen Schwierigkeiten macht, kann man es hier nochmals nachlesen.
1 l Methan benötigt zur vollständigen Verbrennung 10 Liter Luft (2 l Sauerstoff).
Auf einen Blick – Methan
Summenformel
Methan: CH₄ · molare Masse 16 g/mol · einfachstes Alkan · allg. Formel der Alkane: CₙH₂ₙ₊₂ (hier n = 1).
Tetraeder
Die vier H-Atome ordnen sich tetraedrisch um das C-Atom an. Bindungswinkel: 109,5° (größtmögliche Abstoßung der Bindungselektronenpaare).
Elementaranalyse
Verbrennung → H₂O (Wassernachweis: WaTesMo) + CO₂ (Kalkwasserprobe: Trübung durch CaCO₃) → Methan enthält C und H.
Verbrennung
CH₄ + 2 O₂ → CO₂ + 2 H₂O · ΔH = −888 kJ/mol (exotherm). C wird von −IV auf +IV oxidiert; O von 0 auf −II reduziert.
Häufige Fragen – Methan
Wie weist man experimentell nach, dass Methan Kohlenstoff und Wasserstoff enthält?
Methan wird vollständig verbrannt. Die entstehenden Gase und Dämpfe werden durch zwei Nachweisreagenzien geleitet: Wassernachweis mit wasserfreiem Kupfersulfat (wird blau) oder WaTesMo-Papier (Blaufärbung zeigt Wasser an) → Methan enthält Wasserstoff. CO₂-Nachweis mit Kalkwasser Ca(OH)₂: Trübung durch CaCO₃-Bildung → Methan enthält Kohlenstoff.
Warum ist der Bindungswinkel in Methan 109,5° und nicht 90°?
Die vier bindenden Elektronenpaare stoßen sich gemäß dem VSEPR-Modell (Valence Shell Electron Pair Repulsion) so weit wie möglich ab. Maximale Abstoßung ergibt eine tetraedrische Anordnung mit einem Bindungswinkel von 109,5°. In der vereinfachten Strukturformel zeichnet man 90°-Winkel, weil man so tut, als würde man von oben auf das Molekül blicken.
Warum ist die Verbrennung von Methan eine Redoxreaktion?
Bei der Verbrennung ändert sich die Oxidationszahl des Kohlenstoffs von −IV (in CH₄) auf +IV (in CO₂) → Oxidation. Der Sauerstoff wird von 0 (O₂) auf −II (in CO₂ und H₂O) reduziert → Reduktion. Es findet also ein Elektronenübergang statt: Methan ist das Reduktionsmittel, Sauerstoff das Oxidationsmittel. → Oxidationszahlen (Kl. 9)
Was bedeutet ΔH = −888 kJ/mol bei der Verbrennung?
Das negative Vorzeichen zeigt, dass Energie abgegeben wird – die Reaktion ist exotherm. Pro Mol verbranntem Methan (= 16 g) werden 888 kJ Wärmeenergie freigesetzt. Das erklärt, warum Methan (Erdgas) als Energieträger zum Heizen und Kochen eingesetzt wird. Mehr zur Reaktionsenthalpie: → Enthalpie (Kursstufe)
Wo kommt Methan natürlich vor und warum ist es klimarelevant?
Methan kommt natürlich in Erdgas (Hauptbestandteil), Sumpfgas (Zersetzung organischer Stoffe unter Wasser), Biogas (Gärung) und Grubengas (Steinkohlebergbau) vor. Als Treibhausgas ist CH₄ etwa 25-mal klimawirksamer als CO₂ (bezogen auf 100 Jahre), weil es Infrarotstrahlung besonders effektiv absorbiert.
Lernkarten – Methan
Klicke auf eine Karte, um die Antwort zu sehen.
1Gib Summenformel, molare Masse und Bindungswinkel von Methan an.
Summenformel: CH₄
Molare Masse: 16 g/mol
Bindungswinkel: 109,5° (Tetraeder)
Struktur: 4 H-Atome tetraedrisch um C2Wie weist man bei der Elementaranalyse Kohlenstoff und Wasserstoff nach?
H-Nachweis:
WaTesMo-Papier oder CuSO₄ (wasserfrei) → Blaufärbung = H₂O vorhanden
C-Nachweis:
Kalkwasser Ca(OH)₂ → Trübung = CO₂ vorhanden3Stelle die vollständige Verbrennungsgleichung von Methan auf.
CH₄ + 2 O₂ → CO₂ + 2 H₂O
ΔH = −888 kJ/mol (exotherm)
Kontrolle: C: 1=1 ✓ · H: 4=4 ✓ · O: 4=4 ✓4Welche Oxidationszahlen hat Kohlenstoff in CH₄ und in CO₂? Was folgt daraus?
CH₄: C hat Oxidationszahl −IV
CO₂: C hat Oxidationszahl +IV
→ Oxidationszahl steigt → C wird oxidiert
→ Methan = Reduktionsmittel5Wieviel Liter Luft benötigt 1 l Methan zur vollständigen Verbrennung, und warum?
10 Liter Luft (≈ 2 l O₂, da Luft ≈ 21 % O₂)
CH₄ + 2 O₂ → … · Stöchiometrie: 1 Vol. CH₄ : 2 Vol. O₂
Luft enthält ~20 % O₂ → 2 l O₂ stecken in 10 l LuftWeiter im Kapitel Alkane
← 1 Alkane – Übersicht → 1.4 Butan → 1.5 Homologe Reihe
🔁 Grundlagen (Kl. 9): Lewis-Formeln · Oxidationszahlen
📚 Vertiefung Kursstufe: Enthalpie ΔH -
1 Freiwillig ablaufende Reaktionen
Was du auf dieser Seite lernst
Du wiederholst die Grundbegriffe der Redoxchemie und lernst sie neu zu durchdenken: Was bedeuten Oxidation und Reduktion im Sinne der Elektronenübertragung? Was ist ein korrespondierendes Redoxpaar? Am Beispiel Magnesium + Sauerstoff werden Reaktionsgleichung, Redoxschema und Elektronenbilanz erarbeitet.
Grundlagen aus der 9. Klasse
Den Versuch Magnesium + Sauerstoff und die erste Einführung in Oxidation und Reduktion kennst du bereits aus der 9. Klasse: → Magnesium und Sauerstoff (Kl. 9) · → Neue Definitionen: Oxidation / Reduktion (Kl. 9)
1.1 Wiederholung bekannter Begriffe und Definitionen
Versuch 1: Magnesium + Sauerstoff
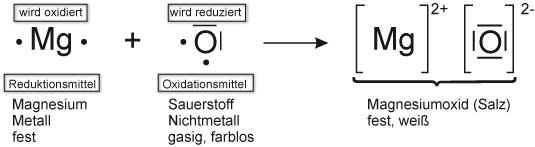
Magnesium verbrennt mit stark leuchtender Flamme. Ein weißer Feststoff bleibt übrig.
Formuliere die Reaktionsgleichungen und ein Redoxschema:
✕Lösung: Reaktionsgleichung und Redoxschema Mg + O₂
Zunächst vereinfacht atomar (natürlich liegt Sauerstoff molekular vor):
↑ Zum Vergrößern klicken
Vollständiger:
Reaktionsgleichung: 2 Mg + O2 → 2 MgO ΔH < 0
Redoxschema (allgemein):
↑ Zum Vergrößern klicken
↑ Zum Vergrößern klicken
 ✕
✕
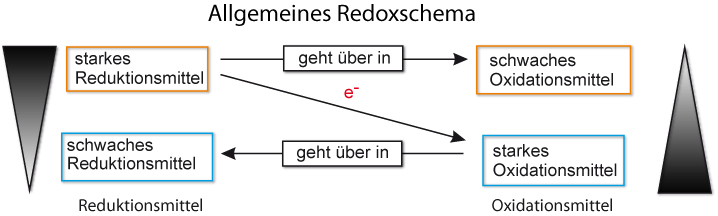 ✕
✕
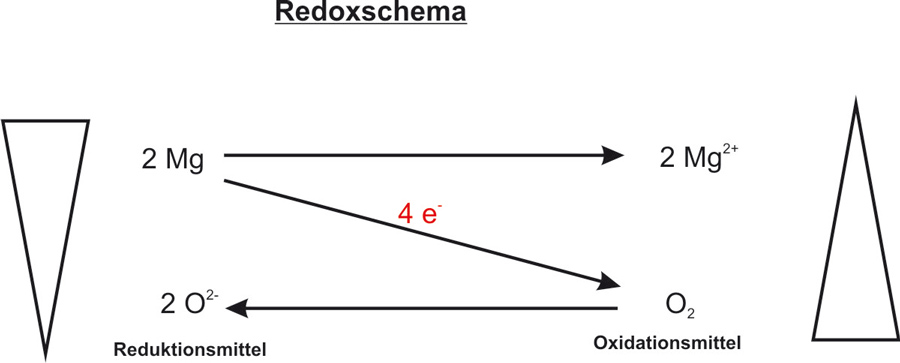
Einfach ist es, wenn man die Teilreaktionen (Oxidation und Reduktion) erstellt und dann erst die Redoxreaktion. Versucht mal diese zu formulieren:
Lösung: Teilreaktionen und Elektronenbilanz Mg + O₂
Oxidation: Mg → Mg2+ + 2 e− | · 2
Reduktion: O2 + 4 e− → 2 O2− | · 1
————————————————————————
Redoxreaktion: 2 Mg + O2 → 2 Mg2+ + 2 O2−Begriffe und Definitionen
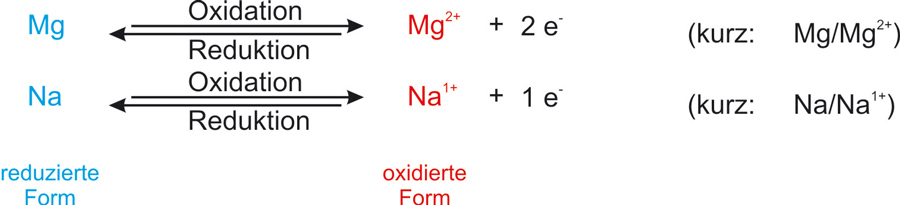
Oxidation = Elektronenabgabe; Erhöhung der Oxidationszahlen
Reduktion = Elektronenaufnahme; Erniedrigung der OxidationszahlenOxidationsmittel: Elektronenakzeptor („Elektronenräuber"); wird bei der Reaktion selbst reduziert. [Eselsbrücke: Putzmittel]
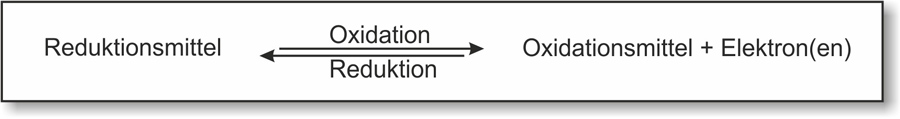
Reduktionsmittel: Elektronendonator („Elektronenspender"); wird bei der Reaktion selbst oxidiert.Redoxreaktionen: Reaktionen mit Elektronenübertragung.
Oxidation und Reduktion laufen gleichzeitig ab.Ein Reduktionsmittel gibt Elektronen ab, die es später wieder aufnehmen kann. Es wird also zu einem Oxidationsmittel.
↑ Zum Vergrößern klicken
✕
↑ Zum Vergrößern klicken
✕
Reduktionsmittel und Oxidationsmittel bilden ein korrespondierendes Redoxpaar:
↑ Zum Vergrößern klicken
✕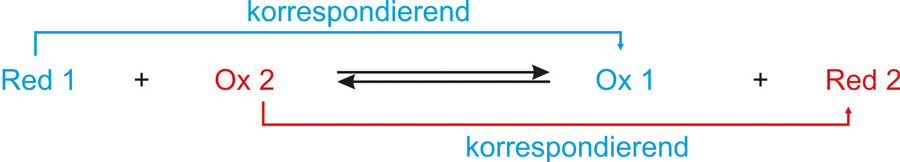
Die übliche Kurzschreibweise für ein Redoxpaar:
Reduzierte Form / oxidierte Form
Me / Men+Bei jeder Redoxreaktion sind zwei korrespondierende Redoxpaare beteiligt (analog: Protolysereaktion).
Wichtig – Elektronenbilanz
Die Zahl der abgegebenen und aufgenommenen Elektronen muss gleich sein – die Elektronenbilanz muss stimmen. Dazu multipliziert man die Teilreaktionen mit dem geeigneten gemeinsamen Vielfachen.
Auf einen Blick – die wichtigsten Aussagen
Oxidation
Oxidation = Elektronenabgabe. Die Oxidationszahl steigt. Das abgebende Teilchen heißt Reduktionsmittel und wird dabei selbst oxidiert.
Reduktion
Reduktion = Elektronenaufnahme. Die Oxidationszahl sinkt. Das aufnehmende Teilchen heißt Oxidationsmittel und wird dabei selbst reduziert.
Korrespondierendes Redoxpaar
Ox/Red-Form bilden ein Redoxpaar (Kurzschreibweise: Men+/Me). Bei jeder Redoxreaktion sind stets zwei korrespondierende Paare beteiligt.
Elektronenbilanz
Abgegebene Elektronen = aufgenommene Elektronen. Teilreaktionen mit dem gemeinsamen Vielfachen multiplizieren, bis die Bilanz stimmt.
Häufige Fragen – Freiwillig ablaufende Redoxreaktionen
Was ist der Unterschied zwischen Oxidation und Reduktion?
Oxidation ist die Abgabe von Elektronen – die Oxidationszahl des betroffenen Atoms steigt. Reduktion ist die Aufnahme von Elektronen – die Oxidationszahl sinkt. Beide Prozesse laufen immer gleichzeitig ab: Kein Teilchen gibt Elektronen ab, ohne dass ein anderes sie sofort aufnimmt. Man spricht daher von einer Redoxreaktion. Grundlagen: → Neue Definitionen Kl. 9
Was versteht man unter einem korrespondierenden Redoxpaar?
Ein korrespondierendes Redoxpaar besteht aus der oxidierten und der reduzierten Form eines Teilchens, z. B. Mg2+/Mg oder O/O2−. Kurzschreibweise: Ox-Form / Red-Form bzw. Men+/Me. Bei jeder Redoxreaktion sind genau zwei solcher Paare beteiligt – analog zu den zwei korrespondierenden Säure-Base-Paaren bei der Protolyse.
Wie unterscheiden sich Oxidationsmittel und Reduktionsmittel?
Das Oxidationsmittel ist der Elektronenakzeptor: Es nimmt Elektronen auf und wird dabei selbst reduziert (Eselsbrücke: „Putzmittel oxidiert = nimmt auf"). Das Reduktionsmittel ist der Elektronendonator: Es gibt Elektronen ab und wird dabei selbst oxidiert. Im Beispiel Mg + O₂ ist Mg das Reduktionsmittel, O₂ das Oxidationsmittel.
Wie muss die Elektronenbilanz bei einer Redoxreaktion aussehen?
Die Anzahl der abgegebenen Elektronen (Oxidation) muss exakt gleich der Anzahl der aufgenommenen Elektronen (Reduktion) sein. Um das zu erreichen, multipliziert man die Teilreaktionen mit geeigneten ganzzahligen Faktoren (kleinstes gemeinsames Vielfaches). Beispiel Mg + O₂: Die Oxidation (2 e− pro Mg) wird mit 2 multipliziert, die Reduktion (4 e− pro O₂) bleibt 1× → 4 e− auf beiden Seiten.
Was ist der Unterschied zwischen der atomaren und der molekularen Schreibweise der Reaktionsgleichung?
Die atomare Schreibweise (vereinfacht) betrachtet nur einzelne Atome und ist gut für das Verständnis der Elektronenübertragung. Die molekulare Schreibweise berücksichtigt den tatsächlichen Aggregatzustand der Stoffe (O₂ liegt molekular vor) und liefert die vollständige, ausbalancierte Reaktionsgleichung: 2 Mg + O2 → 2 MgO (ΔH < 0).
Lernkarten – Freiwillig ablaufende Redoxreaktionen
Klicke auf eine Karte, um die Antwort zu sehen.
1Was bedeutet Oxidation im Sinne der Elektronenübertragung?
Oxidation = Elektronenabgabe
→ Oxidationszahl steigt
→ Das abgebende Teilchen heißt Reduktionsmittel
(wird selbst oxidiert)2Was bedeutet Reduktion im Sinne der Elektronenübertragung?
Reduktion = Elektronenaufnahme
→ Oxidationszahl sinkt
→ Das aufnehmende Teilchen heißt Oxidationsmittel
(wird selbst reduziert)3Was versteht man unter einem korrespondierenden Redoxpaar? Gib die Kurzschreibweise an.
Ox-Form und Red-Form eines Teilchens bilden ein Paar.
Kurzschreibweise: Men+/Me
(erst oxidierte, dann reduzierte Form)
Bei jeder Redoxreaktion: 2 Paare4Woran erkennt man das Oxidationsmittel und das Reduktionsmittel in einer Reaktion?
Oxidationsmittel:
nimmt e− auf → wird reduziert
Reduktionsmittel:
gibt e− ab → wird oxidiert
Merke: Jedes Oxidationsmittel wird selbst reduziert.5Stelle die Teilreaktionen für 2 Na + Cl₂ → 2 NaCl auf und prüfe die Elektronenbilanz.
Oxidation: Na → Na+ + e− | ·2
Reduktion: Cl2 + 2 e− → 2 Cl− | ·1
————————————
2 Na + Cl2 → 2 Na+ + 2 Cl−
Bilanz: 2 e− abg. = 2 e− aufg. ✓Weiter im Kapitel Elektrochemie
← Elektrochemie – Übersicht → 1 Freiwillig ablaufende Reaktionen – Teil B → 1.2 Erstellung einer Redoxreihe
🔁 Grundlagen (Kl. 9): Magnesium + Sauerstoff · Neue Definitionen Oxidation / Reduktion · Oxidationszahlen
-
1.4 Weitere Redoxreaktionen
1.4 Weitere (komplexere) Redoxreaktionen
Die Redoxreaktionen sind nicht immer ganz so einfach. Hier zunächst ein Beispiel:
Aufgabe: Schaut, welche Redox-Paare in eurer Tabelle (siehe Moodle) vorhanden sind.
Beispiel 1: Reaktion von Kaliumdichromat mit Eisen(II)-SulfatTeilchen: Kaliumdichromat: 2 K¹⁺ Cr₂O₇²⁻
Eisen(II)-sulfat: Fe²⁺ SO₄²⁻Oxidation: Fe²⁺ → Fe³⁺ + e⁻ | x 6
Reduktion: Cr₂O₇²⁻ + 14 H₃O⁺ + 6 e⁻ → 2 Cr³⁺ + 21 H₂ORedox: Cr₂O₇²⁻ + 14 H₃O⁺ + 6 Fe²⁺ → Fe³⁺ + 2 Cr³⁺ + 21 H₂O
Rktgl: 6 FeSO₄ (aq) + K₂Cr₂O₇ (aq) + 7 H₂SO₄ (aq) → 3 Fe₂(SO₄)₃ (aq) + Cr₂(SO₄)₃ (aq) + K₂SO₄ (aq) + 7 H₂O (l)
Beispiel 2: „Cl-Gas kann im Labor gewonnen werden, indem man Kaliumdichromat mit Salzsäure reagieren lässt. Der Ansatz für die Reaktionsgleichung lautet:
__ Cr₂O₇²⁻ + __H₃O⁺ + __ Cl⁻ → ___Cr³⁺ + __Cl₂ + __ H₂ORichten Sie die Redoxgleichung ein. Formulieren Sie dazu die Teilgleichungen mit Oxidationszahlen.
{slider title="Lösung" open="false" class="icon"}
Oxidation: 2 Cl⁻ → Cl₂ + 2 e⁻ | x 3
Reduktion: Cr₂O₇²⁻ + 14 H₃O⁺ + 6 e⁻ → 2 Cr³⁺ + 21 H₂O
Redox: Cr₂O₇²⁻ + 14 H₃O⁺ + 6 Cl⁻ → 3 Cl₂ + 2 Cr³⁺ + 21 H₂O{/sliders}
Aufgabe 1: Geben Sie in den nachfolgenden Formeln die Oxidationszahlen aller Atome an:
(vgl. Tafelanschrieb)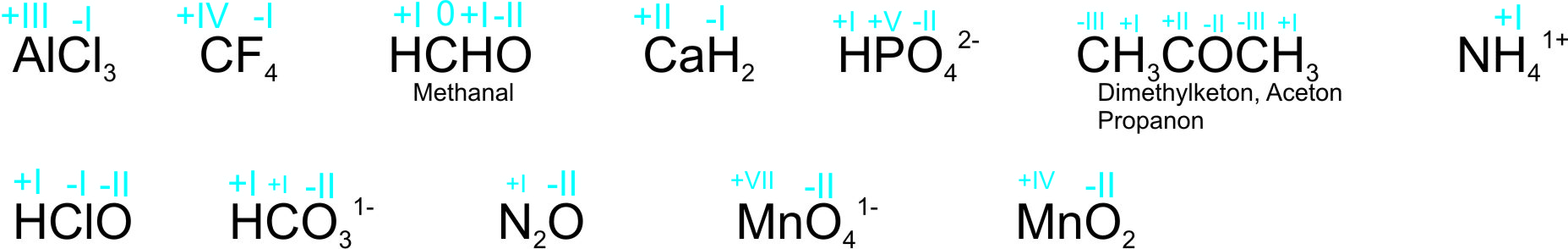
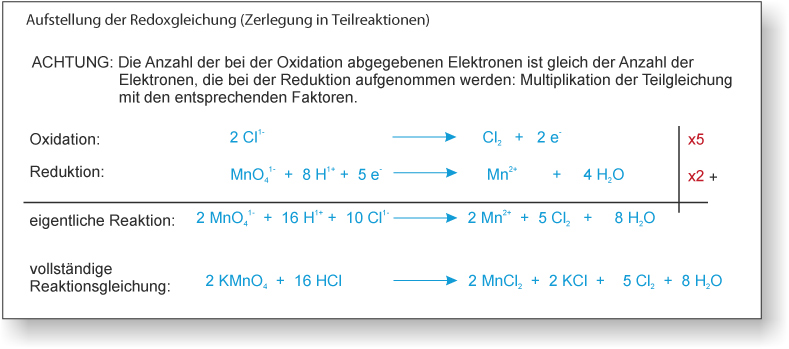
Aufgabe 2: Auf konzentrierte Kaliumpermangantlösung (KMnO₄) lässt man konzentrierte Salzsäure (HCl) einwirken. Bei dieser Reaktion entsteht u.a. Chlorgas und Mangan(II)-chlorid.
Vervollständigen Sie die folgenden Gleichungen für die obige Redoxreaktion (Vereinfacht wird statt H₃O⁺ H⁺ formuliert).{slider title="Tipp" open="false" class="icon"}
__ Cl⁻ + __ MnO₄¹⁻ + __ H⁺ → __ Cl₂ + __ Mn²⁺ + __ H₂O
{/sliders}
{slider title="Lösung" open="false" class="icon"}
{/sliders}
-
2.3 Katalytische Hydrierung
2.3 Katalytische Hydrierung
Hinweis: Markownikow-Regel: Bei Addition von z.B. Halogenwasserstoff bekommt das wasserstoffhaltigere C-Atom bekommt das H; das wasserstoffärmere Atom bekommt dann das Halogen. "Wer hat, dem wird gegeben" [bezieht sich auf H-Atome].
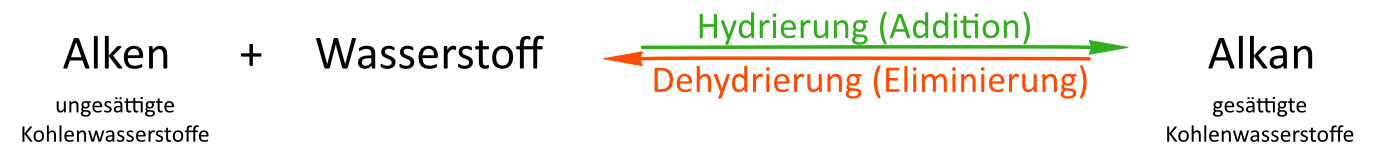
a) Alle Alkene lassen sich zu Alkane hydrieren.Hierbei handelt es sich um eine Redoxreaktion! Kohlenstoff wird reduziert (Oxidationszahlerniedrigung), H wird oxidiert. Hydrierung: Reduktion von Kohlenstoff
Die Dehydrierung ist die Umkehrung der Hydrierung: Oxidation von Kohlenstoff
b) Allgemein: Die Hydrierung ist eine umkehrbare Reaktion (Dehydrierung)
Eliminierungsreaktionen: Abspaltung kleiner Moleküle!
Übungsaufgabe:
An Propen wird Chlorwasserstoff addiert. Formuliere hierfür eine Reaktionsgleichung in Strukturformeln mit bindenden und nichtbindenden Elektronenpaaren. Beachte dabei auch die Markownikow-Regel (siehe oben).
{slider title="Lösung" open="false" class="icon"}
{/sliders}
-
3 Redoxreaktionen mit Molekülen - Oxidationszahlen
3 Redoxreaktionen mit Molekülen
Bei der Verbrennung von Stoffen bilden sich Oxide, ohne dass es zur Bildung von Ionen kommt. Beispiele dafür sind die Verbrennung von Wasserstoff, Kohlenstoff, Schwefel und Phosphor.
Um diese Reaktion als Redoxreaktion erfassen zu können, hat man als Hilfsgröße die Oxidationszahl eingeführt.
3.1 Oxidationszahl
Def.: Die Oxidationszahl gibt an, welche Ladung ein Atom in einem Molekül oder in einem anderen Teilchen hätte, wenn alle am Aufbau des Teilchens beteiligten Atome in Form von Ionen vorlägen.
Die sich für die Atome in der Verbindung ergebenden formalen Ladungszahlen nennt man Oxidationszahlen. Zur Unterscheidung von Ionenladungen werden sie als römische Zahlen an die Elementsymbole geschrieben.
Vorgehensweise: Vgl. dazu die zwei Beispiele 3.2 und 3.3 um die Schritte nachvollziehen zu können.
1. Schritt: Strukturformel erstellen.
2. Schritt: Ermittlung der Elektronegativität aller Elemente (siehe PSE) :
3. Schritt: Bindungselektronen werden formal dem elektronegativeren Bindungspartner zugeteilt. Besitzen die Bindungspartner die gleiche Elektronegativität erhalten sie je die Hälfte der Bindungselektronen.Faustregel: (Hinweis: Wann immer eindeutige Strukturformeln möglich sind, würde ich keine Faustregeln nutzen)
- Fluor immer: –I
- Wasserstoff: +I
- Sauerstoff: -II
- Halogene: -I (sofern nicht mit Sauerstoff oder einem elektronegativeren Halogen verbunden sind)
4. Schritt: Man bestimmt die Hauptgruppennummer des Elements und zählt dann die Elektronen, welche das Element jetzt "formal" hätte (vgl. 3. Schritt). Dann berechnet man entsprechend folgender Formel:
Oxidationszahl = Hauptgruppennummer des Elements – Elektronenanzahl im Molekül
Bsp. Sauerstoff im Wassermolekül: Oxidationszahl(O) = steht in der 6. Hauptgruppe = VI - 8 = -2 (bzw. - II)
Bsp. Wasserstoff im Wassermolekül: Oxidationszahl(H) = I - 0 = +1
5. Schritt: Kontrolle: Summe der Oxidationszahlen muss 0 sein (bei elektr. Neutralen Molekülen).
Mit Hilfe der Oxidationszahl lassen sich die Begriffe Oxidation und Reduktion neu fassen:Oxidation: Elektronenabgabe) bedeutet eine Erhöhung der Oxidationszahl.
Reduktion: (Elektronenaufnahme) bedeutet eine Erniedrigung der Oxidationszahl.
Redoxreaktionen: sind Vorgänge bei denen sich die Oxidationszahlen der beteiligten Atomarten ändern.3.2 Vollständige Verbrennung von Kohlenstoff
Kohlenstoff Sauerstoff Kohlenstoff(IV)-oxid
Atom Molekül Molekül

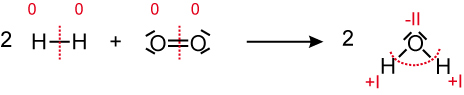
→ Kohlenstoff wird oxidiert, Sauerstoff wird reduziert.3.3 Reaktion von Wasserstoff mit Sauerstoff
Wasserstoff Sauerstoff Wasser
Oxidationszahlen von Wasserstoff wird positiver → Wasserstoff wird oxidiert
Oxidationszahlen von Sauerstoff wird negativer → Sauerstoff wird reduziert3.5 Reaktion von Wasserstoff mit Stickstoff zu Ammoniak (Ammoniaksynthese)
Oxidationszahlen von Wasserstoff wird positiver → Wasserstoff wurde oxidiert
Oxidationszahlen von Stickestoff wurde negativer → Stickstoff wurde reduziert3.6 Reaktion von Schwefel mit Sauerstoff zu Schwefeldioxid
Man muss nicht immer die Lewis-Formeln (Strukturformeln) zeichnen. Manchmal genügt es, nach den Faustregeln zu arbeiten.
Oxidationszahlen von Schwefel wird positiver → Schwefel wurde oxidiert
Oxidationszahlen von Sauerstoff wurde negativer → Sauerstoff wurde reduziert3.7 Synthese von Chlorwasserstoff aus den Elementen
Oxidationszahlen von Wasserstoff wird positiver → Wasserstoff wurde oxidiert
Oxidationszahlen von Chor wurde negativer → Chlor wurde reduziert3.8 Synthese von Schwefelwasserstoff aus den Elementen
Oxidationszahlen von Wasserstoff wird positiver → Wasserstoff wurde oxidiert
Oxidationszahlen von Schwefel wurde negativer → Schwefel wurde reduziert -
6.1.4 Aldehydnachweise
6.1.4 Aldehydnachweise
a) Schiffsche-Probe mit Fuchsinschwefliger Säure
Fuchsinschweflige Säure ergibt mit Aldehyden eine rotviolette Farbe. Dieser Aldehydnachweis beruht nicht auf der Reduktionswirkung von Aldehyden!
b) Tollens-Probe (Silberspiegel)
Versuchsaufbau (gilt auch für Fehling-Probe)
Versuchsdurchführung:
Schutzbrille aufsetzen, weite Ärmel hochkrempeln, Haare zurückbinden.
- Gib in das RG etwa zwei fingerbreit Silbernitratlösung.
- Füge mit der Pipette tropfenweise verdünnte Ammoniaklösung hinzu, bis sich der entstehende Niederschlag gerade wieder auflöst.
- Gib nun in das RG zwei fingerbreit Probelösung.
- Stelle das RG in das heiße Wasserbad.
Beobachtung:
Es bildet sich ein Silberspiegel auf der Innenseite des Reagenzglas.
Auswertung:
Es bedeutet, dass sich die Silber-Ionen zu elementarem Silber reduzierthaben. Da eine Reduktion nur zusammen mit einer Oxidationablaufen, muss etwas anderes oxidiert worden sein. Da es ein Aldehyd-Nachweisist, kann man davon ausgehen, dass das C-Atom der Aldehyd-Gruppe oxidiertwurde. Da diese Reaktion in alkalischer Lösung abläuft (Ammoniak wurde dazugegeben), formuliert man mit Hilfe von Hydroxid-Ionen (OH⁻).
c) Fehling-Reagenz
Versuchsdurchführung:
Schutzbrille aufsetzen, weite Ärmel hochkrempeln, Haare zurückbinden.- Gib in das RG etwa 5 ml Fehling 1-Lösung und dann 5 ml Fehling 2-Lösung.
- Füge ein Spatellöffel Glucose zu.
- Stelle das RG nach kurzem Schütteln in das heiße Wasserbad.
Beobachtung:
Es bildet sich ein roter Niederschlag von Kupfer(I)-Oxid (Cu₂O).Auswertung:
Diese Reaktion verläuft recht analog zum Silberspiegel (Tollens-Reagens). Nur wird hierbei das Metall-Ion nicht komplett reduziert, sondern das Cu²⁺ wird zu Cu¹⁺ reduziert, wobei es sich sofort mit einem Oxid-Ion verbindet und den rötlichen Niederschlag bildet. Sauerstofflieferant ist auch in diesem Fall wie bei Tollens-Probe das Hydroxid-Ionen, da eine alkalische Lösung vorliegt.
Aufgabe: Versucht mit Hilfe der oberen Gleichung jetzt die Reaktionsgleichungen für das Fehlingreagenz zu formulieren.
{slider title="Lösung" open="false" class="icon"}
{/sliders}
-
Elektrochemie - Übersicht
Was du auf dieser Seite findest
Diese Seite ist die Übersicht zum Kapitel Elektrochemie der Kursstufe (Baden-Württemberg). Du findest hier alle Themen von den freiwillig ablaufenden Redoxreaktionen über galvanische Zellen, Standardelektrodenpotential und die Nernst-Gleichung bis hin zur Elektrolyse – direkt verlinkt und mit kurzen Beschreibungen.
Grundlagen aus der 9. Klasse
Oxidation, Reduktion, Elektronenübertragung und Oxidationszahlen hast du bereits in der 9. Klasse kennengelernt: → Redoxreaktionen (Kl. 9) · → Oxidationszahlen
Elektrochemie I – Themen im Überblick
Kapitel 1
Freiwillig ablaufende Redoxreaktionen
Elektronenübertragung · Redoxpaare · Grundbegriffe
Kapitel 1.2
Erstellung einer Redoxreihe
Reaktionsfreudigkeit · edle und unedle Metalle
Kapitel 2
Galvanische Zellen · Daniell-Element
Halbzellen · Elektroden · metallische Bindung
Kapitel 2.2
Standardelektrodenpotential & NHE
Normalwasserstoffelektrode · Normalpotentiale
Kapitel 2.5
Elektrochemische Spannungsreihe
Standardpotentiale · EMK-Berechnung · Anwendung
Kapitel 2.7
Nernst-Gleichung
Konzentrationsabhängigkeit des Elektrodenpotentials
Kapitel 3
Elektrolyse
Erzwungene Redoxreaktionen · Zersetzungsspannung
Elektrochemie II – Anwendungen
Kapitel 4.1
Volta-Element
Historische galvanische Zelle · Polarisation
Kapitel 4.2
Bleiakkumulator
Aufladbare Zelle · Lade- und Entladevorgang
Kapitel 4.3
Brennstoffzelle
H₂/O₂-Zelle · Wasserstofftechnologie
Kapitel 4.7
Korrosion & Korrosionsschutz
Rosten · Sauerstoffkorrosion · → Schutzmaßnahmen
Vollständige Inhaltsübersicht
1 Freiwillig ablaufende Redoxreaktionen
- 1.1 Wiederholung bekannter Begriffe und Definitionen | → Teil B
- 1.2 Erstellung einer Redoxreihe | → Wiederholung Oxidationszahlen
- 1.3 Stellung des Redoxpaares (½ H₂ / H⁺ + 1 e⁻) in der Redoxreihe
- 1.4 Weitere Redoxreaktionen
2 Elektrochemische (Galvanische) Zellen
- 2.1 Daniell-Element
- 2.1a Metallische Bindung
-
2.2 Standardelektrodenpotential und NHE
- 2.2.1 Standardwasserstoffhalbzelle (Normalwasserstoffelektrode, NHE)
- 2.2.2 Standardelektrodenpotential von Zink
- 2.3 Festlegung für das Vorzeichen der Standardelektrodenpotentiale (Normalpotentiale)
- 2.4 Die elektromotorische Kraft (EMK)
- 2.5 Elektrochemische Spannungsreihe
- 2.6 Konzentrationszelle
- 2.7 Nernst-Gleichung
3 Elektrolyse
- 3.1 Elektrolyse einer Zinkbromid-Lösung (Zinkiodid)
- 3.2 Elektrolyse einer Kupfer(II)-chloridlösung
- 3.3 Zersetzungsspannung
4 Anwendungen (Elektrochemie II)
- 4.1 Volta-Element
- 4.2 Bleiakkumulator
- 4.3 Brennstoffzelle
- 4.4 Weitere Batterien | → Alkali-Mangan-Batterie
- 4.5 Akkumulatoren
- 4.6 Herstellung von Stoffen (erzwungene Redoxreaktionen) | → Raffination von Kupfer
- 4.7 Korrosion
Auf einen Blick – die wichtigsten Aussagen
Galvanische Zelle
In einer galvanischen Zelle läuft eine freiwillige Redoxreaktion ab. Das unedlere Metall wird oxidiert (Anode, Minuspol), das edlere Metall wird reduziert (Kathode, Pluspol).
Standardelektrodenpotential
Das Standardelektrodenpotential E° wird gegen die Normalwasserstoffelektrode (NHE) gemessen. Die EMK einer Zelle ergibt sich aus E°(Kathode) − E°(Anode).
Nernst-Gleichung
Die Nernst-Gleichung beschreibt, wie das Elektrodenpotential E von der Konzentration der Ionen abhängt: E = E° + (RT / nF) · ln([Ox]/[Red]).
Elektrolyse
Bei der Elektrolyse werden Redoxreaktionen durch elektrischen Strom erzwungen. Anode: Oxidation · Kathode: Reduktion – umgekehrt zur galvanischen Zelle.
Häufige Fragen – Elektrochemie
Was ist der Unterschied zwischen einer galvanischen Zelle und der Elektrolyse?
In einer galvanischen Zelle läuft eine thermodynamisch freiwillige Redoxreaktion ab – die Zelle erzeugt elektrischen Strom. Bei der Elektrolyse dagegen wird eine nicht-freiwillige Redoxreaktion durch von außen angelegten Strom erzwungen. In beiden Fällen gilt: An der Anode findet Oxidation, an der Kathode Reduktion statt – allerdings ist die Anode bei der galvanischen Zelle der Minuspol, bei der Elektrolyse der Pluspol. Mehr dazu: → Elektrolyse
Wie berechnet man die EMK (elektromotorische Kraft) einer elektrochemischen Zelle?
Die EMK (elektromotorische Kraft) einer galvanischen Zelle ergibt sich aus der Differenz der Standardelektrodenpotentiale beider Halbzellen: EMK = E°(Kathode) − E°(Anode). Das Metall mit dem höheren E°-Wert bildet die Kathode (Pluspol), das mit dem niedrigeren die Anode (Minuspol). Beispiel: Cu/Zn-Daniell-Element: EMK = +0,34 V − (−0,76 V) = 1,10 V. Details: → EMK
Was besagt die Nernst-Gleichung?
Die Nernst-Gleichung beschreibt die Abhängigkeit des Elektrodenpotentials E von der Konzentration der beteiligten Ionen: E = E° + (RT / nF) · ln([Ox]/[Red]), wobei R die universelle Gaskonstante (8,314 J·mol⁻¹·K⁻¹), T die Temperatur in Kelvin, n die Anzahl der übertragenen Elektronen und F die Faraday-Konstante (96 485 C·mol⁻¹) ist. Bei 25 °C vereinfacht sich das zu: E = E° + (0,0592 V / n) · lg([Ox]/[Red]). Mehr dazu: → Nernst-Gleichung
Warum wird Zink im Daniell-Element als Minuspol bezeichnet?
Zink hat ein niedrigeres Standardelektrodenpotential (E° = −0,76 V) als Kupfer (E° = +0,34 V). Zink ist das unedlere Metall und gibt leichter Elektronen ab (Oxidation). Die Zinkelektrode ist daher die Anode und gleichzeitig der Minuspol der galvanischen Zelle. Die Elektronen fließen über den äußeren Stromkreis zur Kupferelektrode (Kathode, Pluspol), wo Cu²⁺-Ionen reduziert werden.
Was versteht man unter der elektrochemischen Spannungsreihe?
Die elektrochemische Spannungsreihe (auch: Spannungsreihe der Metalle) ordnet Redoxpaare nach ihrem Standardelektrodenpotential E°, gemessen gegen die NHE bei Standardbedingungen (25 °C, 1 mol/L, 1 bar). Unedle Metalle (kleine E°-Werte, z. B. Li, K, Mg, Zn) stehen oben, edle Metalle (große E°-Werte, z. B. Cu, Ag, Au) unten. Mit ihr lässt sich ablesen, welche Redoxreaktionen freiwillig ablaufen und wie groß die EMK einer Zelle ist. Details: → Elektrochemische Spannungsreihe
Lernkarten – Elektrochemie
Klicke auf eine Karte, um die Antwort zu sehen.
1Was bedeutet „Oxidation" und „Reduktion" im Kontext der Elektrochemie?
Oxidation = Elektronenabgabe (an der Anode).
Reduktion = Elektronenaufnahme (an der Kathode).
Eselsbrücke: OIL RIG – Oxidation Is Loss, Reduction Is Gain.2Was ist das Standardelektrodenpotential E° und wie wird es gemessen?
E° ist das Potential einer Halbzelle gegenüber der Normalwasserstoffelektrode (NHE) bei Standardbedingungen (25 °C, 1 mol/L, 1 bar).
NHE: E° = 0,00 V (Referenz).3Nenne die Vorzeichen-Regel für Anode und Kathode bei galvanischer Zelle vs. Elektrolyse.
Galvanische Zelle:
Anode = Minuspol (−) | Kathode = Pluspol (+)
Elektrolyse:
Anode = Pluspol (+) | Kathode = Minuspol (−)4Was beschreibt die Nernst-Gleichung? Gib die Formel für 25 °C an.
Abhängigkeit des Potentials E von der Konzentration:
E = E° + (0,0592 V / n) · lg([Ox] / [Red])
n = Anzahl der übertragenen Elektronen
Bei [Ox] = [Red]: E = E°5Berechne die EMK des Daniell-Elements:
Cu²⁺/Cu: E° = +0,34 V | Zn²⁺/Zn: E° = −0,76 VKathode (Pluspol): Cu²⁺/Cu, E° = +0,34 V
Anode (Minuspol): Zn²⁺/Zn, E° = −0,76 V
EMK = E°(Kathode) − E°(Anode)
= 0,34 V − (−0,76 V) = 1,10 VWeiter im Kapitel Elektrochemie
→ Kapitel 1: Freiwillig ablaufende Redoxreaktionen → Elektrochemie II: Anwendungen
🔁 Grundlagen: Redoxreaktionen (Kl. 9) · Oxidationszahlen (Kl. 9)
📚 Weitere Kapitel der Kursstufe: Energetik & Thermodynamik · Gleichgewichtsreaktionen