Nachweisreaktionen
-
01.1 Methan
Was du auf dieser Seite lernst
Methan (CH₄) ist das einfachste Alkan und gleichzeitig der Einstieg in die Organische Chemie. Du lernst, wie man über die qualitative Elementaranalyse auf die Summenformel schließt, wie die Strukturformel und der Bindungswinkel aussehen, und warum die Verbrennung von Methan eine Redoxreaktion ist.
Grundlagen aus der 9. Klasse
Lewis-Formeln, Atombindung und Oxidationszahlen hast du in der 9. Klasse kennengelernt: → Lewis-Formeln (Kl. 9) · → Oxidationszahlen (Kl. 9)
1.1.1 Vorkommen
Methan kommt vor in: Erdgas, Sumpfgas, Biogas, Grubengas.
1.1.2 Eigenschaften
- farb- und geruchloses Gas
- geringere Dichte als Luft
- brennbar
1.1.3 Ermittlung der Summenformel (Molekülformel) und Strukturformel
a) Qualitative Analyse (Elementaranalyse)
Hierfür wird der zu untersuchende Stoff verbrannt und die Verbrennungsprodukte bestimmt.
Bildet sich Wasser, ist Wasserstoff als Element vorhanden.
Kohlenstoff lässt sich als Ruß (unvollständige Verbrennung) oder als Kohlenstoffdioxid nachweisen. Der CO₂-Nachweis erfolgt mit der Kalkwasserprobe: Das entstandene Gas wird in Kalkwasser eingeleitet – eine Trübung zeigt CO₂ an.↑ Zum Vergrößern klicken
✕
- Nachweis von Wasserstoff → Bildung von Wasser → WaTesMo-Papier oder wasserfreies Kupfersulfat.
- Nachweis von C → Bildung von CO2 → Nachweis als CaCO3:
Ca(OH)2 (aq) + CO2 (g) → CaCO3 (s) + H2O (l)
Die Verbrennungsprodukte (Wasser, Kohlenstoffdioxid) zeigen, dass Methan Kohlenstoff, Wasserstoff und eventuell Sauerstoff enthält.
b) Bestimmung der molaren Masse
Mit der Gaswägung lässt sich die molare Masse von Methan bestimmen: M(Methan) = 16 g/mol · Molekülmasse 16 u.c) Summenformel: CH4
d) Strukturformel
Man zeichnet Methan meist mit einem Winkel von 90°. Dieser Winkel entspricht nicht dem tatsächlichen Bindungswinkel (vgl. unten). Man kann sich aber vorstellen, dass man direkt auf das Molekül blickt.↑ Zum Vergrößern klicken
✕ ✕
✕
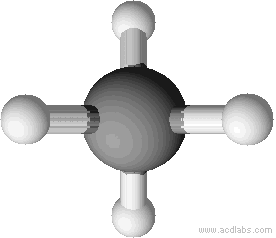
Tetraedrische Anordnung der Wasserstoffatome um das Kohlenstoffatom (Bindungswinkel 109,5°). Erklärung: größtmögliche Entfernung der Wasserstoffatome.
1.1.4 Vollständige Verbrennung
0 −IV +I +IV −II +I −II
2 O2 + CH4 → CO2 + 2 H2O ΔH = −888 kJ/mol↑ Zum Vergrößern klicken
✕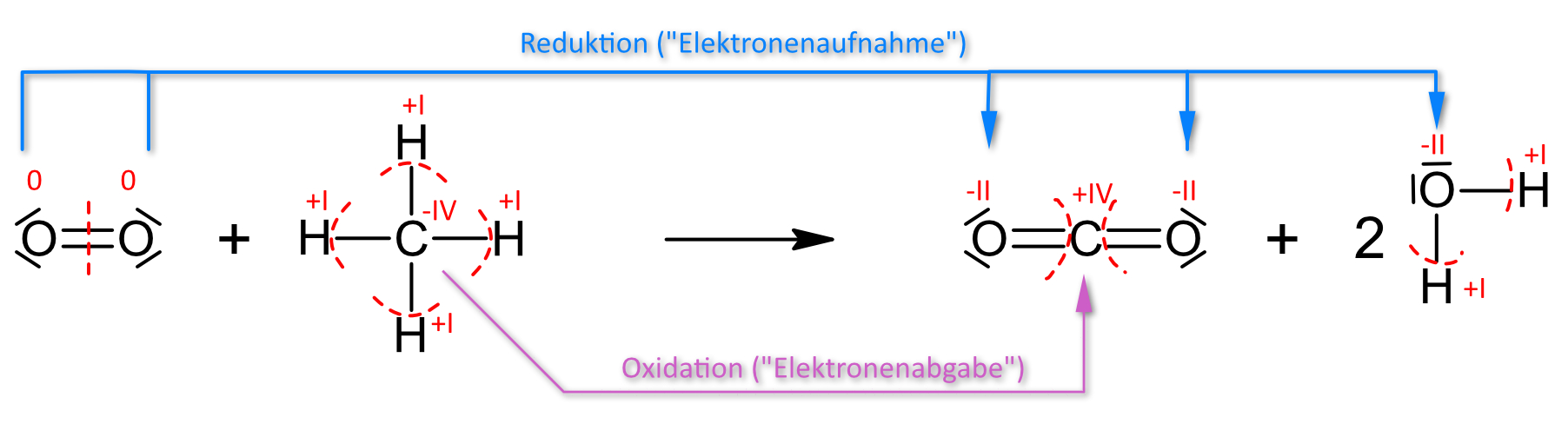
Hinweis: Wenn die Ermittlung der Oxidationszahlen Schwierigkeiten macht, kann man es hier nochmals nachlesen.
1 l Methan benötigt zur vollständigen Verbrennung 10 Liter Luft (2 l Sauerstoff).
Auf einen Blick – Methan
Summenformel
Methan: CH₄ · molare Masse 16 g/mol · einfachstes Alkan · allg. Formel der Alkane: CₙH₂ₙ₊₂ (hier n = 1).
Tetraeder
Die vier H-Atome ordnen sich tetraedrisch um das C-Atom an. Bindungswinkel: 109,5° (größtmögliche Abstoßung der Bindungselektronenpaare).
Elementaranalyse
Verbrennung → H₂O (Wassernachweis: WaTesMo) + CO₂ (Kalkwasserprobe: Trübung durch CaCO₃) → Methan enthält C und H.
Verbrennung
CH₄ + 2 O₂ → CO₂ + 2 H₂O · ΔH = −888 kJ/mol (exotherm). C wird von −IV auf +IV oxidiert; O von 0 auf −II reduziert.
Häufige Fragen – Methan
Wie weist man experimentell nach, dass Methan Kohlenstoff und Wasserstoff enthält?
Methan wird vollständig verbrannt. Die entstehenden Gase und Dämpfe werden durch zwei Nachweisreagenzien geleitet: Wassernachweis mit wasserfreiem Kupfersulfat (wird blau) oder WaTesMo-Papier (Blaufärbung zeigt Wasser an) → Methan enthält Wasserstoff. CO₂-Nachweis mit Kalkwasser Ca(OH)₂: Trübung durch CaCO₃-Bildung → Methan enthält Kohlenstoff.
Warum ist der Bindungswinkel in Methan 109,5° und nicht 90°?
Die vier bindenden Elektronenpaare stoßen sich gemäß dem VSEPR-Modell (Valence Shell Electron Pair Repulsion) so weit wie möglich ab. Maximale Abstoßung ergibt eine tetraedrische Anordnung mit einem Bindungswinkel von 109,5°. In der vereinfachten Strukturformel zeichnet man 90°-Winkel, weil man so tut, als würde man von oben auf das Molekül blicken.
Warum ist die Verbrennung von Methan eine Redoxreaktion?
Bei der Verbrennung ändert sich die Oxidationszahl des Kohlenstoffs von −IV (in CH₄) auf +IV (in CO₂) → Oxidation. Der Sauerstoff wird von 0 (O₂) auf −II (in CO₂ und H₂O) reduziert → Reduktion. Es findet also ein Elektronenübergang statt: Methan ist das Reduktionsmittel, Sauerstoff das Oxidationsmittel. → Oxidationszahlen (Kl. 9)
Was bedeutet ΔH = −888 kJ/mol bei der Verbrennung?
Das negative Vorzeichen zeigt, dass Energie abgegeben wird – die Reaktion ist exotherm. Pro Mol verbranntem Methan (= 16 g) werden 888 kJ Wärmeenergie freigesetzt. Das erklärt, warum Methan (Erdgas) als Energieträger zum Heizen und Kochen eingesetzt wird. Mehr zur Reaktionsenthalpie: → Enthalpie (Kursstufe)
Wo kommt Methan natürlich vor und warum ist es klimarelevant?
Methan kommt natürlich in Erdgas (Hauptbestandteil), Sumpfgas (Zersetzung organischer Stoffe unter Wasser), Biogas (Gärung) und Grubengas (Steinkohlebergbau) vor. Als Treibhausgas ist CH₄ etwa 25-mal klimawirksamer als CO₂ (bezogen auf 100 Jahre), weil es Infrarotstrahlung besonders effektiv absorbiert.
Lernkarten – Methan
Klicke auf eine Karte, um die Antwort zu sehen.
1Gib Summenformel, molare Masse und Bindungswinkel von Methan an.
Summenformel: CH₄
Molare Masse: 16 g/mol
Bindungswinkel: 109,5° (Tetraeder)
Struktur: 4 H-Atome tetraedrisch um C2Wie weist man bei der Elementaranalyse Kohlenstoff und Wasserstoff nach?
H-Nachweis:
WaTesMo-Papier oder CuSO₄ (wasserfrei) → Blaufärbung = H₂O vorhanden
C-Nachweis:
Kalkwasser Ca(OH)₂ → Trübung = CO₂ vorhanden3Stelle die vollständige Verbrennungsgleichung von Methan auf.
CH₄ + 2 O₂ → CO₂ + 2 H₂O
ΔH = −888 kJ/mol (exotherm)
Kontrolle: C: 1=1 ✓ · H: 4=4 ✓ · O: 4=4 ✓4Welche Oxidationszahlen hat Kohlenstoff in CH₄ und in CO₂? Was folgt daraus?
CH₄: C hat Oxidationszahl −IV
CO₂: C hat Oxidationszahl +IV
→ Oxidationszahl steigt → C wird oxidiert
→ Methan = Reduktionsmittel5Wieviel Liter Luft benötigt 1 l Methan zur vollständigen Verbrennung, und warum?
10 Liter Luft (≈ 2 l O₂, da Luft ≈ 21 % O₂)
CH₄ + 2 O₂ → … · Stöchiometrie: 1 Vol. CH₄ : 2 Vol. O₂
Luft enthält ~20 % O₂ → 2 l O₂ stecken in 10 l LuftWeiter im Kapitel Alkane
← 1 Alkane – Übersicht → 1.4 Butan → 1.5 Homologe Reihe
🔁 Grundlagen (Kl. 9): Lewis-Formeln · Oxidationszahlen
📚 Vertiefung Kursstufe: Enthalpie ΔH -
02 Alkene
Was du in diesem Kapitel lernst
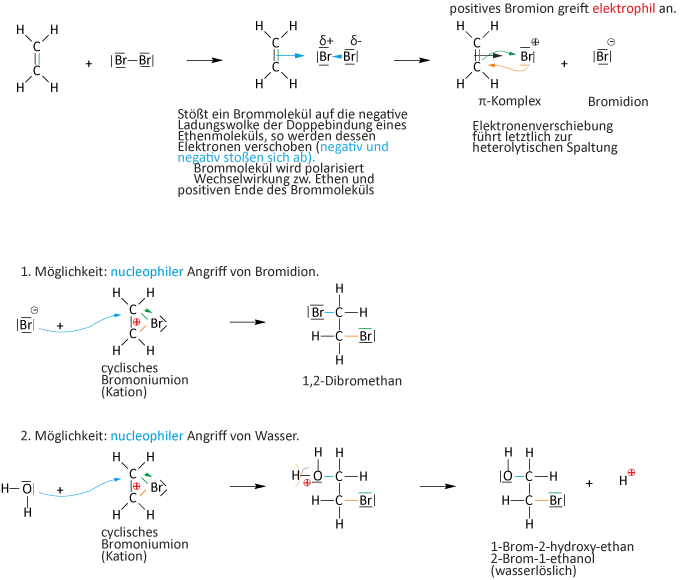
Alkene sind Kohlenwasserstoffe mit mindestens einer C=C-Doppelbindung – der charakteristischen funktionellen Gruppe dieser Verbindungsklasse. Am Beispiel des Ethens (C2H4) lernst du Aufbau, Eigenschaften und typische Reaktionen der Alkene kennen: von der Bromwasserprobe über die cis-trans-Isomerie bis zur katalytischen Hydrierung.
Grundlagen aus der 10. Klasse
Alkene bauen direkt auf dem Wissen über die gesättigten Kohlenwasserstoffe auf – wiederhole bei Bedarf: → 1. Alkane – Homologe Reihe, Genfer Nomenklatur, radikalische Substitution
Kapitelübersicht – 2. Alkene
Klicke auf eine Kachel, um direkt zum Unterkapitel zu springen.
H₂C=CH₂2.1
Ethen
Eigenschaften · Summenformel · Strukturformel · Vorkommen & Verwendung
Br₂2.1.5
Nachweis von Alkenen
Bromwasserprobe · Elektrophile Addition · Reaktionsgleichung
cis
trans2.1.6 / 2.1.7
Isomerien von Alkenen
Konstitutions-Isomerie · cis-trans-Isomerie · (E/Z)-Nomenklatur
But-2-en2.2
Nomenklatur der Alkene
IUPAC-Benennung · Lokanten · Übungsaufgaben
+H₂/Ni2.3
Katalytische Hydrierung
Hydrierung ⇔ Eliminierung · Gleichgewicht · Katalysator Ni / Pt
sp²
sp³2.4
Vergleich Ethen – Ethan
Reaktivität · sp²- vs. sp³-Hybridisierung · π-Elektronensystem
Auf einen Blick – die wichtigsten Aussagen
Funktionelle Gruppe
Alkene sind ungesättigte Kohlenwasserstoffe. Ihre charakteristische funktionelle Gruppe ist die C=C-Doppelbindung (σ- + π-Bindung). Allgemeine Formel: CnH2n.
Nachweis
Die Bromwasserprobe weist C=C-Doppelbindungen nach: Braunes Bromwasser wird durch Additionsreaktion entfärbt – eindeutiger Nachweis auf Mehrfachbindungen.
cis-trans-Isomerie
Die Doppelbindung blockiert die freie Rotation um die C=C-Achse. Dadurch entstehen räumlich verschiedene cis- und trans-Isomere mit unterschiedlichen Eigenschaften.
Reaktionstyp
Typisch für Alkene ist die elektrophile Addition: Die Doppelbindung wird geöffnet, Atome oder Gruppen lagern sich an (z. B. H2, Br2, HBr).
Häufige Fragen – Alkene
Was sind Alkene und wie unterscheiden sie sich von Alkanen?
Alkene sind Kohlenwasserstoffe mit mindestens einer C=C-Doppelbindung. Im Gegensatz zu den gesättigten Alkanen (nur Einfachbindungen) sind Alkene ungesättigt: Die Doppelbindung besteht aus einer σ-Bindung und einer π-Bindung. Die allgemeine Summenformel lautet CnH2n. Das einfachste Alken ist Ethen (C2H4). Alkene sind durch ihre Doppelbindung reaktiver als Alkane; ihr typischer Reaktionstyp ist die elektrophile Addition, nicht die radikalische Substitution der Alkane.
Wie weist man eine C=C-Doppelbindung nach?
Den klassischen Nachweis liefert die Bromwasserprobe: Braunes Bromwasser (Br2 in Wasser) wird durch Additionsreaktion entfärbt, weil das Brom an die Doppelbindung addiert wird. Gleichung am Beispiel Ethen: C2H4 + Br2 → C2H4Br2 (1,2-Dibromethan). Der Test ist eindeutig für alle Verbindungen mit Mehrfachbindungen. → 2.1.5 Nachweis von Alkenen
Was ist cis-trans-Isomerie, und wann tritt sie auf?
Die C=C-Doppelbindung blockiert die freie Drehbarkeit um die Bindungsachse. Wenn an beiden Doppelbindungskohlenstoffen je zwei verschiedene Substituenten sitzen, entstehen zwei räumlich unterschiedliche Isomere: Im cis-Isomer (= Z-Form: zusammen) stehen die gleichartigen Gruppen auf derselben Seite der Doppelbindung; im trans-Isomer (= E-Form: entgegen) auf gegenüberliegenden Seiten. Beispiel: cis-But-2-en und trans-But-2-en haben dieselbe Summenformel (C4H8), aber verschiedene Siedepunkte. → 2.1.6/2.1.7 Isomerien von Alkenen
Wie werden Alkene nach IUPAC benannt?
Die Nomenklatur der Alkene folgt denselben Grundregeln wie bei den Alkanen, mit Besonderheiten: (1) Die längste Kette, die die Doppelbindung enthält, ist die Hauptkette. (2) Sie wird so nummeriert, dass die Doppelbindung die niedrigstmögliche Lokante erhält. (3) Die Endung lautet „-en" (mehrere Doppelbindungen: -dien, -trien). (4) Die Position der Doppelbindung steht als Lokant vor der Endung: z. B. But-1-en, nicht 1-Buten (moderne IUPAC-Schreibweise). Bei cis-trans-Isomeren wird das Konfigurationspräfix vorangestellt: cis-But-2-en oder (Z)-But-2-en. → 2.2 Nomenklatur der Alkene
Was ist katalytische Hydrierung, und wie verhält sie sich zur Eliminierung?
Katalytische Hydrierung und Eliminierung sind Umkehrreaktionen: Bei der Hydrierung wird H2 mithilfe eines Nickel- oder Platin-Katalysators an die C=C-Doppelbindung addiert → Alken wird zu Alkan (z. B. C2H4 + H2 → C2H6). Bei der Eliminierung wird H2 unter hoher Temperatur abgespalten → Alkan wird zu Alken. Die Gesamtreaktion ist umkehrbar: Ethen ⇔ Ethan. Wichtig: Der Katalysator beeinflusst nur die Reaktionsgeschwindigkeit, verschiebt aber die Gleichgewichtslage nicht. → 2.3 Katalytische Hydrierung
Lernkarten – Alkene
Klicke auf eine Karte, um die Antwort zu sehen.
1Was ist die funktionelle Gruppe der Alkene, und woraus besteht sie?
Die C=C-Doppelbindung. Sie besteht aus einer σ-Bindung (Überlappung entlang der Achse) und einer π-Bindung (seitliche Überlappung). Alkene sind deshalb ungesättigt und reaktiver als Alkane.
2Wie lautet die allgemeine Formel der Alkene? Nenne die ersten vier mit Formel.
CnH2n (n ≥ 2)
Ethen C2H4 · Propen C3H6
Buten C4H8 · Penten C5H103Wie funktioniert der Bromwassertest? Was beobachtet man?
Braunes Bromwasser wird mit dem Alken gemischt. Das Bromwasser entfärbt sich, weil Br2 durch elektrophile Addition an die C=C-Doppelbindung gebunden wird. → Nachweis auf Mehrfachbindung.
4Wann tritt cis-trans-Isomerie auf? Was unterscheidet cis von trans?
Wenn an beiden C-Atomen der C=C-Bindung je zwei verschiedene Substituenten sitzen. cis: gleichartige Gruppen auf einer Seite; trans: auf gegenüberliegenden Seiten. Freie Rotation um die Doppelbindung ist nicht möglich.
5Berechne: Wie viel g H2 werden benötigt, um 28 g Ethen vollständig zu hydrieren?
C2H4 + H2 → C2H6
M(C2H4) = 28 g/mol → n = 1 mol
Stöchiometrie 1:1 → n(H2) = 1 mol
m(H2) = 1 mol · 2 g/mol = 2 g H2
Weiter im Fach Chemie / 10. Klasse
← 1. Alkane → 3. Alkine ↑ Übersicht 10. Klasse
🔭 Vertiefung in der Kursstufe: Aromaten – Benzol und seine Derivate · Cycloalkane
-
02.1.5 Nachweis von Alkenen (Mehrfachbindungen)
2.1.5 Nachweis von Alkenen (Doppelbindung)
Versuch: Ein Erlenmeyerkolben wird unter Wasser mit 250 ml Ethen gefüllt, anschließend werden 0,5 ml Brom dazugegeben und mit dem Stopfen verschlossen.
Alternativ: Hexen + Bromwasser (VORSICHT FALLS MAN BROM NIMMT ⇨ heftige Reaktion)
Beobachtung:
Die Bromfarbe verschwindet; Volumenabnahme; der Erlenmeyerkolben wird warm; es entsteht ein flüssiges Produkt, die Dichte ist größer als 1 g/cm³.Auswertung:
Zwei Hypothesen:I) Substitution:
II) Addition:
ErgebnisBei der Reaktion Ethen + Brom entsteht (fast) nur ein Reaktionsprodukt. „Bromwasserstoffnebel“ waren kaum zu sehen. Es fand somit eine Addition statt.
Additionsreaktionen: Reaktionen bei denen sich zwei Moleküle zu einem Molekül vereinigen! Es kommt dabei zur Anlagerung von Atomen oder Atomgruppen an Doppelbindungen (Mehrfachbindun-gen).
Reaktionsmechanismus: AE-Reaktionen (elektrophile Addition)
= typische Reaktion von Alkenen
-
03 Alkine
Was du in diesem Kapitel lernst
Alkine sind Kohlenwasserstoffe mit mindestens einer C≡C-Dreifachbindung – noch reaktiver als die Alkene. Das wichtigste Alkin ist Ethin (Acetylen): du lernst seine Eigenschaften, seine technische Herstellung aus Calciumcarbid und die für Alkine typischen zweistufigen Additionsreaktionen kennen.
Grundlagen aus der 10. Klasse
Alkine bauen auf dem Wissen über ungesättigte Verbindungen auf – wiederhole bei Bedarf: → 2. Alkene – C=C-Doppelbindung, Bromwasserprobe, Additionsreaktion
Kapitelübersicht – 3. Alkine
Klicke auf eine Kachel, um direkt zum Unterkapitel zu springen.
3.1
Ethin (Acetylen)
Physikalische & chemische Eigenschaften · Summenformel C2H2 · Strukturformel · Bananenbindung
→ 3.1.1 Eigenschaften · 3.1.2 Formelermittlung3.1.3 – 3.1.5
Herstellung & Verwendung
Herstellung aus CaC2 · Carbidlampe · Verwendung als Brenngas & Ausgangsstoff
→ 3.1.3 Herstellung · 3.1.4 Carbidlampe · 3.1.5 Verwendung3.2
Reaktionstyp bei Alkinen
Elektrophile Addition · Bromierung · Wasseranlagerung · Übungsaufgaben
→ 3.2 Reaktionstyp & Übungen
Auf einen Blick – die wichtigsten Aussagen
Funktionelle Gruppe
Alkine besitzen eine C≡C-Dreifachbindung (1 σ- + 2 π-Bindungen). Die Bindungslänge ist mit 120 pm kürzer als bei der Doppelbindung (134 pm). Allgemeine Formel: CnH2n−2.
Herstellung
Ethin entsteht aus Calciumcarbid und Wasser: CaC2 + 2 H2O → C2H2 + Ca(OH)2. Diese Reaktion liefert das Gas auch in der Carbidlampe.
Reaktionstyp
Alkine reagieren durch elektrophile Addition. Die Reaktion läuft zweistufig ab: erst entsteht ein Alken-Zwischenprodukt, dann wird erneut addiert → schließlich ein Alkan oder Derivat.
Linearstruktur
Ethin ist linear: alle vier Atome liegen auf einer Geraden (Bindungswinkel 180°). Die Dreifachbindung besteht aus drei „Bananenbindungen" (sp-Hybridisierung).
Häufige Fragen – Alkine
Was sind Alkine, und was unterscheidet sie von Alkenen?
Alkine sind Kohlenwasserstoffe mit mindestens einer C≡C-Dreifachbindung, bestehend aus einer σ-Bindung und zwei π-Bindungen. Die allgemeine Formel lautet CnH2n−2 (noch zwei H-Atome weniger als bei Alkenen: CnH2n). Alkine sind durch die Dreifachbindung noch reaktiver als Alkene. Das einfachste Alkin ist Ethin (C2H2), auch Acetylen genannt. Wie Alkene zeigen Alkine elektrophile Additionsreaktionen, jedoch oft zweistufig.
Wie wird Ethin (Acetylen) technisch hergestellt?
Ethin lässt sich aus Calciumcarbid (CaC2) und Wasser herstellen. Reaktionsgleichung: CaC2 + 2 H2O → C2H2 + Ca(OH)2. Calciumcarbid wird in der Carbidlampe (Grubenlampe) genutzt: Das entstehende Ethin verbrennt mit einer hellen, stark leuchtenden Flamme. Industriell wird Ethin heute hauptsächlich durch Cracken von Erdgas gewonnen. → 3.1.3 Herstellung
Was ist die Besonderheit der linearen Struktur von Ethin?
Beim Ethin sind alle vier Atome linear angeordnet (Bindungswinkel 180°, sp-Hybridisierung). Die C≡C-Dreifachbindung besteht nach dem Bananenbindungsmodell aus drei gebogenen Bindungen (σ + 2 π). Die Bindungslänge beträgt nur 120 pm (zum Vergleich: C=C 134 pm, C–C 154 pm). Diese kompakte Struktur erklärt die hohe Reaktivität und die ausgeprägte elektrophile Addition. → 3.1 Ethin
Wie verläuft die Bromierung von Ethin – und warum ist sie zweistufig?
Ethin reagiert mit Brom in einer elektrophilen Addition, die zweistufig abläuft: In der ersten Stufe addiert Br2 an die Dreifachbindung → es entsteht das Zwischenprodukt trans-1,2-Dibromethen (noch eine Doppelbindung vorhanden). In der zweiten Stufe reagiert dieses mit weiterem Br2 → 1,1,2,2-Tetrabromethan (gesättigtes Endprodukt). Wird Br2 im Unterschuss eingesetzt, kann man die Reaktion auf der Dibromstufe stoppen. → 3.2 Reaktionstyp
Welche Verwendungen hat Ethin in Industrie und Technik?
Ethin (Acetylen) wird vielfältig genutzt: (1) Autogenschweißen und Schneiden: Die Verbrennung mit Sauerstoff erzeugt eine Flamme von über 3000 °C. (2) Ausgangsstoff in der Chemie: Aus Ethin werden wichtige Kunststoffe und Lösungsmittel hergestellt (z. B. PVC über Vinylchlorid). (3) Carbidlampen: Historisch als tragbare Lichtquelle in Bergbau und Feuerwehr. (4) Bei Pflanzen spielt das analoge Ethylen (= Ethen) als Phytohormon eine Rolle – Ethin kann diese Wirkung verstärken.
Lernkarten – Alkine
Klicke auf eine Karte, um die Antwort zu sehen.
1Was ist die funktionelle Gruppe der Alkine, und woraus besteht sie?
Die C≡C-Dreifachbindung. Sie besteht aus einer σ-Bindung + zwei π-Bindungen. Bindungslänge: 120 pm. Hybridisierung: sp. Alle vier Atome in Ethin sind linear angeordnet (180°).
2Wie lautet die allgemeine Formel der Alkine? Nenne Ethin und Propin mit Formel.
CnH2n−2 (n ≥ 2)
Ethin: C2H2 (HC≡CH)
Propin: C3H4 (CH3–C≡CH)3Wie wird Ethin aus Calciumcarbid hergestellt? Nenne die Reaktionsgleichung.
CaC2 + 2 H2O
→ C2H2 + Ca(OH)2
Calciumcarbid reagiert mit Wasser zu Ethin und Calciumhydroxid.4Wie verläuft die Bromierung von Ethin – welche zwei Stufen gibt es?
Stufe 1: C2H2 + Br2 → C2H2Br2 (trans-1,2-Dibromethen, noch C=C)
Stufe 2: + Br2 → C2H2Br4 (1,1,2,2-Tetrabromethan)5Berechne: Wie viel g Br2 werden benötigt, um 26 g Ethin vollständig zu tetrabromieren?
C2H2 + 2 Br2 → C2H2Br4
M(C2H2) = 26 g/mol → n = 1 mol
n(Br2) = 2 mol → m = 2 · 160 g/mol = 320 g Br2
Weiter im Fach Chemie / 10. Klasse
← 2. Alkene → 5. Alkohole ↑ Übersicht 10. Klasse
🔭 Vertiefung in der Kursstufe: Cycloalkane · Aromaten – Benzol und seine Derivate
-
04.1 Monosaccharide
4.1 Monosaccharide
4.1.1 Glucose - Traubenzucker
Vorkommen: Trauben, Früchte
a) physikalische Eigenschaften- Aggregatzustand: fest; Schmelzpunkt um 146°C; weiteres Erhitzen führt zur Zersetzung.
Folgerung: Glucose besitzt hohe zwischenmolekulare Kräfte (Vermutung: H-Brückenbindung) und van-der-Waals-Kräfte.
- Löslichkeit:
Glucose löst sich sehr gut in Wasser (67g/100ml), dagegen löst sich Glucose nicht in Benzin. Eine wässrige Glucoselösung zeigt (fast) keine elektrische Leitfähigkeit.
Folgerung: Glucose enthält polare Gruppen, die mit Wasser H-Brücken eingehen können. Es entsteht keine Ionen.
b) qualitative Elementaranalyse
Reaktion von Glucose mit konzentrierter Schwefelsäure: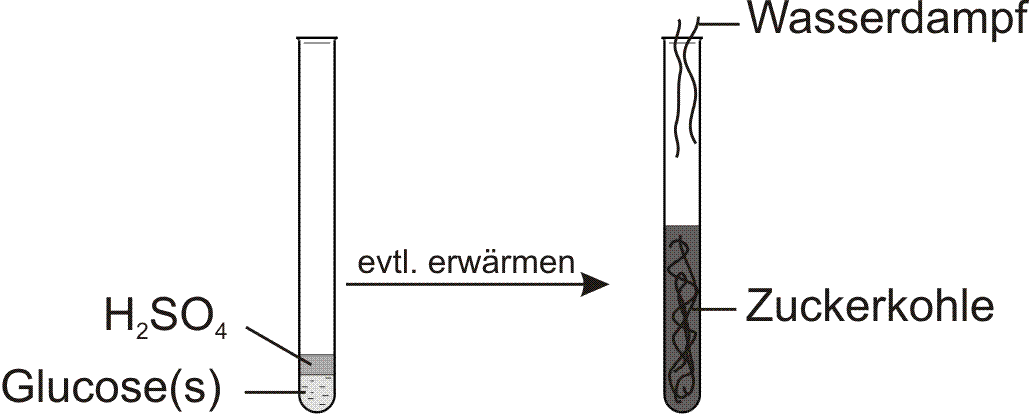
Folgerung: Glucose enthält Kohlenstoff.
Mitteilung: Glucose enthält neben C noch H und O.
c) quantitative Elementaranalyse
Die quantitative Elementaranalyse nach Liebig ergibt:
3,6 g Glucose liefert bei der Verbrennung:- 5,28 g CO2
- 2,16 g H2O
Glucose besitzt folgende Summenformel: CnH2nOn
Von dieser allgemeinen Formel [C(H2O)]n leitet sich die Bezeichnung Kohlenhydrate ab.
Hinweis: Im Heft folgen jetzt die Arbeitsanleitung zur Strukturaufklärung (mit den diversen Experimenten). Hier folgt jedoch gleich das Ergebnis. Die Reaktionsgleichungen von Fehling und Tollens-Reagenz finden sich dann auf anderen Seiten.Ergebnis:
Glucose ist ein Polyhydroxyaldehyd, genauer Pentahydroxyhexanal, ein Aldehydzucker oder Aldose.
Aldose = Monosaccharide, mit terminaler Carbonylgruppe (Aldehyd)
Ketosen = Monosaccharide, mit nicht endständiger Carbonylgruppe (Keton).
Fischerprojektion:
Es gelten folgende Regeln:
- Die C-C-Kette wird senkrecht geschrieben.
- Die am höchsten oxidierte Gruppe steht oben.
- Die C-C-Bindungen sind bei jedem C-Atom nach hinten abgewinkelt;
- dann zeigen die waagrechten Bindungen nach vorne;
- Bei der offenen Glucoseform gibt es vier asymmetrische C-Atome ==> 24-Isomere;
- Die Bezeichnung erfolgt nach dem untersten C-Atom (hier C5-Atom).
- Da die OH-Gruppe rechts steht ==> D-Konfiguration.
- ==> D-(+)-Glucose
(L-Glucose erhält man nur synthetisch)
Bildung von Glucose:
Bei Pflanzen (Fotosynthese) und Tieren (durch Abbau von anderen Molekülen).
Fotosynthese:
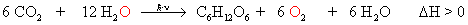
60 Mrd t Kohlenstoff werden dabei im Jahr gebunden.
Abbau von Glucose:
Bei der Zellatmung (Pflanzen, Pilze, Tiere)
- Aggregatzustand: fest; Schmelzpunkt um 146°C; weiteres Erhitzen führt zur Zersetzung.
-
04.1.5 Fructose und Keto-Enol-Tautomerie
4.1.5 Fructose = Fruchtzucker
Vorkommen: in Früchten, Nektar, Honig; vor allem industriell hergestellte Fructose
Eigenschaften: kristallisiert schlecht aus wässriger Lösung → sirupartige Flüssigkeit.
Summenformel: C6H12O6
Fructose ist somit ein Strukturisomer der Glucose.
a) Seliwanow-Probe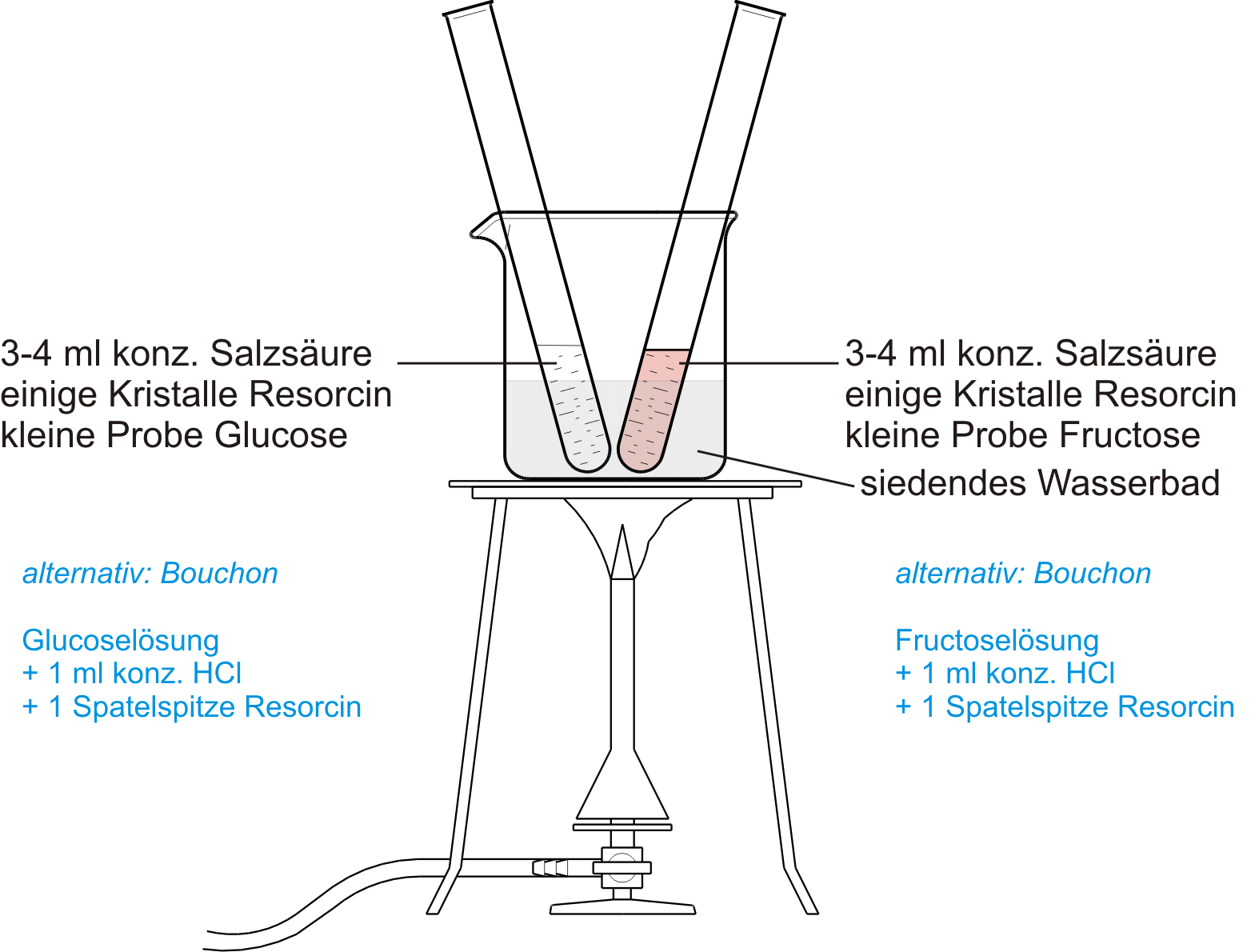
Nachweis, ob es sich bei Kohlenhydraten um Ketosen oder Aldosen handelt.
Ketose --> roter Farbstoff
Aldose --> keine/langsame Reaktion --> farblos
Info: Die Seliwanow-Reaktion ist ein Nachweis für Ketohexosen in der Furanose-Ringform. Da sie im sauren Milieu abläuft, kommt es nicht zur Keto-En(di)ol-Tautomerie. Mit Glucose fällt die Probe deshalb negativ aus.
Strukturformeln: Offenkettige und Ringbildung durch die Halbacetalbildung: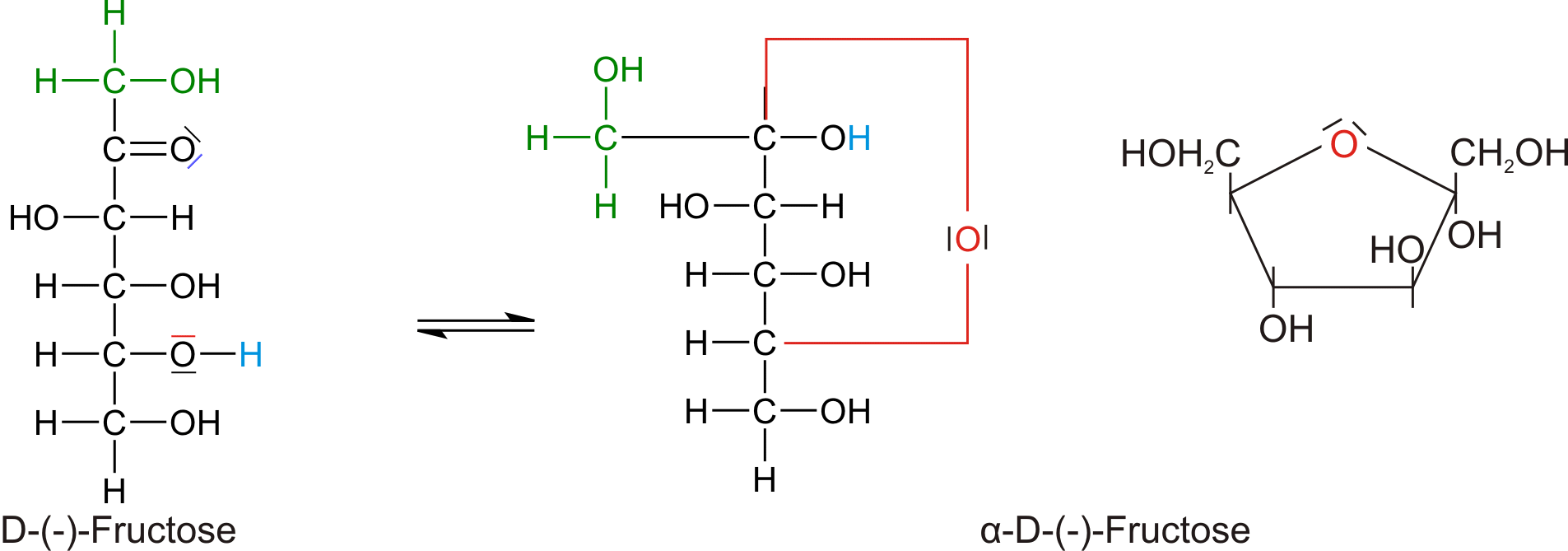
Fructose bildet wie Glucose Anomere. Neben der Kettenform des Moleküls enthält das Gleichgewicht zwei anomere Pyranosen ( β-D-Fructose und α-D-Fructose; Halbacetalbildung mit dem C5-Atom) und zwei anomere Furanosen ( β-D-Fructose und α-D-Fructose; Halbacetalbildung mit dem C6-Atom).
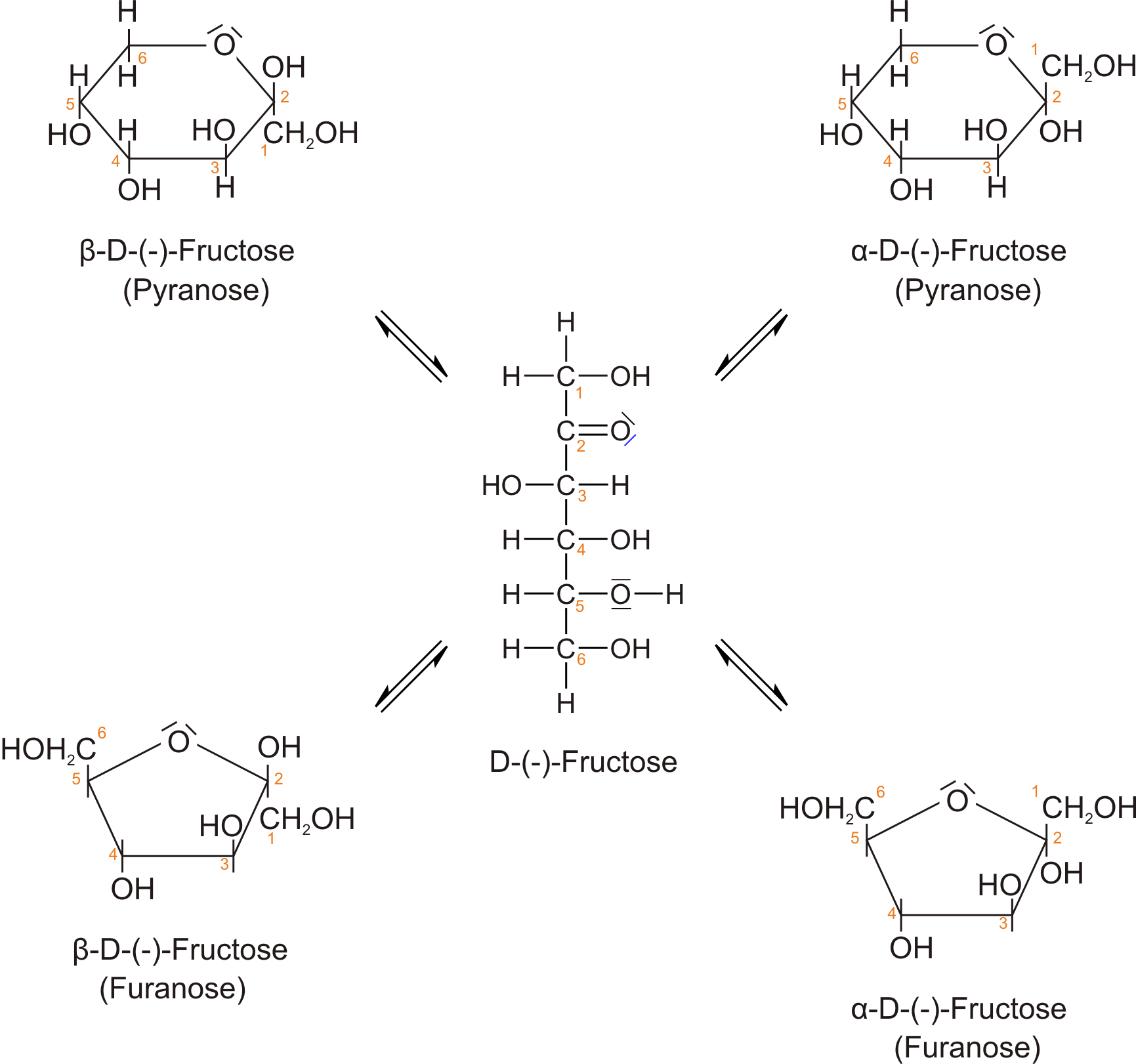
Keto-Enol -Tautomerie
Versuche mit Fructose:- Fehling → positiv
- Tollens → positiv
- GOD (Glucose-Nachweis) + Lauge → positiv
Funktioniert nicht mit einer Ketogruppe, da diese nicht weiter oxidiert werden kann. Grund, warum die Nachweise trotzdem positiv verlaufen: Innermolekulare Umlagerung unter Protonenwanderung und Elektronenverschiebung.
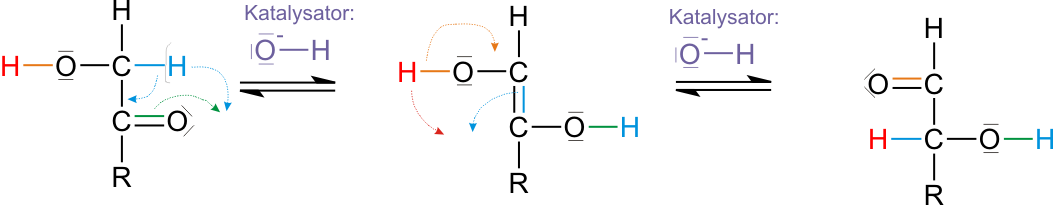
Genauer:
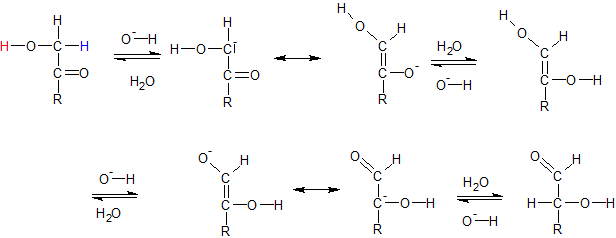
Glucose und Fructose stehen im Gleichgewicht (Glucose überwiegt); bei der Oxidation von Glucose wird Glucose aus dem GG entfernt → Fructose wird aufgebraucht.
-
04.2 Disaccharide
4.2 Disaccharide
4.2.1 Maltose (Malzzucker)
Vorkommen: Entsteht durch unvollständige Hydrolyse von Stärke .
Stärke -----(Enzym: Amylase)-----> MaltoseVerwendung: Gerstenmalz (Bier brauen)
Eigenschaften:
- Fehling positiv
- zeigt Mutarotation
- besteht aus 2 α-D-Glucoseeinheiten, α-1→4 glycosidisch verknüpft.
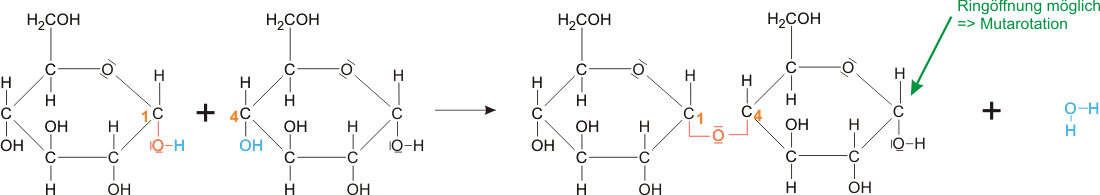
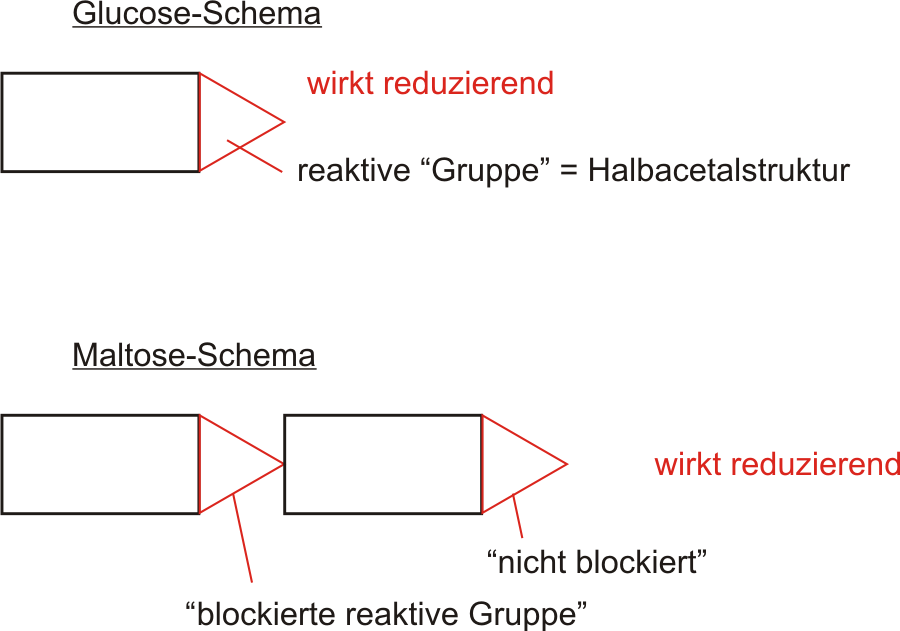
4.2.2 CellobioseVorkommen: Verdauungsprodukt von Pflanzenfressern aus Zellulose
Eigenschaften:
- Fehling positiv
- zeigt Mutarotation
- besteht aus 2 β-D-Glucoseeinheiten, β 1 → 4 glycosidisch verknüpft.

4.2.3 Lactose (Milchzucker)
Vorkommen: Muttermilch von Säugetiere (1,5 – 8 %)
Eigenschaften:- Fehling positiv
- zeigt Mutarotation
Hydrolyse ergibt β-D-Glucose und β-D-Galactose, β-1 → 4 glycosidisch verknüpft.
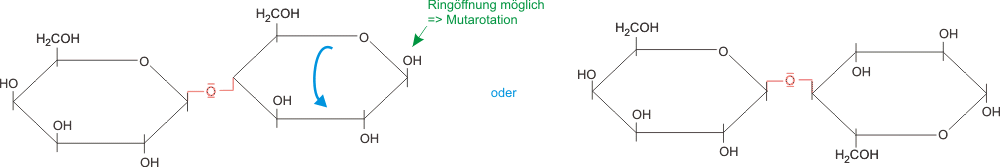
-
04.2.4 Saccharose
4.2.4 Saccharose (Rohr- oder Rübenzucker)
Vorkommen: Haushaltszucker, Kristallzucker, Zuckerrüben (18-20%), Zuckerrohr (16-22%)
Summenformel: C12H22O11 → Dissaccharide (2 Moleküle Monosaccharid minus 1 Molekül Wasser)
Physikalische Eigenschaften:
- hoher Schmelzpunkt (ca. 180°C)
- harte Kristalle
Folgerung:
- Molekülgitter mit vielen H-Brückenbindungen
- sehr leicht löslich in Wasser
- eine Rohrzuckerlösung ist zähflüssig → viele Wasserstoffbrücken
Chemische Eigenschaften:
- Fehling negativ
- zeigt keine Mutarotation
Schülerexperiment: Nach einer Hydrolyse mit verdünnter Salzsäure:
- Fehling positiv
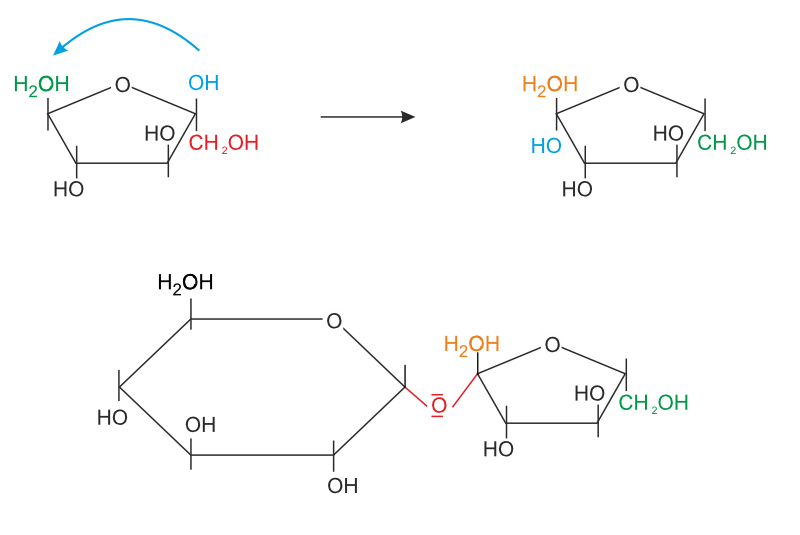
- Saccharose besteht aus α-D-Glucose und β-D-Fructose
- Beide Monosaccharide sind α-1→2-glycosidisch verknüpft
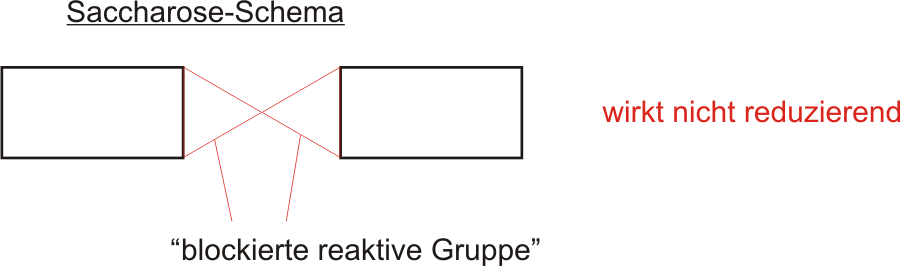
Spaltung der Saccharose mit verdünnter Salzsäure = saure Hydrolyse
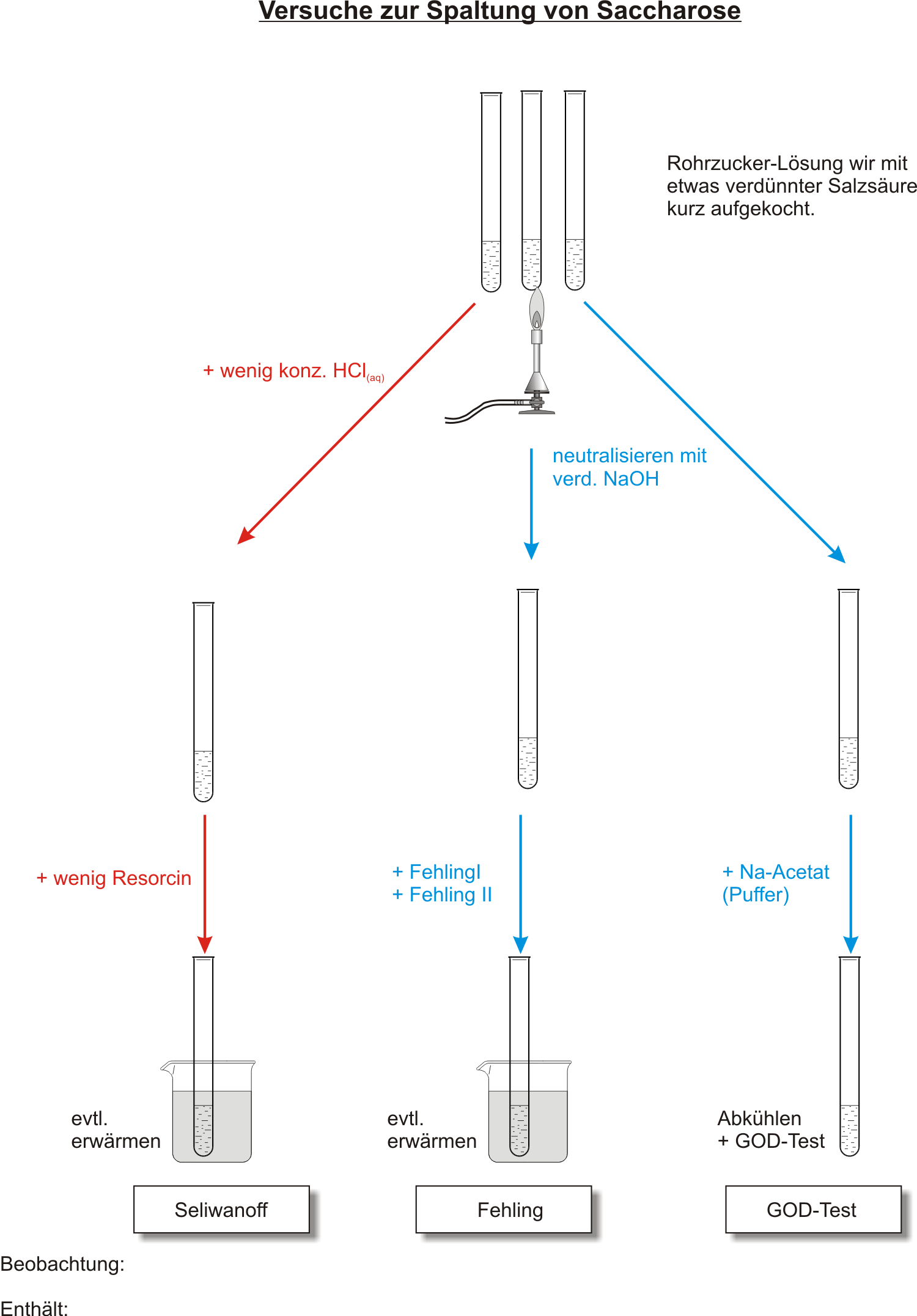
färbt sich rosa roter Niederschlag positiv
enthält Fructose Aldehydgruppe Glucose

Unter Hydrolyse versteht man einen Vorgang, bei dem Atombindungen unter Aufnahme von Wasser gespalten werden (Bsp. Esterspaltungen).
Wichtig: die leichte Hydrolisierbarkeit spricht für eine Verknüpfung über Sauerstoff.
4.2.5 Invertzucker
Saccharose dreht die Ebene des polarisierten Lichts nach rechts. Während der Hydrolyse (durch verdünnte Salzsäure oder Ferment/Enzym Invertase) nimmt die Drehung fortwährend ab und geht in eine Linksdrehung über:
Saccharose + Wasser → D-Glucose + D-Fructose
+66° + 0° + 54,7 - 92,4
Zahlenwerte αsp in ml/(g • dm)
Man bezeichnet daher diese Spaltung als Inversion des Rohrzuckers und das entstehende Gemisch als Invertzucker.
Inversion: Vorzeichenwechsel der optischen Aktivität im Verlauf einer Reaktion optisch aktiver Verbindungen. -
04.3 Polysaccharide-amylose
5.4.3 Polysaccharide
- Wichtigsten Beispiele: Stärke, Glykogen (tier. Stärke), Cellulose
- Funktion: Speicher- und Gerüstsubstanz
- Monomere der genannten Beispiele: Glucose; unterschiedl. Verknüpfung
4.3.1 Stärke
a) Vorkommen:
- Pflanzen (Speicherstoff, osmotisch nicht wirksam)
- Nahrungsmittel (Brot, Teigwaren, Kartoffel, usw.),
b) Aufbau eines Stärkemoleküls:
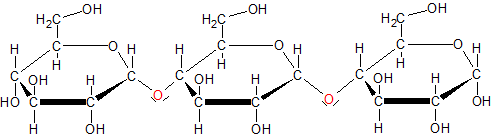
c) Bau: α-D-Glucose – StärkekornAmyolse Amylopektin Anteil: (10-30%) (70-90%) Bau: linearen Ketten (helikaler
(Schrauben-)Struktur)
stark verzweigten Strukturen Verknüpfung α-1,4-glykosidisch α-1,4-glykosidischen
α-1,6-glykosidischenLöslichkeit in heißem Wasser kolloidal löslich unlöslich Mit I2 bildet es __ Lösung blaue violette Im Stärkekorn Hülle Innen
d) Nachweis: Iodstärke-Reaktion
Versuch: Zu einer Stärkelösung gibt man ein paar Tropfen einer Lösung von Iod in Kaliumiodid (Iod-Kaliumiodid-Lösung, Lugolsche Lösung) Elementares Iod ist in Wasser kaum löslich. Liegen jedoch schon gelöste Iodid-Ionen vor, löst sich das Iod unter Bildung von Polyiodidionen:2 I2 + I- → I3- + I2 → I5-
Beobachtung: Lösung wird tiefblau
Beim Erhitzen wird die Lösung hell, beim Abkühlen wieder tiefblau
Erklärung: Die Stärkemoleküle sind spiralig angeordnet, in den entstehenden Hohlraum lagern sich Jodmoleküle ein die dort durch van-der-Waals-Kräfte gebunden werden. Eine blaue Iod-Stärke-Einlagerungsverbindung bildet sich. Das gelbe Licht wird absorbiert, die Lösung erscheint blau. Beim Erhitzen nimmt die Beweglichkeit der I2-Moleküle zu, so dass beim Erhitzen eine Entfärbung eintritt.Eigenschaften von Stärke (Amylose)
- in kaltem Wasser: unlöslich
- heißem Wasser: löslich
- schmeckt nicht süß
- kolloide Lösung (Kolloide: Moleküle oder Aggregate, die sich aus etw. 103 bis 109 Atomen zusammensetzt und in einem Dispersionsmittel verteilt sind).
Versuch:
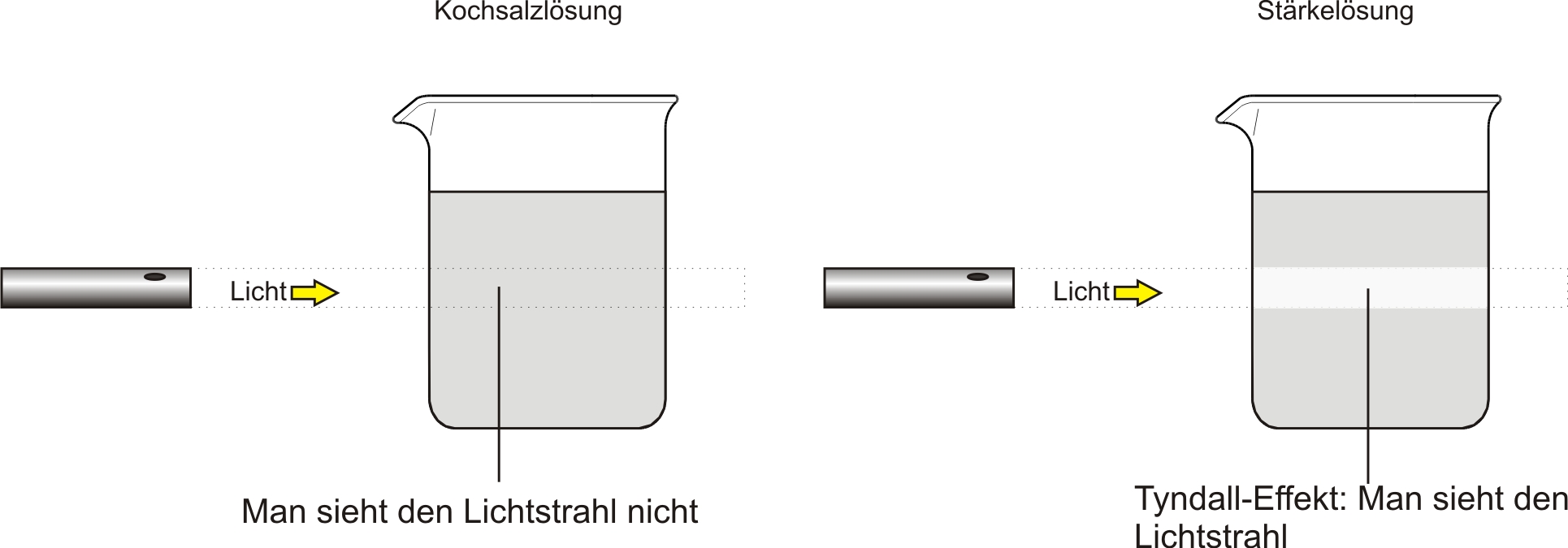
Beobachtung:
Im Gegensatz zu NaCl-Lösung ist der Verlauf des Lichtes in der Stärkelösung sichtbar (= Tyndall-Effekt).
Erklärung:
Gebündeltes Licht wird beim Durchgang durch kolloid- oder molekulardisperse Systeme gestreut (d.H. jedes Teilchen streut einen Teil des auftreffenden Lichtes in alle Richtungen des Raums. Dieser von Tyndall 1868 erstmals untersuchte Effekt tritt immer dann auf, wenn Teilchen vorliegen, deren Größe etwa der Wellenlänge des Lichtes entsprechen. Solche Teilchen haben einen Durchmesser von 1 bis 1000 nm.van-der-Waals-Kräfte/strong
-
1 Alkane
Was du auf dieser Seite findest
Das Kapitel Alkane ist das erste Kapitel der Organischen Chemie in Klasse 10 (Baden-Württemberg). Du lernst die einfachsten Kohlenwasserstoffe kennen: von Methan über Butan bis zur homologen Reihe, Nomenklatur, Eigenschaften und schließlich die radikalische Substitution als ersten organischen Reaktionsmechanismus.
Grundlagen aus der 9. Klasse
Atombindung, Lewis-Formeln und das Konzept der Elektronenpaarbindung hast du in der 9. Klasse kennengelernt: → Atombindung (Kl. 9) · → Lewis-Formeln (Kl. 9)
Unterseiten im Überblick
1.1
Methan
Lewis-Formel · Kugelstabmodell · Verbrennung
1.2 · bei ausreichend Zeit
Ethan
Noch kein eigener Artikel online
1.3 · bei ausreichend Zeit
Propan
Noch kein eigener Artikel online
1.4
Butan
Konstitutionsisomerie · Strukturformeln · Verbrennung
1.5
Homologe Reihe der Alkane
CₙH₂ₙ₊₂ · Strukturformeln C₁–C₁₇ · Siedepunkte
1.6
Genfer Nomenklatur
Hauptkette · Substituenten · Lokanten · → Übungen
1.7
Struktur und Eigenschaften
Einfachbindung · Van-der-Waals-Kräfte · unpolar · hydrophob
1.8
Angriffsfreudige Teilchen
Radikale · Elektrophile · Nucleophile
1.9
Reaktion mit Halogenen
Radikalische Substitution · Start / Kette / Abbruch · Halogenalkane
Vollständige Inhaltsübersicht
- 1.1 Methan – Lewis-Formel, Kugelstabmodell, qualitative Elementaranalyse, Verbrennung
- 1.2 Ethan (bei ausreichend Zeit – noch kein Artikel)
- 1.3 Propan (bei ausreichend Zeit – noch kein Artikel)
- 1.4 Butan – Strukturformeln, Konstitutionsisomerie (n-Butan / Isobutan), Verbrennung
- 1.5 Homologe Reihe der Alkane – allgemeine Formel CₙH₂ₙ₊₂, Strukturformeln C₁–C₁₇, Siedepunkttrend
- 1.6 Genfer Nomenklatur der Alkane – Hauptkette, Substituenten, Lokanten | → Übungen zur Nomenklatur
- 1.7 Struktur und Eigenschaften der Alkane – Einfachbindung, Van-der-Waals-Kräfte, unpolar, Siedepunkte
- 1.8 Angriffsfreudige Teilchen – Radikale, Elektrophile, Nucleophile
- 1.9 Reaktion von Alkanen mit Halogenen – Radikalische Substitution: Start-, Ketten- und Abbruchreaktion, Halogenalkane
Auf einen Blick – Alkane
Homologe Reihe
Alkane haben die allgemeine Formel CₙH₂ₙ₊₂. Jedes folgende Glied der homologen Reihe enthält eine CH₂-Gruppe mehr. Siedepunkt und Schmelzpunkt steigen mit der Kettenlänge.
Eigenschaften
Alkane sind unpolar und reagieren wegen der starken Einfachbindung normalerweise nicht. Zwischen den Molekülen wirken nur Van-der-Waals-Kräfte – daher niedrige Siedepunkte und schlechte Wasserlöslichkeit.
Radikalische Substitution
Alkane reagieren mit Halogenen durch radikalische Substitution (UV-Licht): Start (homolytische Spaltung) → Kettenreaktion (Radikal greift CH-Bindung an) → Abbruch (zwei Radikale verbinden sich).
Genfer Nomenklatur
Regeln: 1. Längste Kette bestimmen. 2. Substituenten von der nächstgelegenen Seite nummerieren. 3. Substituenten alphabetisch benennen. Beispiel: 3-Ethyl-2,2-dimethylhexan.
Häufige Fragen – Alkane
Was ist ein Alkan und was bedeutet „gesättigt"?
Alkane sind Kohlenwasserstoffe, die ausschließlich Einfachbindungen zwischen Kohlenstoffatomen besitzen. Die allgemeine Formel lautet CₙH₂ₙ₊₂. „Gesättigt" bedeutet, dass jedes C-Atom die maximale Anzahl an H-Atomen trägt – es gibt keine Doppel- oder Dreifachbindungen, an die weitere Atome addiert werden könnten. Beispiele: Methan CH₄, Ethan C₂H₆, Propan C₃H₈.
Warum steigt der Siedepunkt in der homologen Reihe der Alkane?
Mit zunehmender Kettenlänge steigt die Moleküloberfläche, über die Van-der-Waals-Kräfte wirken. Mehr Kontaktfläche bedeutet stärkere intermolekulare Anziehung – daher muss mehr Energie aufgewendet werden, um die Moleküle voneinander zu trennen, was sich in einem höheren Siedepunkt zeigt. → Homologe Reihe
Was sind die drei Schritte der radikalischen Substitution?
1. Startreaktion: UV-Licht spaltet Cl₂ homolytisch in zwei Chlorradikale (Cl•).
2. Kettenreaktion: Cl• greift CH₄ an → HCl + CH₃•; CH₃• reagiert mit Cl₂ → CH₃Cl + Cl• (Kette läuft weiter).
3. Abbruchreaktion: Zwei beliebige Radikale verbinden sich zu einem stabilen Molekül – die Kette bricht ab.
Das Verhältnis der Produkte (Mono-, Di-, Trichlormethan …) hängt von den Bedingungen ab. → Radikalische SubstitutionWas ist der Unterschied zwischen Elektrophilen, Nucleophilen und Radikalen?
Elektrophile sind elektronenarme Teilchen, die Elektronenpaare suchen (Lewis-Säuren).
Nucleophile sind elektronenreiche Teilchen mit freien Elektronenpaaren (Lewis-Basen).
Radikale sind Teilchen mit einem ungepaarten Elektron; sie entstehen durch homolytische Bindungsspaltung (z. B. durch UV-Licht) und sind besonders reaktiv. → Angriffsfreudige TeilchenWie benennt man verzweigte Alkane nach der Genfer Nomenklatur?
Schrittweise Vorgehensweise:
1. Längste durchgehende Kohlenstoffkette = Hauptkette → gibt den Stammnamen.
2. Nummerierung: von der Seite beginnen, die den ersten Substituenten mit der kleinsten Zahl ergibt.
3. Substituenten: Alkylgruppen mit Lokant und Namen (z. B. 2-Methyl-). Mehrere gleiche: di-, tri-, tetra-. Alphabetische Reihenfolge bei verschiedenen.
Beispiel: 3-Ethyl-2,2-dimethylhexan. → Genfer NomenklaturLernkarten – Alkane
Klicke auf eine Karte, um die Antwort zu sehen.
1Was ist die allgemeine Summenformel der Alkane? Gib drei Beispiele an.
Allg. Formel: CₙH₂ₙ₊₂
Methan: CH₄ (n = 1)
Ethan: C₂H₆ (n = 2)
Propan: C₃H₈ (n = 3)
→ Gesättigte Kohlenwasserstoffe2Was sind Van-der-Waals-Kräfte und welche Auswirkung haben sie auf Alkane?
Schwache Dispersionskräfte zwischen unpolaren Molekülen.
→ Alkane: niedrige Siedepunkte
→ Schlecht löslich in Wasser
→ Siedepunkt steigt mit Kettenlänge (mehr Kontaktfläche)3Was versteht man unter Konstitutionsisomerie? Erkläre am Beispiel Butan.
Gleiche Summenformel, verschiedene Verknüpfung der Atome.
C₄H₁₀: n-Butan (gerade Kette)
und 2-Methylpropan / Isobutan (verzweigt)
→ unterschiedliche Siedepunkte!4Was entsteht bei der vollständigen Verbrennung von Alkanen?
Vollständige Verbrennung (Oxidation):
Alkan + O₂ → CO₂ + H₂O
Beispiel Methan:
CH₄ + 2 O₂ → CO₂ + 2 H₂O (ΔH < 0)
→ Exotherme Reaktion5Benenne: CH₃–CH(CH₃)–CH₂–CH₂–CH₃ nach Genfer Nomenklatur.
Längste Kette: 5 C → Pentan
Methylgruppe an C2 → 2-Methylpentan
Kontrolle: Nummerierung von links ergibt Lokant 2,
von rechts Lokant 4 → kleinste Zahl = 2 ✓Weiter im Kapitel Organische Chemie
← Klasse 10 – Übersicht → 2 Alkene
🔁 Grundlagen (Kl. 9): Atombindung · Lewis-Formeln
📚 Vertiefung Kursstufe: Cycloalkane · Aromaten -
4.3.2 Cellulose
4.3.2 Cellulose
Vorkommen: Cellulose ist das in der Natur am häufigsten auftretende Kohlenhydrat. Sie ist die Gerüstsubstanz in der Pflanzenwelt.
z.B.: Baumwolle, Flachs, Hanf (fast 100%); Stroh (30%); Holz (40-50% Cellulose).
Eigenschaften: Cellulose ist eine weiße, in Wasser und in den meisten organischen Lösungsmitteln unlösliche Substanz.
Hydrolyse der Cellulose:
a) Versuch: Filterpapierschnitzel werden mit konz. Salzsäure übergossen. Diese Mischung gibt man in 50 mL Wasser und erhitzt etwa 10 Minuten.
Anschließend wird die Fehlingsche Probe durchgeführt.
Beobachtung: roter Niederschlag
b) Versuch: GOD-Test mit der hydrolisierten Cellulose.
Beobachtung: Grünfärbung des Teststreifens.Folgerung: Cellulose enthält als Baustein D-Glucose.
c) Versuch: Dünnschichtchromatographie
Ein Chromatogramm gibt genauen Aufschluss über die Bausteine: Glucose. Bei vorsichtiger Hydrolyse ist außer β-D-Glucose auch noch Cellobiose nachweisbar (Cellobiose ist ein Disaccharid aus 2 ∙ β-D-Glucosemolekülen).
Aufbau eines Cellulosemoleküls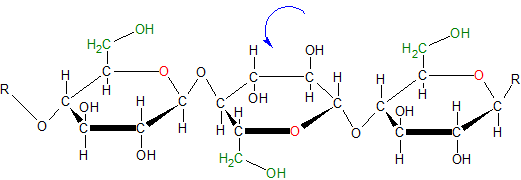
CellobioseAusschließlich β-(1,4)-glycosidische Bindung
Bei der Cellulose handelt es sich um fadenförmig gestreckes Makromoleküle. Diese Makromoleküle lagern sich zu Elementarfibrillen zusammen (H-Brücken).
4.3.3 Unterschied: Cellulose – Stärkea) Räumlich unterschiedliche Verknüpfung der Glucoseringe in den Makromolekülen
Cellulose: (-Glu-Glu-Glu-Glu- verknüpft β 1→4)
Stärke (z.B. Amylose) (-Glu-Glu-Glu-Glu- verknüpft α 1→4 )
b) Unterschiedliche Anordnung der Makromoleküle
Cellulose: langgestreckte, unverzweigte Kettenmoleküle
Stärke: verzweigte Kettenmoleküle, die spiralig aufgerollt sind.
c) Unterschiedliche Molekülmasse
Cellulose: bis 1,8 Millionen u
Stärke: bis 50 000 u4.3.4 Verwendung der Cellulose
Nahrungsmittel: Der Mensch kann β-1,4-Bindungen der Cellulose nicht abbauen ( → Ballaststoffe).
Im Dickdarm schaffen das anaerobe Bakterien→ Umwandlung in Fettsäuren → Resorption.
Kühe: Pansen: Mikroorganismen → Celluloseverdauung
Pferde u.a. Dickdarm
Einige Pilze und Silberfischchen (eine der wenigen Tiere mit eigenen Cellulasen).
Wichtigste Textilfasern: Baumwolle.
Aus Hanf, Flachs, Jute werden Leinen, Säcke, Segeltuch, Matten usw. hergestellt.
Papier
4.3.4 Derivate der Cellulose
a) Cellulose – Kunstseiden
b) Schießbaumwolle (Christian Friedrich Schönbein, Metzinger Chemiker, geb. 1799).
Schießbaumwolle ist Cellulosenitrat (fälschlicherweise als Nitrocellulose bezeichnet).
Herstellung der Schießbaumwolle: 20 mL konz. H2SO4 + 10 ml rauchende HNO3 zur Kühlung kaltes Wasserbad; 2 g Watte dazugeben und mit Galsstab umrühren. Nach 10 Minuten wird die veresterte Watte nur gut mit Wasser ausgewaschen und anschließend im Exsikkator getrocknet.
Schießbaumwolle ist Grundlage für raucharmes Schießpulver, welches das Schwarzpulver ersetzte. z.T. mit Nitroglycerin versetzt dient die Schießbaumwolle als Sprengmittel mit einem Initialzünder.erbrennung
Normale Watte, die fast ausschließlich aus Cellulose besteht, ist nur schwer brennbar. Schießbaumwolle verbrennt explosionsartig mit einer Stichflamme. Bei der Verbrennung der Schießbaumwolle werden große Mengen stabiler Gase frei, die durch ihre Ausdehnung zu einer Druckwelle führen, die typischerweise eine Explosion begleitet. Die entstandenen Gase sind Stickstoff (N2), Stickoxide (NOx) , Kohlenstoffmonoxid (CO), sowie Kohlendioxid (CO2).
Reaktionsgleichung der Herstellung von Nitriersäure
Summenformeln:
2 H2SO4 + HNO3 → NO2+ + H3O1+ + HSO41-
Herstellung von Schießbaumwolle: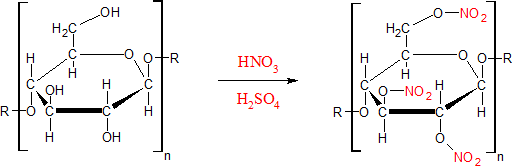
-
5 Alkohole - Alkanole
Was du in diesem Kapitel lernst
Alkohole (Alkanole) sind Kohlenwasserstoffe mit mindestens einer OH-Gruppe (Hydroxygruppe). Am Beispiel des Ethanols lernst du Eigenschaften, Formelermittlung und typische Reaktionen kennen. Dazu kommen die homologe Reihe, der induktive Effekt und die wichtigen mehrwertigen Alkohole wie Glycerin und Glykol.
Grundlagen aus der 10. Klasse
Alkohole enthalten eine C-Kette wie die Alkane, Alkene und Alkine. Wiederhole bei Bedarf: → 3. Alkine – C≡C-Dreifachbindung, Additionsreaktion · → 2. Alkene – Funktionelle Gruppen, Isomerie
Kapitelübersicht – 5. Alkohole (Alkanole)
Klicke auf eine Kachel, um direkt zum Unterkapitel zu springen.
5.1 Ethanol
C₂H₅OH5.1
Ethanol
Herstellung · Physikalische & chemische Eigenschaften · Alkoholismus
→ 5.1.1 Herstellung · 5.1.2 Eigenschaften · 5.1.6 Alkoholismus5.1.3
Formelermittlung
Verbrennungsanalyse · Summen- und Strukturformel von Ethanol · Molare Masse
5.1.4
Ethanol + Alkalimetall
Versuch: Natrium in Ethanol · Reaktionsgleichung · Vergleich mit Wasser
5.1.5
Induktiver Effekt
+I-Effekt und −I-Effekt · Elektronenverschiebung · Polarität der O–H-Bindung
5.2 Homologe Reihe & Systematik
5.2
Homologe Reihe der Alkohole
Hydroxy- & Methylgruppe · wichtige Alkohole · Löslichkeit · H-Brückenbindung
→ 5.2.1 Gruppen · 5.2.2 Wichtige Alkohole · 5.2.3 Löslichkeit5.2.4 / 5.2.5
Primär · Sekundär · Tertiär
Unterscheidung nach C-Nachbarn · allgemeine Formel der Alkanole CnH2n+1OH
5.2.6
Mehrwertige Alkohole
Glykol (Ethandiol) · Glycerin (Propantriol) · Sorbit · Vorkommen & Verwendung
5.3 Reaktionen · 5.4 Ether
5.3
Chemische Reaktionen
Bindungsverhältnisse · Redox mit Na · Verbrennung · Reaktion mit HBr · Dehydratisierung
→ 5.3.1–5.3.5 am Beispiel von Ethanol5.4
Ether
Herstellung · Physikalische Eigenschaften · Chemische Eigenschaften · Verwendung
⚠️ Seite noch nicht online
Auf einen Blick – die wichtigsten Aussagen
Funktionelle Gruppe
Alkohole besitzen eine oder mehrere OH-Gruppen (Hydroxygruppen). Die Formel einwertiger Alkanole lautet CnH2n+1OH. Die OH-Gruppe bestimmt die typischen Eigenschaften: Löslichkeit in Wasser, H-Brückenbindungen, Reaktivität.
Induktiver Effekt
Der negative induktive Effekt (−I) des Sauerstoffs zieht Elektronen aus der C–O-Bindung, wodurch das H in der OH-Gruppe leicht abspaltbar (schwach sauer) wird. Alkylgruppen zeigen den +I-Effekt.
prim / sek / tert
Primäre Alkohole: OH am C-Atom mit 1 C-Nachbarn. Sekundäre: 2 C-Nachbarn. Tertiäre: 3 C-Nachbarn. Die Klassifizierung bestimmt das Reaktionsverhalten (z. B. Oxidierbarkeit).
Reaktionen
Ethanol reagiert als schwache Säure mit Natrium (→ Natriumethanolat + H2), verbrennt zu CO2 + H2O und reagiert mit HBr durch nucleophile Substitution zu Bromoethan.
Häufige Fragen – Alkohole (Alkanole)
Was sind Alkohole, und was ist ihre funktionelle Gruppe?
Alkohole (Alkanole) sind organische Verbindungen mit mindestens einer Hydroxygruppe (–OH). Das einfachste Mitglied ist Methanol (CH3OH), das wichtigste im Alltag ist Ethanol (C2H5OH). Die allgemeine Formel einwertiger Alkanole lautet CnH2n+1OH. Die OH-Gruppe verleiht Alkoholen ihre charakteristischen Eigenschaften: gute Wasserlöslichkeit (durch H-Brücken), höhere Siedepunkte als vergleichbare Alkane, und schwach saures Verhalten gegenüber Alkalimetallen.
Was unterscheidet primäre, sekundäre und tertiäre Alkohole?
Die Klassifizierung richtet sich danach, an wie vielen C-Atomen das OH-tragende Kohlenstoffatom gebunden ist: Primärer Alkohol: das OH-C hat einen C-Nachbarn (z. B. Ethanol, 1-Propanol). Sekundärer Alkohol: das OH-C hat zwei C-Nachbarn (z. B. 2-Propanol = Isopropanol). Tertiärer Alkohol: das OH-C hat drei C-Nachbarn (z. B. 2-Methyl-2-propanol). Diese Unterscheidung ist entscheidend für die Oxidierbarkeit: primäre → Aldehyde → Carbonsäuren; sekundäre → Ketone; tertiäre können nicht oxidiert werden. → 5.2.4
Wie reagiert Ethanol mit Natrium, und was beweist das über die OH-Gruppe?
Ethanol reagiert mit Natrium ähnlich wie Wasser, jedoch langsamer: 2 C2H5OH + 2 Na → 2 C2H5ONa + H2↑. Es entsteht Natriumethanolat und Wasserstoffgas. Die Reaktion zeigt, dass die OH-Gruppe in Alkoholen schwach sauer ist: das H-Atom der OH-Gruppe wird als H⁺ abgegeben (schwächere Säure als Wasser, weil der +I-Effekt der Ethylgruppe die O–H-Bindung weniger polarisiert). → 5.1.4
Was ist der induktive Effekt, und wie wirkt er in der OH-Gruppe?
Als induktiven Effekt bezeichnet man die Verschiebung der Elektronendichte in einer Bindungskette durch einen elektronegativen oder elektropositiven Substituenten. Der Sauerstoff der OH-Gruppe ist stark elektronegativ und zieht Elektronen aus dem benachbarten C-Atom heraus → negativer induktiver Effekt (−I). Die O–H-Bindung ist stark polarisiert, das H-Atom leicht abspaltbar. Alkylgruppen geben Elektronen ab (+I-Effekt), was die Säurestärke der Alkohole gegenüber Wasser leicht herabsetzt. → 5.1.5
Was sind mehrwertige Alkohole, und wo kommen sie vor?
Mehrwertige Alkohole tragen mehr als eine OH-Gruppe. Wichtige Vertreter: Glykol (Ethan-1,2-diol, 2 OH-Gruppen) – Frostschutzmittel und Ausgangsstoff für Kunststoffe (PET). Glycerin (Propan-1,2,3-triol, 3 OH-Gruppen) – natürlicher Bestandteil von Fetten und Ölen, Zusatz in Kosmetik, Lebensmitteln und Arzneimitteln. Sorbit (Hexan-1,2,3,4,5,6-hexol) – Zuckerersatzstoff. Durch die vielen OH-Gruppen bilden mehrwertige Alkohole besonders viele H-Brücken → sehr hohe Siedepunkte, sirupartige Konsistenz. → 5.2.6
Lernkarten – Alkohole
Klicke auf eine Karte, um die Antwort zu sehen.
1Was ist die funktionelle Gruppe der Alkohole? Wie lautet die allgemeine Formel?
Funktionelle Gruppe: –OH (Hydroxygruppe)
Allgemeine Formel einwertiger Alkanole: CnH2n+1OH
Beispiele: Methanol CH3OH · Ethanol C2H5OH2Was ist ein primärer, sekundärer und tertiärer Alkohol? Nenne je ein Beispiel.
Primär: OH-C hat 1 C-Nachbarn → Ethanol
Sekundär: 2 C-Nachbarn → 2-Propanol
Tertiär: 3 C-Nachbarn → 2-Methyl-2-propanol
Tertiäre Alkohole sind nicht oxidierbar.3Was passiert, wenn Ethanol mit Natrium reagiert? Gleichung?
2 C2H5OH + 2 Na →
2 C2H5ONa + H2↑
Natriumethanolat + Wasserstoff. Langsamer als Na + H₂O (schwächere Säure).4Was ist Glycerin? Nenne Formel, Anzahl der OH-Gruppen und eine Verwendung.
Propan-1,2,3-triol
Formel: C3H5(OH)3
3 OH-Gruppen → sirupartig, hygroskopisch
Verwendung: Kosmetik, Lebensmittel (E422), Fettbaustein5Berechne: Wie viel g H2 entstehen bei der Reaktion von 46 g Ethanol mit überschüssigem Natrium?
2 C2H5OH + 2 Na → 2 C2H5ONa + H2
M(C2H5OH) = 46 g/mol → n = 1 mol
Verhältnis 2:1 → n(H2) = 0,5 mol
m(H2) = 0,5 · 2 g/mol = 1 g H2
Weiter im Fach Chemie / 10. Klasse
← 3. Alkine → 6. Carbonylverbindungen ↑ Übersicht 10. Klasse
🔭 Vertiefung in der Kursstufe: Naturstoffe – Aminosäuren, Glucose, Enzyme
-
5.1.3 Formelermittlung von Ethanol
5.1.3 Formelermittlung von Ethanol
I. Qualitative Elementaranalyse
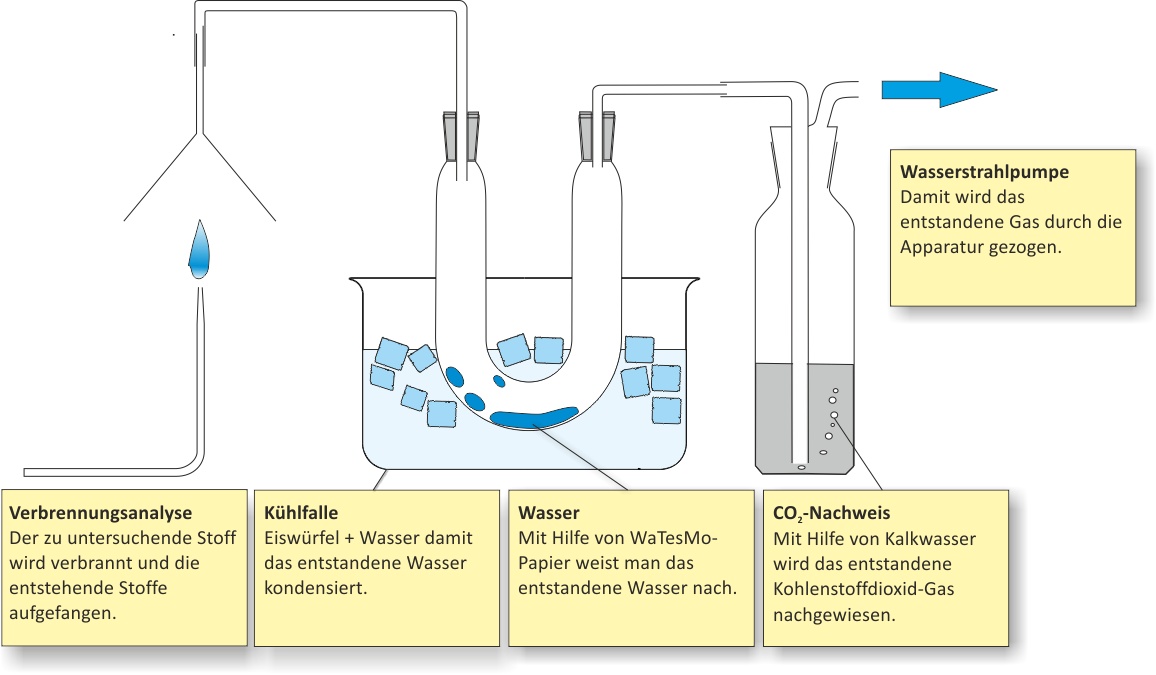
Versuch 1: Verbrennungsanalyse
- Ethanol verbrennt zu Wasser und Kohlenstoffdioxid;
- Nachweis von CO₂: Kalkwasser (weißer NS)
- Nachweis von H₂O: Watesmo-Papier wird blau
1. Ergebnis: Ethanol enthält somit zumindest C und H.
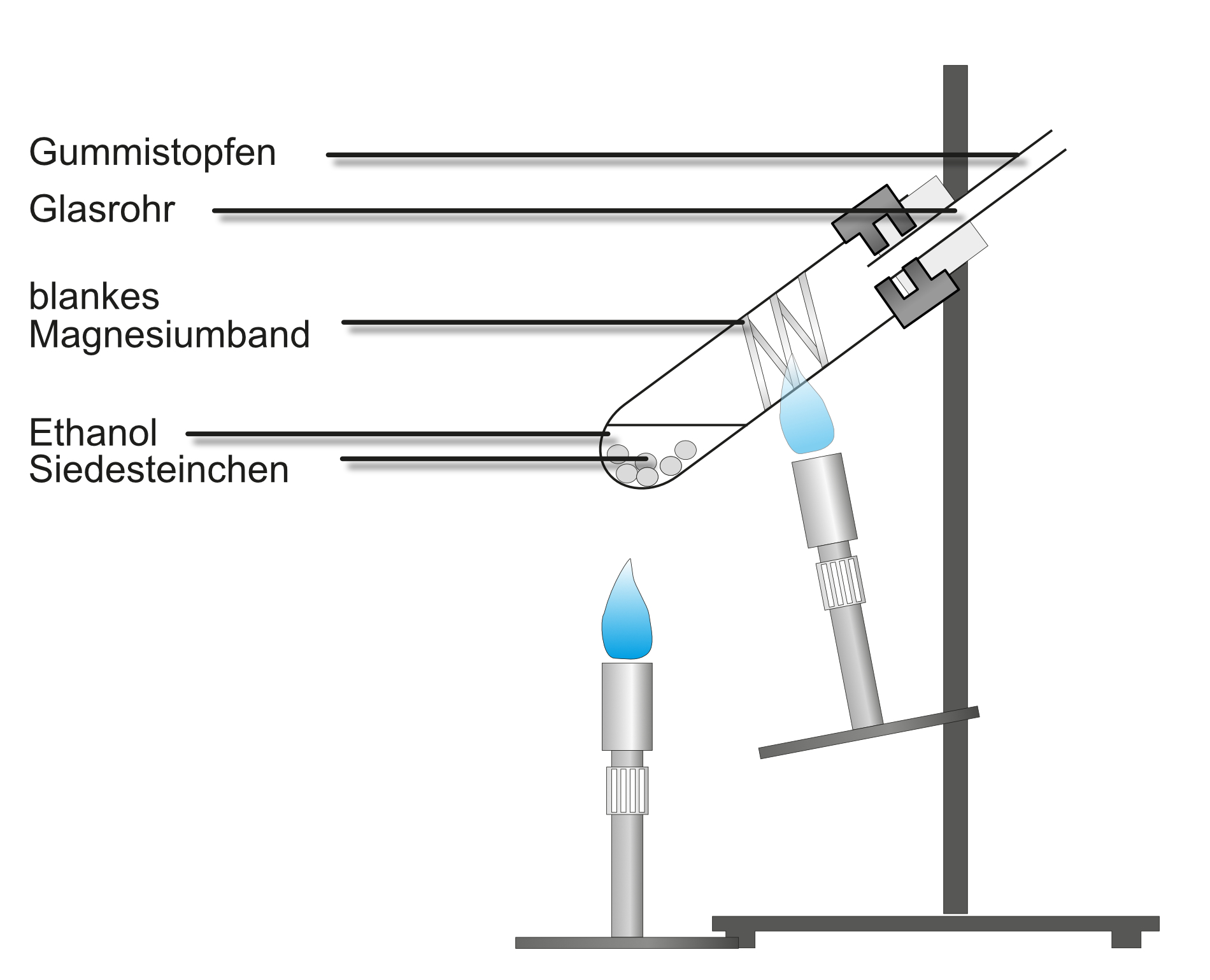
Versuch 2: Ethanol reagiert mit Magnesium - SauerstoffnachweisDurchführung:
- Aufbau siehe Abbildung
- Zunächst wird das Magnesiumband zum Glühen gebracht
- Danach verdampft man den Alkohol, der über das glühende Magnesiumband streicht.
Beobachtung:
Sobald Ethanol über das glühende Magnesiumband streicht glüht dieses heller auf und es bleibt ein kristalliner weißer Feststoff (Magnesiumoxid) übrig.
Ergebnis:
- Ethanol enthält neben Kohlenwasserstoff und Wasserstoff noch Sauerstoff.
II. Molekülmassenbestimmung (Verdampfungsmethode)
Hinweis: Dieser Versuch nur bei ausreichender Zeit durchgeführt. Nicht wundern, falls ihr das nicht im Heft stehen habt (dann kommt es auch in der Klausur nicht dran).
{slider title="Molmassenbestimmung nur bei viel Zeit" open="false" class="icon"}
Versuch: Molmassenbestimmung von Ethanol
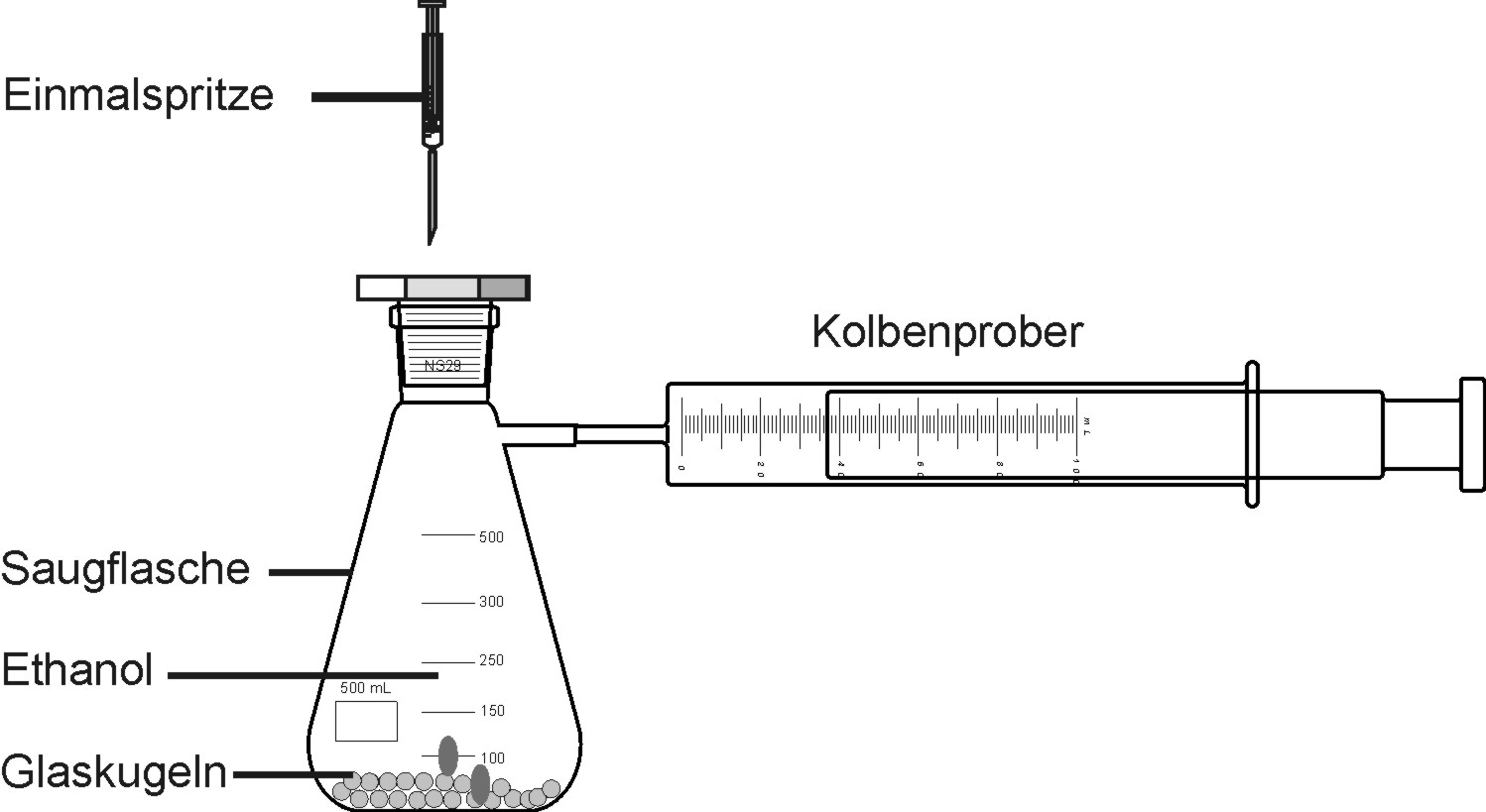
In den Erlenmeyerkolben werden 0,1 ml Ethanol eingespritzt. Auf der vergrößerten Oberfläche der Glasperlen wird das Ethanol leicht verdampft. Das entsprechende Gasvolumen kann am Kolbenprober abgelesen werden.
Auswertung:
0,1 ml Ethanol haben bei Standardbedingungen (SATP)* (25°C) ein Dampfvolumen von 43 ml.
0,1 ml Ethanol haben bei Normalbedinungen (0°C) ein Dampfvolumen von 37,8 ml.Eingesetzte Masse Ethanol: über Dichte:
ρ = Dichte
m = Masse
V = Volumen
Rechnung:
37,8 ml Ethanol (NB) haben die Masse 0,079 g: ρ = m/V = 0,079 g/37,8 ml = 0,0021 g/ml
Über das molare Gasvolumen bei Normalbedingung Vm (Gas) = 22,4 L kann man die Molmasse berechnen.
1 mol Ethanoldampf unter NB haben die Masse:
M(Ethanol) = (0,079 g * 22 400 ml)/37,8 ml = 46,8 g (Dreisatz)
{/sliders}
Literaturwert: M(Ethanol) = 46 g/mol.
_______________
* SATP-Bedingungen (Standard Ambient Temperature and Pressure)
-
5.1.3 Formelermittlung von Ethanol - Teil II
III. Quantitative Elementaranalyse
46g Ethanol ergeben bei der Verbrennung 88 g CO₂ und 54 g H₂O
- in 2 mol CO₂ sind 2 mol C (24g) enthalten
- in 3 mol H₂O sind 6 mol H (6g) enthalten
46 g Ethanol enthalten somit 2 mol C (24g) und 6 mol H (6g) und 1 mol (16g).
Atomzahlverhältnis im Ethanol: C : H : O = 2 : 6 : 1
Verhältnisformel: C₂H₆O₁
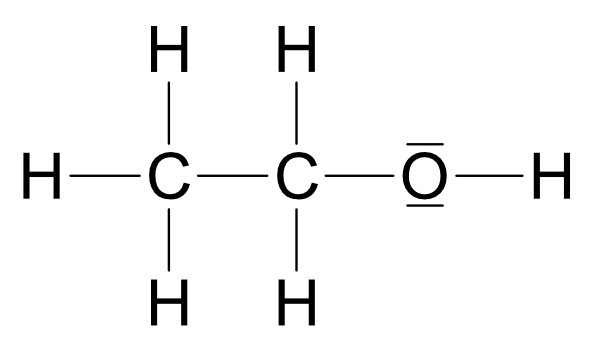
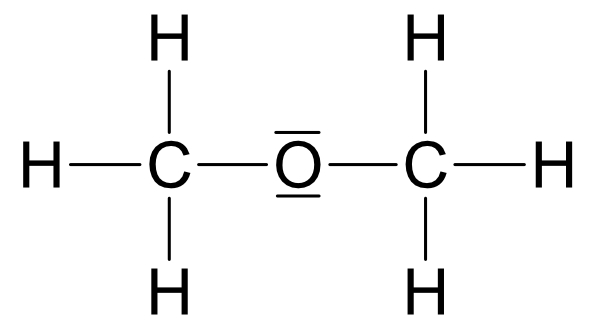
Molekülformel: C₂H₆O (Molekülmasse = 46u)IV. Ermittlung der Strukturformel von C₂H₆O
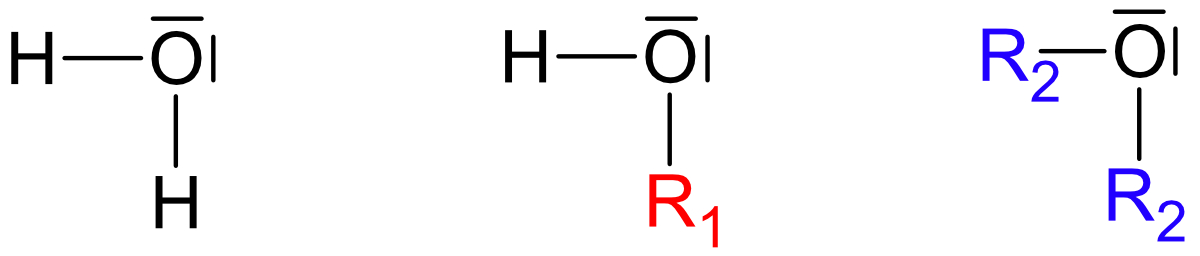
Zwei Möglichkeiten:
Wichtig: Ethanol und Dimethylether sind Derivate (Abkömmlinge) des Wassers.Beide Strukturen leiten sich vom Wasser ab, jedoch ist Struktur a wasserähnlicher.
R1 = - C₂H₅ (Ethylrest)
R2 = - CH₃ (Methylrest)
Siedepunkt: Struktur a +78°C und Struktur b -25°CUm herauszufinden, welche dieser Strukturen auf Ethanol zutrifft bitte nächste Seite anschauen.
-
5.1.9 Nachweisreaktionen
5.1.8 Weitere Aminosäuren
Vergleiche ausgegebenes Arbeitsblatt
Essenzielle (lebenswichtige) Aminosäuren
8 Aminosäuren können nicht im menschlichen Körper synthetisierst werden. Sie müssen mit der Nahrung aufgenommen werden.5.1.9 Nachweisreaktionen
a) Schwefelnachweise
Pb²⁺ (aq) + 2 Ac⁻ (aq) + H₂S (g) → PbS (s) + 2 HAc
Bleiacetatlsg. Schwefelwasserstoff Bleisulfid Essigsäure
schwarz
b) NinhydrinreaktionNinhydrin ist ein Reagens zum Nachweis von Ammoniak und primären Aminogruppen, insbesondere von Aminosäuren.
Zwei Moleküle Ninhydrin reagieren in alkalischen Milieu mit kurzen Oligopeptiden zu einem blauen Farbstoff, Ruhmanns Violett. -
5.3 Eiweiße
5.3 Eiweiße
5.3.1 Definitionen
- Eiweiße sind makromolekulare Verbindungen (über 100 Bausteine), deren Moleküle durch Peptidbindung verknüpft sind. Sie erfüllen eine biologische Funktion und sind die eigentlichen „Träger des Lebens“.
- Proteine (einfache Eiweiße); sie bestehen nur aus Aminosäurebaugruppen.
- Proteide (zusammengesetzte Eiweiße); sie enthalten zusätzlich prosthetische Gruppen (Zucker, Nukleinsäuren, Phosphorsäure, Farbstoffe, Vitamine u.a.)
5.3.2 Spaltung der Eiweiße (Hydrolyse)
- durch Erhitzen mit Säuren oder Alkalien
- durch Enzyme
5.3.3 Nachweisreaktionen
Peptide werden mit Hilfe charakteristischer Farbreaktionen nachgewiesen.
5.3.3.1 Biuret - Reaktion (Biuret - Probe)Versuch: Einige ml Eiklarlösung (oder Milch) werden mit derselben Menge verd. Natronlauge versetzt und leicht erwärmt; anschließend tropft man Kupfersulfatlsg. dazu.
Beobachtung: rot bis blauviolette Farbe
Alle Verbindungen, die 3 und mehr peptidartige Bindungen enthalten, färben sich mit Kupfersulfat in alkalischer Lösung. Die Probe ist nicht spezifisch für Eiweiß, da auch einige andere Substanzen (z.B. Biuret) eine positive Reaktion bewirken.Bei dieser Proteinbestimmungsmethode gehen Verbindungen mit mindestens zwei Peptidbindungen in wässrig alkalischer Lösung einen farbigen Komplex mit vorhandenen zweiwertigen Kupferionen ein. Daraus resultiert ein Farbumschlag nach dunkelviolett.
5.3.3.2 Xanthoprotein - Reaktion
Versuch: Zu Eiklarlösung (oder Milch) wird konz. Salpetersäure (HNO₃) getropft.
Beobachtung: Gelbfärbung
Mit konz. Salpetersäure färben sich Eiweißstoffe gelb. Bei dieser Probe reagieren die im Peptid enthaltenen aromatischen Aminosäuren (Tyrosin, Tryptophan) unter Nitrierung zu Nitrofarbstoffen. Positive Probe auch bei menschlicher Haut. -
6.1.4 Aldehydnachweise
6.1.4 Aldehydnachweise
a) Schiffsche-Probe mit Fuchsinschwefliger Säure
Fuchsinschweflige Säure ergibt mit Aldehyden eine rotviolette Farbe. Dieser Aldehydnachweis beruht nicht auf der Reduktionswirkung von Aldehyden!
b) Tollens-Probe (Silberspiegel)
Versuchsaufbau (gilt auch für Fehling-Probe)
Versuchsdurchführung:
Schutzbrille aufsetzen, weite Ärmel hochkrempeln, Haare zurückbinden.
- Gib in das RG etwa zwei fingerbreit Silbernitratlösung.
- Füge mit der Pipette tropfenweise verdünnte Ammoniaklösung hinzu, bis sich der entstehende Niederschlag gerade wieder auflöst.
- Gib nun in das RG zwei fingerbreit Probelösung.
- Stelle das RG in das heiße Wasserbad.
Beobachtung:
Es bildet sich ein Silberspiegel auf der Innenseite des Reagenzglas.
Auswertung:
Es bedeutet, dass sich die Silber-Ionen zu elementarem Silber reduzierthaben. Da eine Reduktion nur zusammen mit einer Oxidationablaufen, muss etwas anderes oxidiert worden sein. Da es ein Aldehyd-Nachweisist, kann man davon ausgehen, dass das C-Atom der Aldehyd-Gruppe oxidiertwurde. Da diese Reaktion in alkalischer Lösung abläuft (Ammoniak wurde dazugegeben), formuliert man mit Hilfe von Hydroxid-Ionen (OH⁻).
c) Fehling-Reagenz
Versuchsdurchführung:
Schutzbrille aufsetzen, weite Ärmel hochkrempeln, Haare zurückbinden.- Gib in das RG etwa 5 ml Fehling 1-Lösung und dann 5 ml Fehling 2-Lösung.
- Füge ein Spatellöffel Glucose zu.
- Stelle das RG nach kurzem Schütteln in das heiße Wasserbad.
Beobachtung:
Es bildet sich ein roter Niederschlag von Kupfer(I)-Oxid (Cu₂O).Auswertung:
Diese Reaktion verläuft recht analog zum Silberspiegel (Tollens-Reagens). Nur wird hierbei das Metall-Ion nicht komplett reduziert, sondern das Cu²⁺ wird zu Cu¹⁺ reduziert, wobei es sich sofort mit einem Oxid-Ion verbindet und den rötlichen Niederschlag bildet. Sauerstofflieferant ist auch in diesem Fall wie bei Tollens-Probe das Hydroxid-Ionen, da eine alkalische Lösung vorliegt.
Aufgabe: Versucht mit Hilfe der oberen Gleichung jetzt die Reaktionsgleichungen für das Fehlingreagenz zu formulieren.
{slider title="Lösung" open="false" class="icon"}
{/sliders}