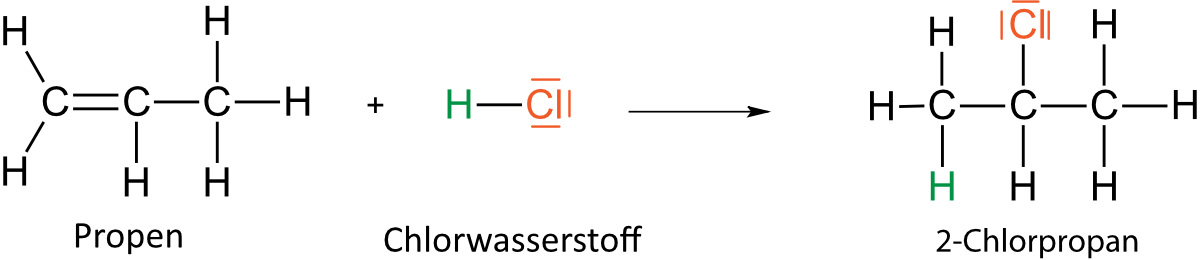Additionsreaktion
-
02 Alkene
Was du in diesem Kapitel lernst
Alkene sind Kohlenwasserstoffe mit mindestens einer C=C-Doppelbindung – der charakteristischen funktionellen Gruppe dieser Verbindungsklasse. Am Beispiel des Ethens (C2H4) lernst du Aufbau, Eigenschaften und typische Reaktionen der Alkene kennen: von der Bromwasserprobe über die cis-trans-Isomerie bis zur katalytischen Hydrierung.
Grundlagen aus der 10. Klasse
Alkene bauen direkt auf dem Wissen über die gesättigten Kohlenwasserstoffe auf – wiederhole bei Bedarf: → 1. Alkane – Homologe Reihe, Genfer Nomenklatur, radikalische Substitution
Kapitelübersicht – 2. Alkene
Klicke auf eine Kachel, um direkt zum Unterkapitel zu springen.
H₂C=CH₂2.1
Ethen
Eigenschaften · Summenformel · Strukturformel · Vorkommen & Verwendung
Br₂2.1.5
Nachweis von Alkenen
Bromwasserprobe · Elektrophile Addition · Reaktionsgleichung
cis
trans2.1.6 / 2.1.7
Isomerien von Alkenen
Konstitutions-Isomerie · cis-trans-Isomerie · (E/Z)-Nomenklatur
But-2-en2.2
Nomenklatur der Alkene
IUPAC-Benennung · Lokanten · Übungsaufgaben
+H₂/Ni2.3
Katalytische Hydrierung
Hydrierung ⇔ Eliminierung · Gleichgewicht · Katalysator Ni / Pt
sp²
sp³2.4
Vergleich Ethen – Ethan
Reaktivität · sp²- vs. sp³-Hybridisierung · π-Elektronensystem
Auf einen Blick – die wichtigsten Aussagen
Funktionelle Gruppe
Alkene sind ungesättigte Kohlenwasserstoffe. Ihre charakteristische funktionelle Gruppe ist die C=C-Doppelbindung (σ- + π-Bindung). Allgemeine Formel: CnH2n.
Nachweis
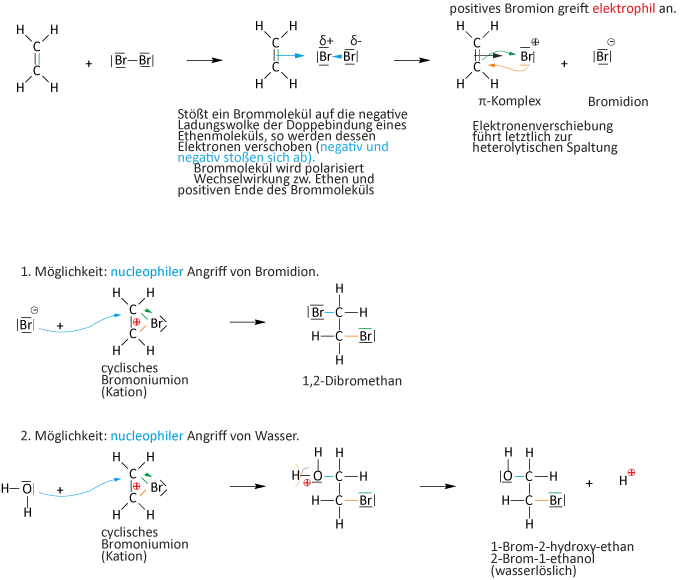
Die Bromwasserprobe weist C=C-Doppelbindungen nach: Braunes Bromwasser wird durch Additionsreaktion entfärbt – eindeutiger Nachweis auf Mehrfachbindungen.
cis-trans-Isomerie
Die Doppelbindung blockiert die freie Rotation um die C=C-Achse. Dadurch entstehen räumlich verschiedene cis- und trans-Isomere mit unterschiedlichen Eigenschaften.
Reaktionstyp
Typisch für Alkene ist die elektrophile Addition: Die Doppelbindung wird geöffnet, Atome oder Gruppen lagern sich an (z. B. H2, Br2, HBr).
Häufige Fragen – Alkene
Was sind Alkene und wie unterscheiden sie sich von Alkanen?
Alkene sind Kohlenwasserstoffe mit mindestens einer C=C-Doppelbindung. Im Gegensatz zu den gesättigten Alkanen (nur Einfachbindungen) sind Alkene ungesättigt: Die Doppelbindung besteht aus einer σ-Bindung und einer π-Bindung. Die allgemeine Summenformel lautet CnH2n. Das einfachste Alken ist Ethen (C2H4). Alkene sind durch ihre Doppelbindung reaktiver als Alkane; ihr typischer Reaktionstyp ist die elektrophile Addition, nicht die radikalische Substitution der Alkane.
Wie weist man eine C=C-Doppelbindung nach?
Den klassischen Nachweis liefert die Bromwasserprobe: Braunes Bromwasser (Br2 in Wasser) wird durch Additionsreaktion entfärbt, weil das Brom an die Doppelbindung addiert wird. Gleichung am Beispiel Ethen: C2H4 + Br2 → C2H4Br2 (1,2-Dibromethan). Der Test ist eindeutig für alle Verbindungen mit Mehrfachbindungen. → 2.1.5 Nachweis von Alkenen
Was ist cis-trans-Isomerie, und wann tritt sie auf?
Die C=C-Doppelbindung blockiert die freie Drehbarkeit um die Bindungsachse. Wenn an beiden Doppelbindungskohlenstoffen je zwei verschiedene Substituenten sitzen, entstehen zwei räumlich unterschiedliche Isomere: Im cis-Isomer (= Z-Form: zusammen) stehen die gleichartigen Gruppen auf derselben Seite der Doppelbindung; im trans-Isomer (= E-Form: entgegen) auf gegenüberliegenden Seiten. Beispiel: cis-But-2-en und trans-But-2-en haben dieselbe Summenformel (C4H8), aber verschiedene Siedepunkte. → 2.1.6/2.1.7 Isomerien von Alkenen
Wie werden Alkene nach IUPAC benannt?
Die Nomenklatur der Alkene folgt denselben Grundregeln wie bei den Alkanen, mit Besonderheiten: (1) Die längste Kette, die die Doppelbindung enthält, ist die Hauptkette. (2) Sie wird so nummeriert, dass die Doppelbindung die niedrigstmögliche Lokante erhält. (3) Die Endung lautet „-en" (mehrere Doppelbindungen: -dien, -trien). (4) Die Position der Doppelbindung steht als Lokant vor der Endung: z. B. But-1-en, nicht 1-Buten (moderne IUPAC-Schreibweise). Bei cis-trans-Isomeren wird das Konfigurationspräfix vorangestellt: cis-But-2-en oder (Z)-But-2-en. → 2.2 Nomenklatur der Alkene
Was ist katalytische Hydrierung, und wie verhält sie sich zur Eliminierung?
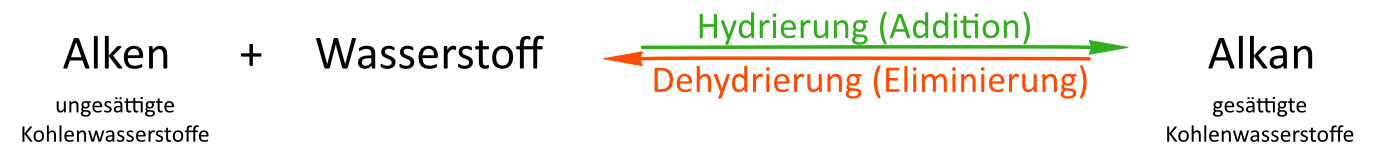
Katalytische Hydrierung und Eliminierung sind Umkehrreaktionen: Bei der Hydrierung wird H2 mithilfe eines Nickel- oder Platin-Katalysators an die C=C-Doppelbindung addiert → Alken wird zu Alkan (z. B. C2H4 + H2 → C2H6). Bei der Eliminierung wird H2 unter hoher Temperatur abgespalten → Alkan wird zu Alken. Die Gesamtreaktion ist umkehrbar: Ethen ⇔ Ethan. Wichtig: Der Katalysator beeinflusst nur die Reaktionsgeschwindigkeit, verschiebt aber die Gleichgewichtslage nicht. → 2.3 Katalytische Hydrierung
Lernkarten – Alkene
Klicke auf eine Karte, um die Antwort zu sehen.
1Was ist die funktionelle Gruppe der Alkene, und woraus besteht sie?
Die C=C-Doppelbindung. Sie besteht aus einer σ-Bindung (Überlappung entlang der Achse) und einer π-Bindung (seitliche Überlappung). Alkene sind deshalb ungesättigt und reaktiver als Alkane.
2Wie lautet die allgemeine Formel der Alkene? Nenne die ersten vier mit Formel.
CnH2n (n ≥ 2)
Ethen C2H4 · Propen C3H6
Buten C4H8 · Penten C5H103Wie funktioniert der Bromwassertest? Was beobachtet man?
Braunes Bromwasser wird mit dem Alken gemischt. Das Bromwasser entfärbt sich, weil Br2 durch elektrophile Addition an die C=C-Doppelbindung gebunden wird. → Nachweis auf Mehrfachbindung.
4Wann tritt cis-trans-Isomerie auf? Was unterscheidet cis von trans?
Wenn an beiden C-Atomen der C=C-Bindung je zwei verschiedene Substituenten sitzen. cis: gleichartige Gruppen auf einer Seite; trans: auf gegenüberliegenden Seiten. Freie Rotation um die Doppelbindung ist nicht möglich.
5Berechne: Wie viel g H2 werden benötigt, um 28 g Ethen vollständig zu hydrieren?
C2H4 + H2 → C2H6
M(C2H4) = 28 g/mol → n = 1 mol
Stöchiometrie 1:1 → n(H2) = 1 mol
m(H2) = 1 mol · 2 g/mol = 2 g H2
Weiter im Fach Chemie / 10. Klasse
← 1. Alkane → 3. Alkine ↑ Übersicht 10. Klasse
🔭 Vertiefung in der Kursstufe: Aromaten – Benzol und seine Derivate · Cycloalkane
-
02.1.5 Nachweis von Alkenen (Mehrfachbindungen)
2.1.5 Nachweis von Alkenen (Doppelbindung)
Versuch: Ein Erlenmeyerkolben wird unter Wasser mit 250 ml Ethen gefüllt, anschließend werden 0,5 ml Brom dazugegeben und mit dem Stopfen verschlossen.
Alternativ: Hexen + Bromwasser (VORSICHT FALLS MAN BROM NIMMT ⇨ heftige Reaktion)
Beobachtung:
Die Bromfarbe verschwindet; Volumenabnahme; der Erlenmeyerkolben wird warm; es entsteht ein flüssiges Produkt, die Dichte ist größer als 1 g/cm³.Auswertung:
Zwei Hypothesen:I) Substitution:
II) Addition:
ErgebnisBei der Reaktion Ethen + Brom entsteht (fast) nur ein Reaktionsprodukt. „Bromwasserstoffnebel“ waren kaum zu sehen. Es fand somit eine Addition statt.
Additionsreaktionen: Reaktionen bei denen sich zwei Moleküle zu einem Molekül vereinigen! Es kommt dabei zur Anlagerung von Atomen oder Atomgruppen an Doppelbindungen (Mehrfachbindun-gen).
Reaktionsmechanismus: AE-Reaktionen (elektrophile Addition)
= typische Reaktion von Alkenen
-
03 Alkine
Was du in diesem Kapitel lernst
Alkine sind Kohlenwasserstoffe mit mindestens einer C≡C-Dreifachbindung – noch reaktiver als die Alkene. Das wichtigste Alkin ist Ethin (Acetylen): du lernst seine Eigenschaften, seine technische Herstellung aus Calciumcarbid und die für Alkine typischen zweistufigen Additionsreaktionen kennen.
Grundlagen aus der 10. Klasse
Alkine bauen auf dem Wissen über ungesättigte Verbindungen auf – wiederhole bei Bedarf: → 2. Alkene – C=C-Doppelbindung, Bromwasserprobe, Additionsreaktion
Kapitelübersicht – 3. Alkine
Klicke auf eine Kachel, um direkt zum Unterkapitel zu springen.
3.1
Ethin (Acetylen)
Physikalische & chemische Eigenschaften · Summenformel C2H2 · Strukturformel · Bananenbindung
→ 3.1.1 Eigenschaften · 3.1.2 Formelermittlung3.1.3 – 3.1.5
Herstellung & Verwendung
Herstellung aus CaC2 · Carbidlampe · Verwendung als Brenngas & Ausgangsstoff
→ 3.1.3 Herstellung · 3.1.4 Carbidlampe · 3.1.5 Verwendung3.2
Reaktionstyp bei Alkinen
Elektrophile Addition · Bromierung · Wasseranlagerung · Übungsaufgaben
→ 3.2 Reaktionstyp & Übungen
Auf einen Blick – die wichtigsten Aussagen
Funktionelle Gruppe
Alkine besitzen eine C≡C-Dreifachbindung (1 σ- + 2 π-Bindungen). Die Bindungslänge ist mit 120 pm kürzer als bei der Doppelbindung (134 pm). Allgemeine Formel: CnH2n−2.
Herstellung
Ethin entsteht aus Calciumcarbid und Wasser: CaC2 + 2 H2O → C2H2 + Ca(OH)2. Diese Reaktion liefert das Gas auch in der Carbidlampe.
Reaktionstyp
Alkine reagieren durch elektrophile Addition. Die Reaktion läuft zweistufig ab: erst entsteht ein Alken-Zwischenprodukt, dann wird erneut addiert → schließlich ein Alkan oder Derivat.
Linearstruktur
Ethin ist linear: alle vier Atome liegen auf einer Geraden (Bindungswinkel 180°). Die Dreifachbindung besteht aus drei „Bananenbindungen" (sp-Hybridisierung).
Häufige Fragen – Alkine
Was sind Alkine, und was unterscheidet sie von Alkenen?
Alkine sind Kohlenwasserstoffe mit mindestens einer C≡C-Dreifachbindung, bestehend aus einer σ-Bindung und zwei π-Bindungen. Die allgemeine Formel lautet CnH2n−2 (noch zwei H-Atome weniger als bei Alkenen: CnH2n). Alkine sind durch die Dreifachbindung noch reaktiver als Alkene. Das einfachste Alkin ist Ethin (C2H2), auch Acetylen genannt. Wie Alkene zeigen Alkine elektrophile Additionsreaktionen, jedoch oft zweistufig.
Wie wird Ethin (Acetylen) technisch hergestellt?
Ethin lässt sich aus Calciumcarbid (CaC2) und Wasser herstellen. Reaktionsgleichung: CaC2 + 2 H2O → C2H2 + Ca(OH)2. Calciumcarbid wird in der Carbidlampe (Grubenlampe) genutzt: Das entstehende Ethin verbrennt mit einer hellen, stark leuchtenden Flamme. Industriell wird Ethin heute hauptsächlich durch Cracken von Erdgas gewonnen. → 3.1.3 Herstellung
Was ist die Besonderheit der linearen Struktur von Ethin?
Beim Ethin sind alle vier Atome linear angeordnet (Bindungswinkel 180°, sp-Hybridisierung). Die C≡C-Dreifachbindung besteht nach dem Bananenbindungsmodell aus drei gebogenen Bindungen (σ + 2 π). Die Bindungslänge beträgt nur 120 pm (zum Vergleich: C=C 134 pm, C–C 154 pm). Diese kompakte Struktur erklärt die hohe Reaktivität und die ausgeprägte elektrophile Addition. → 3.1 Ethin
Wie verläuft die Bromierung von Ethin – und warum ist sie zweistufig?
Ethin reagiert mit Brom in einer elektrophilen Addition, die zweistufig abläuft: In der ersten Stufe addiert Br2 an die Dreifachbindung → es entsteht das Zwischenprodukt trans-1,2-Dibromethen (noch eine Doppelbindung vorhanden). In der zweiten Stufe reagiert dieses mit weiterem Br2 → 1,1,2,2-Tetrabromethan (gesättigtes Endprodukt). Wird Br2 im Unterschuss eingesetzt, kann man die Reaktion auf der Dibromstufe stoppen. → 3.2 Reaktionstyp
Welche Verwendungen hat Ethin in Industrie und Technik?
Ethin (Acetylen) wird vielfältig genutzt: (1) Autogenschweißen und Schneiden: Die Verbrennung mit Sauerstoff erzeugt eine Flamme von über 3000 °C. (2) Ausgangsstoff in der Chemie: Aus Ethin werden wichtige Kunststoffe und Lösungsmittel hergestellt (z. B. PVC über Vinylchlorid). (3) Carbidlampen: Historisch als tragbare Lichtquelle in Bergbau und Feuerwehr. (4) Bei Pflanzen spielt das analoge Ethylen (= Ethen) als Phytohormon eine Rolle – Ethin kann diese Wirkung verstärken.
Lernkarten – Alkine
Klicke auf eine Karte, um die Antwort zu sehen.
1Was ist die funktionelle Gruppe der Alkine, und woraus besteht sie?
Die C≡C-Dreifachbindung. Sie besteht aus einer σ-Bindung + zwei π-Bindungen. Bindungslänge: 120 pm. Hybridisierung: sp. Alle vier Atome in Ethin sind linear angeordnet (180°).
2Wie lautet die allgemeine Formel der Alkine? Nenne Ethin und Propin mit Formel.
CnH2n−2 (n ≥ 2)
Ethin: C2H2 (HC≡CH)
Propin: C3H4 (CH3–C≡CH)3Wie wird Ethin aus Calciumcarbid hergestellt? Nenne die Reaktionsgleichung.
CaC2 + 2 H2O
→ C2H2 + Ca(OH)2
Calciumcarbid reagiert mit Wasser zu Ethin und Calciumhydroxid.4Wie verläuft die Bromierung von Ethin – welche zwei Stufen gibt es?
Stufe 1: C2H2 + Br2 → C2H2Br2 (trans-1,2-Dibromethen, noch C=C)
Stufe 2: + Br2 → C2H2Br4 (1,1,2,2-Tetrabromethan)5Berechne: Wie viel g Br2 werden benötigt, um 26 g Ethin vollständig zu tetrabromieren?
C2H2 + 2 Br2 → C2H2Br4
M(C2H2) = 26 g/mol → n = 1 mol
n(Br2) = 2 mol → m = 2 · 160 g/mol = 320 g Br2
Weiter im Fach Chemie / 10. Klasse
← 2. Alkene → 5. Alkohole ↑ Übersicht 10. Klasse
🔭 Vertiefung in der Kursstufe: Cycloalkane · Aromaten – Benzol und seine Derivate
-
04.1.2 Halbacetalbildung
4.1.2 Halbacetalbildung bei Zucker (z.B. Glucose)
a) Strukur eines Aldehyds (Alkanals)
Folgende Abbildung zeigt, wie eine Aldehydgruppe angegriffen werden. Durch die höhere Elektronegativität des Sauerstoffatoms werden die Elektronen vom Kohlenstoff weg hin zum Sauerstoff gezogen (polare Atombindung). Dadurch kann am Kohlenstoff ein nucleophiles (kernliebendes Teilchen) angreifen. Nucleophile Teilchen besitzen ein freies Elektronenpaar, mit dem es angreifen kann.Der Sauerstoff der Aldehydgruppe besitzt ein freies Elektronenpaar. Hier kann ein elektrophiles Teilchen (wie z.B. ein H+ (Proton)) angreifen.
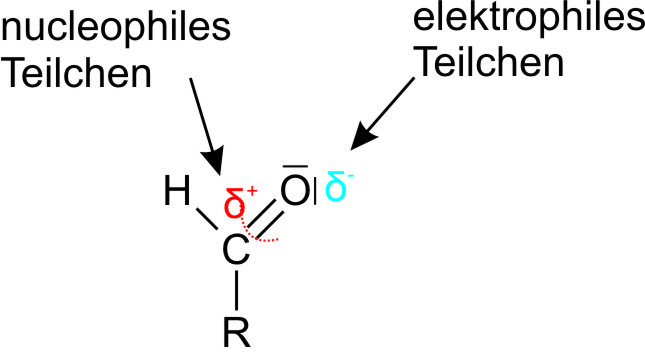
Das Aldehydmolekül enthält eine polare Doppelbindung mit freien Elektronenpaaren; Additionsreaktionen sind möglich.b) Aldehyd + Alkohol (AN-Reaktion = nucleophile Addition)
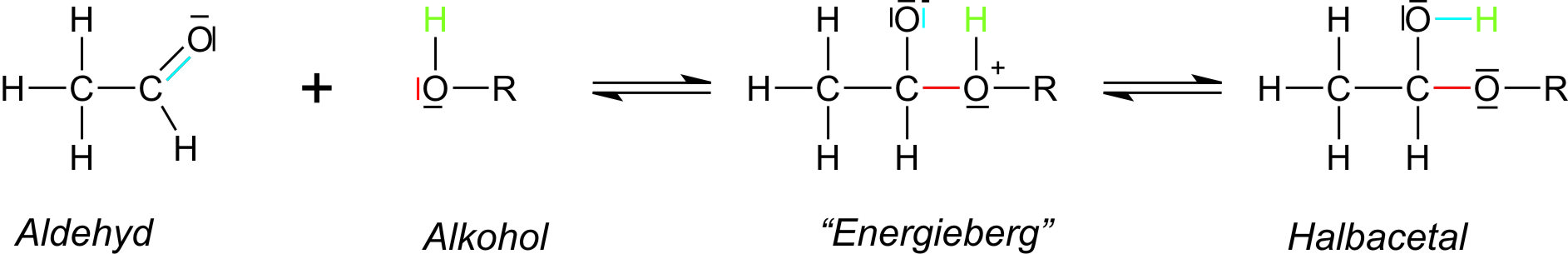
Halbacetale kann man selten isolieren (Ausnahme: Zucker). Ein Halbacetal kann mit Alkohol zu einem Vollacetal weiterreagieren (vgl. Disaccharide).
-
04.1.3 Ringstruktur der Monosaccharide
4.1.3 Ringstruktur der Monosaccharide
Widersprüche:
- Schiffsche Reagenz (typ. Nachweis für Aldehyde) zeigt keine Farbreaktion.
- Drehwinkel in wässriger Lsg. 52,7° statt 112,2°.
- Tollens (1883) schloss daraus, dass Glucose nicht in der offenen Aldehydform vorliegt.
- Die Ursache hierfür ist in der intramolekularen Verknüpfung der Carbonylgruppe mit einer Hydroxylgruppe des gleichen Zuckermoleküls zu suchen. Es kommt also zu einer innermolekularen Halbacetalbildung.
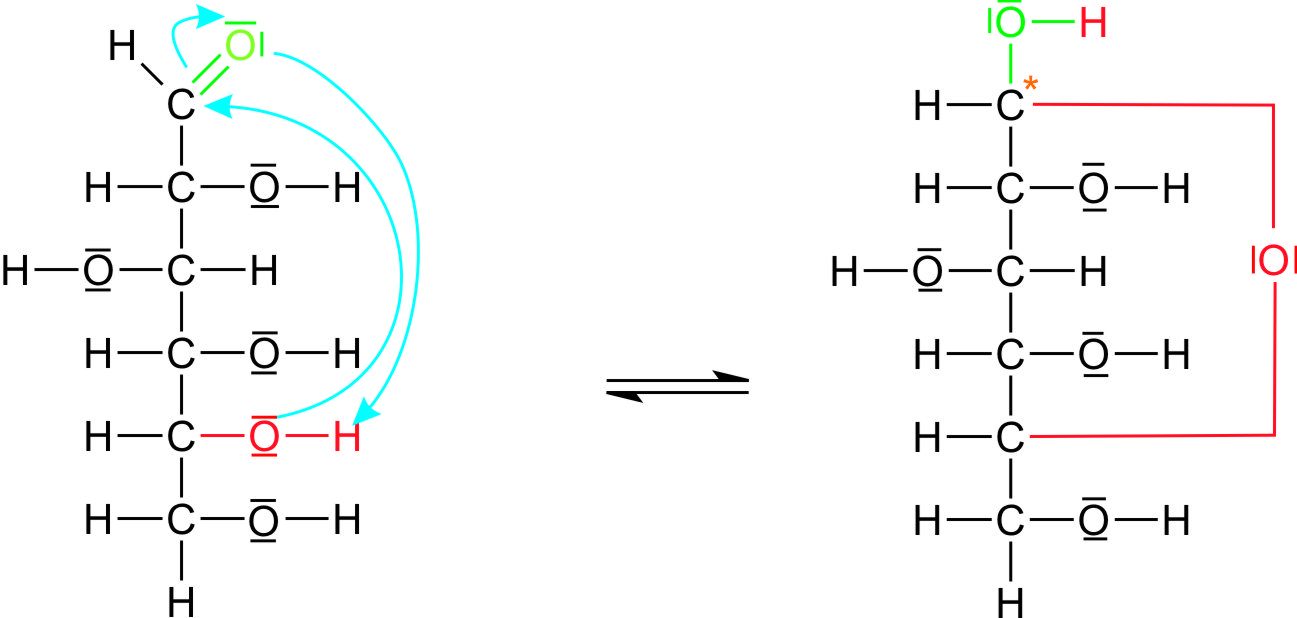
Haworth-Schreibweise- zyklisches Glucose Molekül wird als liegendes Sechseck [Pyranosen] oder Fünfeck [Furanosen] gezeichnet;
- Ringsauerstoffatom findet sich in der rechten hinteren Ecke [Pyranosen] bzw. im hinteren Eck [Furanosen];
- Substituenten, die in der FISCHERprojektion nach links weisen, stehen in der HAWORTH-Projektion oben ["Kommunistenregel"]
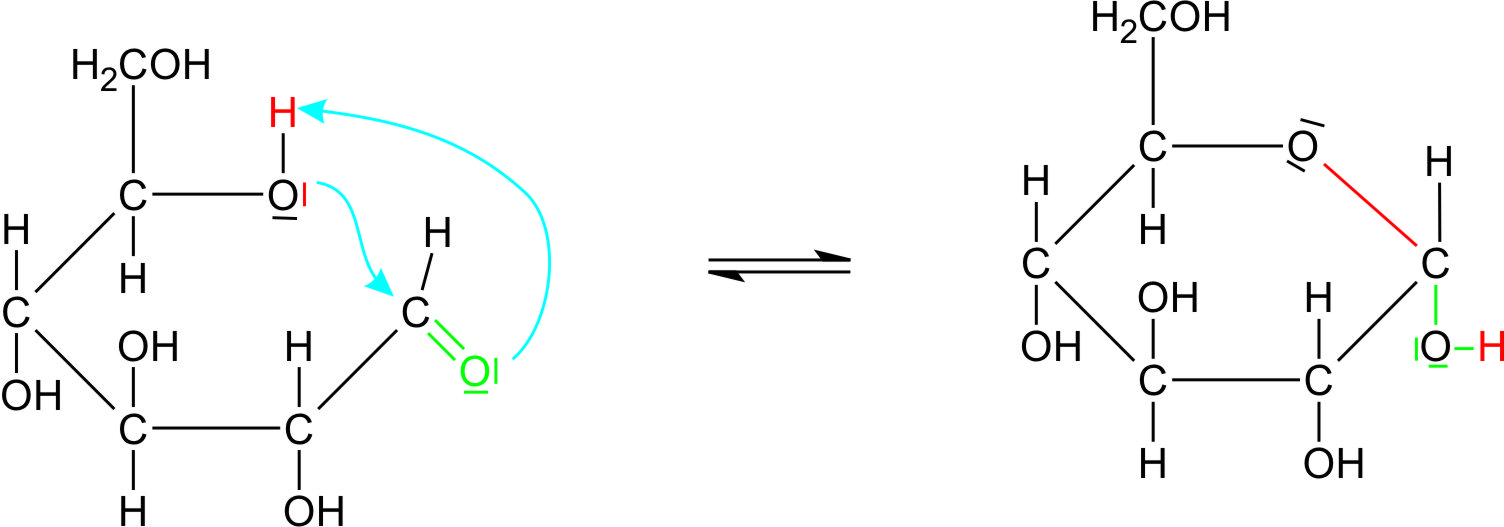
Erklärung der negativen Reaktion der Glucose mit der Schiffschen Reagenz: Es liegt ein Gleichgewicht zwischen der offenen Kette und dem Ring vor, wobei der Anteil der offenen Kette, bei der wirklich ein Aldehyd vorliegt verschwindend gering ist (< 1%):
Aldehydform (offenkettig) ⇌ Halbacetalform (Ring)- Fuchsinschweflige Säure (Schiffsches Reagenz) bildet mit dem Aldehyd eine reversible (umkehrbare) Reaktion, daher findet kein Entzug des Aldehyds statt. Das heißt, es gibt keine GG-Verschiebung und damit keinen wirklichen Aldehydnachweis (der Anteil an offener aldehydhaltigen Glucose ist zu gering).
- Bei der Fehling-Probe und der Tollens-Probe (Silberspiegel) findet eine GG-Verschiebung statt! Die offene Form wird laufend entzogen, neue Ringe gehen auf und es findet langsam der Aldehydnachweis statt.
Durch Ringbildung entstehen 2 Strukturisomere der D-(+)-Glucose (keine Spiegelbildisomere).
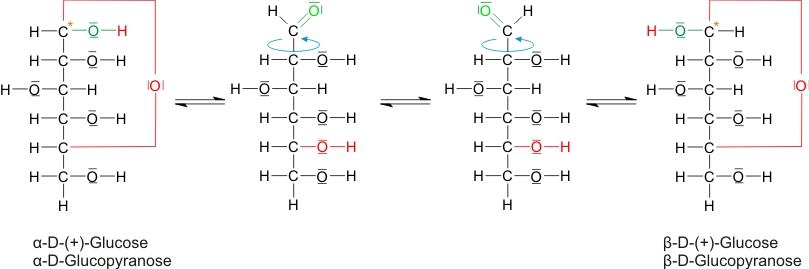
In wässriger Lösung liegen vor:36% 0,26% 64%
Drehwinkel: 112,2° 18,7°
Es entsteht ein neues asymmetrisches C-Atom (= anomeres Kohlenstoffatom) und damit 2 Diasteromere. Anomere = Isomere, die sich nur durch die Stellung der Hydroxylgruppen am anomeren Kohlenstoffatom unterscheiden.
α-Form: OH-Gruppe am neuen asymmetrischen C-Atom liegt auf derselben Seite wie die am untersten asymmetrischen C-Atom.
Muta1rotation: Drehwinkel einer Lösung einer optisch aktiven Substanz ändert sich vom Zeitpunkt des Ansetzens der Lösung kontinuierlich bis zum Erreichen eines festen Wertes. Grund dafür ist, dass man z.B. α-Glucose in eine wässrige Lösung gibt. Sobald sich das Molekül in Wasser löst, öffnen sich einige wenige Moleküle. Bei der erneuten Ringbildung, bildet sich auch β-Glucose. Erst wenn sich der Anteil wie oben angegeben einstellt, ändert sich der Drehwinkel nicht mehr.Glucose α-Form ⇌ offene Form ⇌ β-Form
Bei Glucose ist der Endwert: 0,36 * 112,2° + 0,64 * 18,7° = 52,36°
Haworth-Schreibweise
Achtet auf die Durchnummerierung der C-Atome. Am C1 war ursprünglich die Aldehydgruppe.
α-D-Glucose β-D-Glucose
Nachweis von Glucose: GOD-Test (Glucose-Oxidase-Stäbchen); Achtung beim schriftlichen Abitur: Fehling oder Tollens ist kein Nachweis für Glucose, sondern nur für Aldehydgruppen!- Glucose-Oxidase = Enzym: Oxidiert Glucose am C1-Atom zu Gluconsäure und Wasserstoffperoxid (H2O2).
- Durch das Enzym Peroxidase (z.B. aus Meerettich) wird das Wasserstoffperoxid zu Wasser reduziert.
- je mehr Glucose, umso intensiver die Farbe.
Im Handel als Teststreifen für Diabeteserkrankung.
-----
-
04.1.7 Glycosid- bzw. Vollacetalbildung
zu 4.1.7 Reaktionen der Monosaccharide
Glycosidbildung (~Halbacetal, Vollacetal)
a) Aldehyd + Alkohol ⇌ Halbacetal (nucleophile Addition)
b) Halbacetal + Alkohol ⇌ (Voll)Acetal + WasserTypische Kondensationsreaktion (unter Wasserabspaltung)
Beispiel:
β-D-Glucose + Methanol ⇌ β-Methyl-Glucosid + Wasser
Zucker + Alkohol ⇌ Glycosid + Wasser
Fructose + Alkohol ⇌ Fructosid + Wasser
Glucose + Alkohol ⇌ Glucosid + Wasser
Reaktionen von Zuckern untereinander ergeben Di-, Oligo- und Polysaccharide. -
2.3 Katalytische Hydrierung
2.3 Katalytische Hydrierung
Hinweis: Markownikow-Regel: Bei Addition von z.B. Halogenwasserstoff bekommt das wasserstoffhaltigere C-Atom bekommt das H; das wasserstoffärmere Atom bekommt dann das Halogen. "Wer hat, dem wird gegeben" [bezieht sich auf H-Atome].
a) Alle Alkene lassen sich zu Alkane hydrieren.Hierbei handelt es sich um eine Redoxreaktion! Kohlenstoff wird reduziert (Oxidationszahlerniedrigung), H wird oxidiert. Hydrierung: Reduktion von Kohlenstoff
Die Dehydrierung ist die Umkehrung der Hydrierung: Oxidation von Kohlenstoff
b) Allgemein: Die Hydrierung ist eine umkehrbare Reaktion (Dehydrierung)
Eliminierungsreaktionen: Abspaltung kleiner Moleküle!
Übungsaufgabe:
An Propen wird Chlorwasserstoff addiert. Formuliere hierfür eine Reaktionsgleichung in Strukturformeln mit bindenden und nichtbindenden Elektronenpaaren. Beachte dabei auch die Markownikow-Regel (siehe oben).
{slider title="Lösung" open="false" class="icon"}
{/sliders}