Alkene
-
02 Alkene
Was du in diesem Kapitel lernst
Alkene sind Kohlenwasserstoffe mit mindestens einer C=C-Doppelbindung – der charakteristischen funktionellen Gruppe dieser Verbindungsklasse. Am Beispiel des Ethens (C2H4) lernst du Aufbau, Eigenschaften und typische Reaktionen der Alkene kennen: von der Bromwasserprobe über die cis-trans-Isomerie bis zur katalytischen Hydrierung.
Grundlagen aus der 10. Klasse
Alkene bauen direkt auf dem Wissen über die gesättigten Kohlenwasserstoffe auf – wiederhole bei Bedarf: → 1. Alkane – Homologe Reihe, Genfer Nomenklatur, radikalische Substitution
Kapitelübersicht – 2. Alkene
Klicke auf eine Kachel, um direkt zum Unterkapitel zu springen.
H₂C=CH₂2.1
Ethen
Eigenschaften · Summenformel · Strukturformel · Vorkommen & Verwendung
Br₂2.1.5
Nachweis von Alkenen
Bromwasserprobe · Elektrophile Addition · Reaktionsgleichung
cis
trans2.1.6 / 2.1.7
Isomerien von Alkenen
Konstitutions-Isomerie · cis-trans-Isomerie · (E/Z)-Nomenklatur
But-2-en2.2
Nomenklatur der Alkene
IUPAC-Benennung · Lokanten · Übungsaufgaben
+H₂/Ni2.3
Katalytische Hydrierung
Hydrierung ⇔ Eliminierung · Gleichgewicht · Katalysator Ni / Pt
sp²
sp³2.4
Vergleich Ethen – Ethan
Reaktivität · sp²- vs. sp³-Hybridisierung · π-Elektronensystem
Auf einen Blick – die wichtigsten Aussagen
Funktionelle Gruppe
Alkene sind ungesättigte Kohlenwasserstoffe. Ihre charakteristische funktionelle Gruppe ist die C=C-Doppelbindung (σ- + π-Bindung). Allgemeine Formel: CnH2n.
Nachweis
Die Bromwasserprobe weist C=C-Doppelbindungen nach: Braunes Bromwasser wird durch Additionsreaktion entfärbt – eindeutiger Nachweis auf Mehrfachbindungen.
cis-trans-Isomerie
Die Doppelbindung blockiert die freie Rotation um die C=C-Achse. Dadurch entstehen räumlich verschiedene cis- und trans-Isomere mit unterschiedlichen Eigenschaften.
Reaktionstyp
Typisch für Alkene ist die elektrophile Addition: Die Doppelbindung wird geöffnet, Atome oder Gruppen lagern sich an (z. B. H2, Br2, HBr).
Häufige Fragen – Alkene
Was sind Alkene und wie unterscheiden sie sich von Alkanen?
Alkene sind Kohlenwasserstoffe mit mindestens einer C=C-Doppelbindung. Im Gegensatz zu den gesättigten Alkanen (nur Einfachbindungen) sind Alkene ungesättigt: Die Doppelbindung besteht aus einer σ-Bindung und einer π-Bindung. Die allgemeine Summenformel lautet CnH2n. Das einfachste Alken ist Ethen (C2H4). Alkene sind durch ihre Doppelbindung reaktiver als Alkane; ihr typischer Reaktionstyp ist die elektrophile Addition, nicht die radikalische Substitution der Alkane.
Wie weist man eine C=C-Doppelbindung nach?
Den klassischen Nachweis liefert die Bromwasserprobe: Braunes Bromwasser (Br2 in Wasser) wird durch Additionsreaktion entfärbt, weil das Brom an die Doppelbindung addiert wird. Gleichung am Beispiel Ethen: C2H4 + Br2 → C2H4Br2 (1,2-Dibromethan). Der Test ist eindeutig für alle Verbindungen mit Mehrfachbindungen. → 2.1.5 Nachweis von Alkenen
Was ist cis-trans-Isomerie, und wann tritt sie auf?
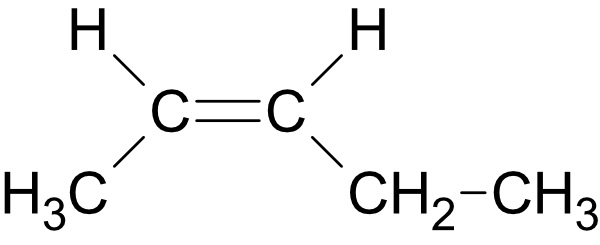
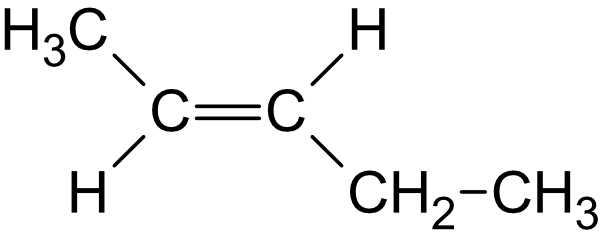
Die C=C-Doppelbindung blockiert die freie Drehbarkeit um die Bindungsachse. Wenn an beiden Doppelbindungskohlenstoffen je zwei verschiedene Substituenten sitzen, entstehen zwei räumlich unterschiedliche Isomere: Im cis-Isomer (= Z-Form: zusammen) stehen die gleichartigen Gruppen auf derselben Seite der Doppelbindung; im trans-Isomer (= E-Form: entgegen) auf gegenüberliegenden Seiten. Beispiel: cis-But-2-en und trans-But-2-en haben dieselbe Summenformel (C4H8), aber verschiedene Siedepunkte. → 2.1.6/2.1.7 Isomerien von Alkenen
Wie werden Alkene nach IUPAC benannt?
Die Nomenklatur der Alkene folgt denselben Grundregeln wie bei den Alkanen, mit Besonderheiten: (1) Die längste Kette, die die Doppelbindung enthält, ist die Hauptkette. (2) Sie wird so nummeriert, dass die Doppelbindung die niedrigstmögliche Lokante erhält. (3) Die Endung lautet „-en" (mehrere Doppelbindungen: -dien, -trien). (4) Die Position der Doppelbindung steht als Lokant vor der Endung: z. B. But-1-en, nicht 1-Buten (moderne IUPAC-Schreibweise). Bei cis-trans-Isomeren wird das Konfigurationspräfix vorangestellt: cis-But-2-en oder (Z)-But-2-en. → 2.2 Nomenklatur der Alkene
Was ist katalytische Hydrierung, und wie verhält sie sich zur Eliminierung?
Katalytische Hydrierung und Eliminierung sind Umkehrreaktionen: Bei der Hydrierung wird H2 mithilfe eines Nickel- oder Platin-Katalysators an die C=C-Doppelbindung addiert → Alken wird zu Alkan (z. B. C2H4 + H2 → C2H6). Bei der Eliminierung wird H2 unter hoher Temperatur abgespalten → Alkan wird zu Alken. Die Gesamtreaktion ist umkehrbar: Ethen ⇔ Ethan. Wichtig: Der Katalysator beeinflusst nur die Reaktionsgeschwindigkeit, verschiebt aber die Gleichgewichtslage nicht. → 2.3 Katalytische Hydrierung
Lernkarten – Alkene
Klicke auf eine Karte, um die Antwort zu sehen.
1Was ist die funktionelle Gruppe der Alkene, und woraus besteht sie?
Die C=C-Doppelbindung. Sie besteht aus einer σ-Bindung (Überlappung entlang der Achse) und einer π-Bindung (seitliche Überlappung). Alkene sind deshalb ungesättigt und reaktiver als Alkane.
2Wie lautet die allgemeine Formel der Alkene? Nenne die ersten vier mit Formel.
CnH2n (n ≥ 2)
Ethen C2H4 · Propen C3H6
Buten C4H8 · Penten C5H103Wie funktioniert der Bromwassertest? Was beobachtet man?
Braunes Bromwasser wird mit dem Alken gemischt. Das Bromwasser entfärbt sich, weil Br2 durch elektrophile Addition an die C=C-Doppelbindung gebunden wird. → Nachweis auf Mehrfachbindung.
4Wann tritt cis-trans-Isomerie auf? Was unterscheidet cis von trans?
Wenn an beiden C-Atomen der C=C-Bindung je zwei verschiedene Substituenten sitzen. cis: gleichartige Gruppen auf einer Seite; trans: auf gegenüberliegenden Seiten. Freie Rotation um die Doppelbindung ist nicht möglich.
5Berechne: Wie viel g H2 werden benötigt, um 28 g Ethen vollständig zu hydrieren?
C2H4 + H2 → C2H6
M(C2H4) = 28 g/mol → n = 1 mol
Stöchiometrie 1:1 → n(H2) = 1 mol
m(H2) = 1 mol · 2 g/mol = 2 g H2
Weiter im Fach Chemie / 10. Klasse
← 1. Alkane → 3. Alkine ↑ Übersicht 10. Klasse
🔭 Vertiefung in der Kursstufe: Aromaten – Benzol und seine Derivate · Cycloalkane
-
02.1 Ethen
2 Alkene
2.1 Ethen
2.1.1 Eigenschaften
- farbloses, brennbares Gas;
- die Flamme leuchtet stärker als bei Methan und Ethan;
- Siedetemperatur: -104°C
- Schmelztemperatur: - 169°C
2.1.2 Ermittlung der Summenformel
a) Qualitative Analyse (Verbrennungsanalyse)
Bei der vollständigen Verbrennung von Ethen entstehen H2O und CO2.
b) Quantitative Analyse (Bestimmung der molaren Masse)
Die molare Masse von Ethen: M(Ethen) = 28 g/mol
Die Molekülmasse von Ethen: 28 u
c) Summenformel (Molekülformel): C2H4
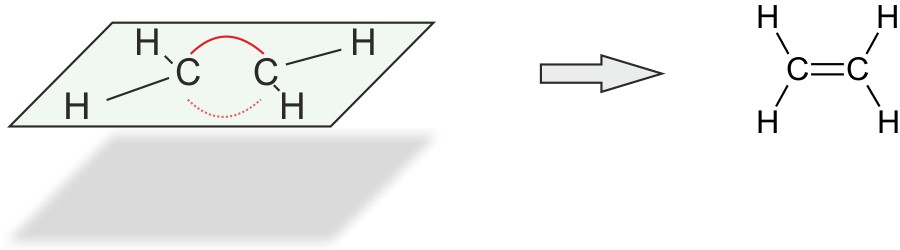
2.1.3 Strukturformel
Die Doppelbindung zwischen den beiden C-Atomen wird durch zwei Elektronenpaare gebildet. Diese stoßen sich ab. Man spricht von einer „Bogenbindung“ („Bananenbindung“).
Im Ethen Molekül betragen die Bindungswinkel 120°.
Alle Atome liegen in einer Ebene.
Die C=C-Doppelbindung verhindert die freie Drehbarkeit um die C-C-Achse.Aufgabe: Wie viel Liter Luft benötigt man bei der Verbrennung von 2 l Ethen
{slider title="Lösung" open="false" class="icon"}
C2H4 + 3 O2 → 2 CO2 + 2 H2O
1 Molekül 3 Moleküle 2 Moleküle 2 Moleküle
Stoffmenge n: 1mol 3 mol 2 mol 2 mol
Mol. Volumen V 22,4 L 67,2 L 44,8 L
Dreisatz: x/2L = 67,7L/22,4L
Zur Vollständigen Verbrennung von 2 L Ethen benötigt man 6 L Sauerstoff, d.h. 30 L Luft.
{/sliders}
.
2.1.4 Vorkommen, Gewinnung und Verwendung
a) Vorkommen
Bei Pflanzen als Hormon (Phytohormon). Steuert:
- Fruchtreifung
- Keimwachstum
- Entwicklung
- Dickenwachstum
- Blattfall
- Informationsweitergabe an benachbarte Pflanzen
b) Gewinnung
- Cracken von Erdöl
c) Verwendung
- Reifung von Früchten
- Herstellung von organischen Stoffen (Kunststoffe, Tenside,...)
-
02.1.5 Nachweis von Alkenen (Mehrfachbindungen)
2.1.5 Nachweis von Alkenen (Doppelbindung)
Versuch: Ein Erlenmeyerkolben wird unter Wasser mit 250 ml Ethen gefüllt, anschließend werden 0,5 ml Brom dazugegeben und mit dem Stopfen verschlossen.
Alternativ: Hexen + Bromwasser (VORSICHT FALLS MAN BROM NIMMT ⇨ heftige Reaktion)
Beobachtung:
Die Bromfarbe verschwindet; Volumenabnahme; der Erlenmeyerkolben wird warm; es entsteht ein flüssiges Produkt, die Dichte ist größer als 1 g/cm³.Auswertung:
Zwei Hypothesen:I) Substitution:
II) Addition:
ErgebnisBei der Reaktion Ethen + Brom entsteht (fast) nur ein Reaktionsprodukt. „Bromwasserstoffnebel“ waren kaum zu sehen. Es fand somit eine Addition statt.
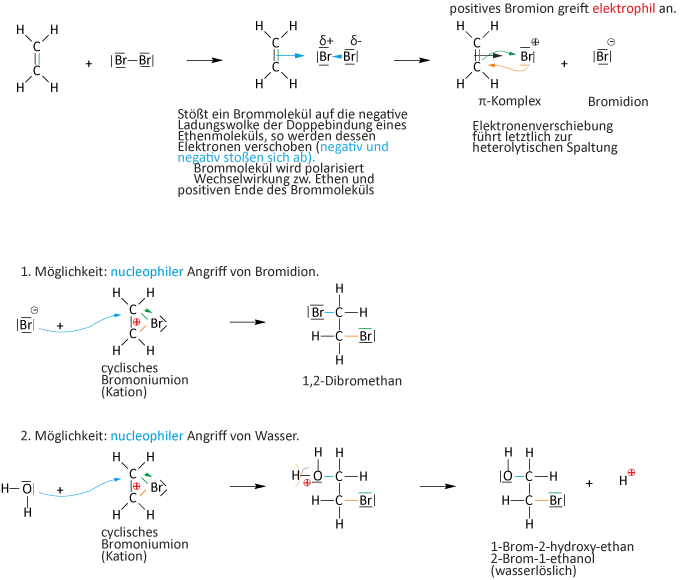
Additionsreaktionen: Reaktionen bei denen sich zwei Moleküle zu einem Molekül vereinigen! Es kommt dabei zur Anlagerung von Atomen oder Atomgruppen an Doppelbindungen (Mehrfachbindun-gen).
Reaktionsmechanismus: AE-Reaktionen (elektrophile Addition)
= typische Reaktion von Alkenen
-
10. Klasse
Was du auf dieser Seite findest
In der 10. Klasse dreht sich alles um die Organische Chemie (Baden-Württemberg). Von den gesättigten Alkanen über Alkene und Alkine bis zu Alkoholen, Carbonylverbindungen und Carbonsäuren – hier findest du alle Kapitel direkt verlinkt.
Kapitel im Überblick
Kapitel 1
Alkane
Methan · Butan · homologe Reihe · Nomenklatur · radikalische Substitution
Kapitel 2
Alkene
Ethen · Doppelbindung · Nachweis · elektrophile Addition · Isomerie
Kapitel 3
Alkine
Ethin · Dreifachbindung · Bananenbindung · Herstellung
Kapitel 4 · bei ausreichend Zeit
Cycloverbindungen
Cycloalkane · (vertieft in der Kursstufe → Aromaten)
Kapitel 5
Alkohole (Alkanole)
Ethanol · Hydroxylgruppe · prim./sek./tert. · mehrwertige Alkohole
Kapitel 6
Carbonylverbindungen
Alkanale (Aldehyde) · Alkanone (Ketone) · Carbonylgruppe · Nachweise
Kapitel 7
Carbonsäuren
Essigsäure · Carboxylgruppe · ZMK · Säure-Base-Reaktionen
Kapitel 8 · ⚠️ noch nicht online
Ester
Veresterung · Estergleichgewicht (→ Kursstufe: Gleichgewichtsreaktionen)
Vollständige Inhaltsübersicht
1 Alkane
- 1.1 Methan
- 1.4 Butan
- 1.5 Homologe Reihe der Alkane
- 1.6 Genfer Nomenklatur der Alkane | → Übungen
- 1.7 Eigenschaften der Alkane
- 1.8 Angriffsfreudige Teilchen (Radikale)
- 1.9 Radikalische Substitution – Halogenalkane
2 Alkene
- 2.1 Ethen
- 2.1.5 Nachweis von Alkenen (Mehrfachbindungen)
- 2.1.6 Isomerien von Alkenen
- 2.2 Nomenklatur der Alkene
- 2.3 Katalytische Hydrierung
- 2.4 Vergleich Ethen / Ethan
3 Alkine
4 Cycloverbindungen (bei ausreichend Zeit)
- → Cycloalkane (Kursstufe) – kein eigener Klasse-10-Artikel
5 Alkohole (Alkanole)
- 5.1 Alkanol, Alkohol (Ethanol)
- 5.1.3 Formelermittlung von Ethanol | → Teil II
- 5.1.4 Versuch: Ethanol + Alkalimetall
- 5.1.5 Induktiver Effekt
- 5.2 Homologe Reihe der Alkohole
- 5.2.4 Primäre, sekundäre und tertiäre Alkohole
- 5.2.6 Mehrwertige Alkohole
- 5.3 Chemische Reaktionen von Alkoholen
6 Carbonylverbindungen (Alkanale und Alkanone)
- 6.1.1 Herstellung von Alkanalen
- 6.1.2 Funktionelle Gruppe der Alkanale (Aldehyde)
- 6.1.4 Aldehydnachweise
- 6.2 Alkanone (Ketone)
- 6.3 Unterscheidung Aldehyde / Ketone
7 Carbonsäuren
- 7.1 Essigsäure (Ethansäure)
- 7.2 Funktionelle Gruppe der Monocarbonsäuren
- 7.3 Vergleich der Siedepunkte – ZMK
- 7.4.1 Säure-Base-Reaktionen
- 7.4.2 Redoxreaktion Essigsäure + Magnesium
8 Ester (noch kein eigener Artikel)
- → Estergleichgewicht (Kursstufe: Gleichgewichtsreaktionen) – kein eigener Klasse-10-Artikel
Auf einen Blick – Organische Chemie Klasse 10
Homologe Reihe
Alkane, Alkene, Alkine und Alkanole bilden je eine homologe Reihe mit gleicher funktioneller Gruppe und sich regelmäßig ändernden Eigenschaften (je +CH₂).
Funktionelle Gruppe
Die funktionelle Gruppe bestimmt die chemischen Eigenschaften: –OH (Alkanole) · C=O (Carbonylverbindungen) · –COOH (Carbonsäuren).
Reaktionstypen
Alkane: radikalische Substitution · Alkene: elektrophile Addition · Alkohole: Oxidation zu Aldehyden/Ketonen · Carbonsäuren: Veresterung.
ZMK & Siedepunkte
Van-der-Waals-Kräfte (Alkane, Alkene) < Dipol-Kräfte < Wasserstoffbrücken (Alkanole, Carbonsäuren). Je stärker die ZMK, desto höher der Siedepunkt.
Häufige Fragen – Organische Chemie Klasse 10
Was ist eine homologe Reihe?
Eine homologe Reihe ist eine Gruppe organischer Verbindungen mit gleicher funktioneller Gruppe und gleichem Reaktionsverhalten, deren Glieder sich jeweils um eine CH₂-Einheit unterscheiden. Mit steigender Kettenlänge nehmen Siedepunkt und Viskosität zu, während die Löslichkeit in Wasser meist abnimmt. Beispiele: Methan–Ethan–Propan–Butan (Alkane) oder Methanol–Ethanol–Propanol (Alkohole).
Was versteht man unter einer funktionellen Gruppe?
Eine funktionelle Gruppe ist ein Atom oder eine Atomgruppe im Molekül, die das typische chemische Verhalten einer Stoffklasse bestimmt. In der Organischen Chemie der 10. Klasse begegnen dir: die Hydroxylgruppe –OH (Alkohole), die Carbonylgruppe C=O (Aldehyde und Ketone) und die Carboxylgruppe –COOH (Carbonsäuren).
Was unterscheidet Alkane, Alkene und Alkine voneinander?
Alkane (Formel CₙH₂ₙ₊₂) besitzen nur Einfachbindungen und reagieren durch radikalische Substitution. Alkene (CₙH₂ₙ) haben mindestens eine C=C-Doppelbindung und reagieren typischerweise durch elektrophile Addition. Alkine (CₙH₂ₙ₋₂) besitzen eine C≡C-Dreifachbindung und sind reaktiver als Alkane, aber ähnlich wie Alkene durch Addition reaktiv. → Vergleich Ethen/Ethan
Was ist der Unterschied zwischen primären, sekundären und tertiären Alkoholen?
Bei einem primären Alkohol trägt das C-Atom mit der –OH-Gruppe nur einen weiteren C-Substituenten (z. B. Ethanol). Beim sekundären Alkohol sind es zwei, beim tertiären drei C-Substituenten. Diese Unterscheidung ist wichtig für die Oxidierbarkeit: Primäre und sekundäre Alkohole können zu Aldehyden bzw. Ketonen oxidiert werden; tertiäre Alkohole sind unter normalen Bedingungen nicht oxidierbar. → Mehr dazu
Wie läuft die radikalische Substitution bei Alkanen ab?
Die radikalische Substitution verläuft in drei Schritten: Startreaktion (Homolytische Spaltung der Cl–Cl-Bindung durch UV-Licht → 2 Cl•), Kettenreaktion (Cl• + CH₄ → CH₃• + HCl; CH₃• + Cl₂ → CH₃Cl + Cl•) und Abbruchreaktion (zwei Radikale verbinden sich). Das Verhältnis der Produkte hängt von den Reaktionsbedingungen ab. → Radikalische Substitution
Lernkarten – Organische Chemie Klasse 10
Klicke auf eine Karte, um die Antwort zu sehen.
1Was ist ein Alkan? Gib die allgemeine Summenformel an.
Kohlenwasserstoff mit ausschließlich Einfachbindungen (gesättigt).
Allg. Formel: CₙH₂ₙ₊₂
Beispiele: Methan CH₄, Ethan C₂H₆, Propan C₃H₈2Welche funktionellen Gruppen kennzeichnen Aldehyde und Ketone? Worin unterscheiden sie sich?
Beide besitzen die Carbonylgruppe C=O.
Aldehyd: C=O am Kettenende (R–CHO)
Keton: C=O in der Kette (R–CO–R')
→ Aldehyde sind oxidierbar, Ketone nicht.3Warum haben Alkohole höhere Siedepunkte als Alkane gleicher Kettenlänge?
Die –OH-Gruppe ermöglicht die Ausbildung von
Wasserstoffbrückenbindungen zwischen den Molekülen.
Diese sind stärker als die Van-der-Waals-Kräfte der Alkane
→ höhere Siedetemperatur4Was ist eine elektrophile Addition? An welchem Bindungstyp läuft sie ab?
Addition an die C=C-Doppelbindung (Alkene).
Ein Elektrophil (e−-armes Teilchen) greift die π-Elektronen an.
Beispiel: Ethen + HBr → Bromoethan
(Markownikow-Regel bei unsymmetrischen Alkenen)5Gib Summenformeln und funktionelle Gruppen für Ethanol, Ethanal und Ethansäure an.
Ethanol: C₂H₆O · –OH (Hydroxylgruppe)
Ethanal: C₂H₄O · –CHO (Aldehydgruppe)
Ethansäure: C₂H₄O₂ · –COOH (Carboxylgruppe)
Oxidationsreihe: Alkohol → Aldehyd → CarbonsäureWeiter auf w-hoelzel.de
← Chemie – 9. Klasse → Chemie – Kursstufe
📚 Verwandte Kursstufen-Themen: Cycloalkane & Aromaten · Gleichgewichtsreaktionen (Estergleichgewicht) · Naturstoffe I (Kohlenhydrate, Ester) · Naturstoffe II (Aminosäuren, Enzyme)
-
2.1.6 Isomerien von Alkenen
2.1.6 Isomerien bei Ethenderivaten
Von Dichlorethen gibt es drei isomere Verbindungen:
2.1.7 cis-trans-Isomerie (bzw. E/Z-Isomerie
Die Doppelbindung blockiert die Drehbarkeit um die C-C-Bindungsachse. Die cis-trans-isomeren Verbindungen unterscheiden sich in ihrem physikalischen (und chemischen) Verhalten.


Dipol
- stärkere zwischenmolekulare Wechselwirkungenhöhere
- Siedetemperatur: 60,3 °C
kein Dipol (symmetrisch)
- schwächere zwischenmolekulare wechselwirkungenniedrigere
- Siedetemperatur: 47,7 °C
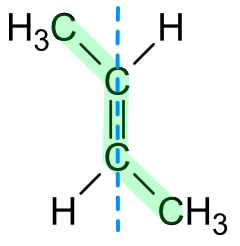
a) trans (lat) = hinüberschreiten, jenseits heute als (E)-IsomerieDie wichtigen Substituenten (Alkylgruppen, Halogen-Atome, Hydroxylgruppe,...) liegen auf der gegenüberliegenden Seite der Doppelbindung.
Heutzutage bezeichnet man es auch als (E)-Isomere, wobei (E) für entgegen gemerkt werden kann.Beispiel: trans-But-2-en (= trans-2-Buten) = (E)-But-2-en.
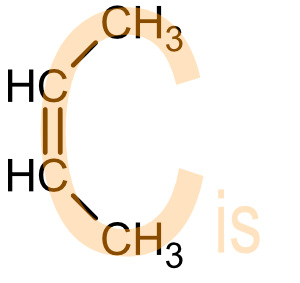
c) cis (lat) = diesseits heute auch als (Z)-Isomere
Die wichtigen Substituenten liegen auf der gleichen Seite der Doppelbindung.
Heute auch als (Z)-Isomere von zusammen.Beispiel: cis-But-2-en (=cis-2-Buten) = (Z)-But-2-en
Eselbrücke: cis: Ein cis-Molekül hat die Form wie ein "C" von "cis".
-
2.2 Nomenklatur der Alkene
2.2 Nomenklatur der Alkene
Da die Nomenklatur der Alkene ähnlich zur Nomenklatur der Alkane ist, soll dieses Thema gleich als Übung besprochen werden. Schüler des Limes-Gymnasium Welzheims: siehe AB!
a) Nenne die homologe Reihe der Alkene bis Decen.
{slider title="Lösung - Homologe Reihe" open="false" class="icon"}
Hinweis: Methen kann es nicht geben; wie sollte bei einem C auch eine C=C-Doppelbindung entstehen. ;-)
Ethen - Propen - Buten - Penten - Hexen - Hepten - Octen - Nonen - Decen{/sliders}
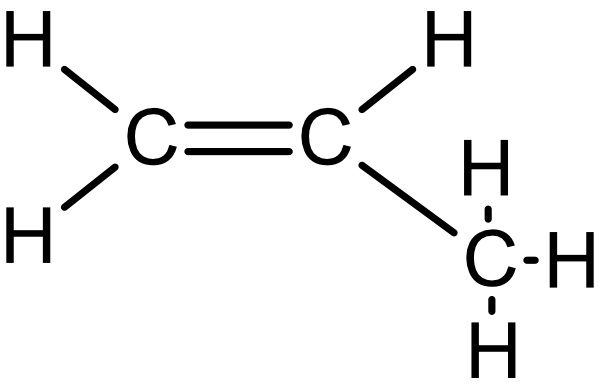
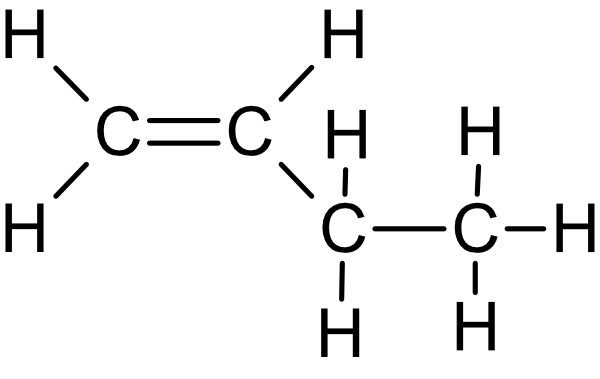
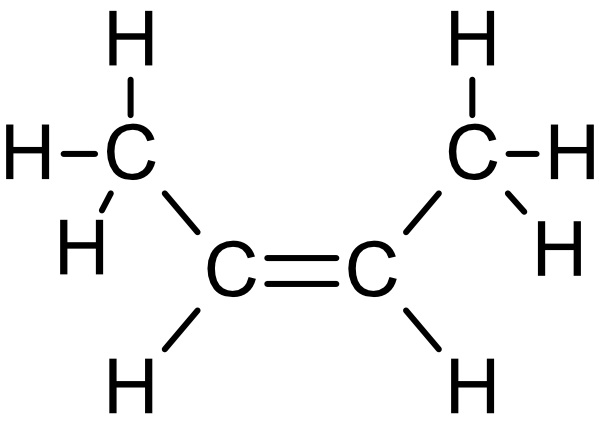
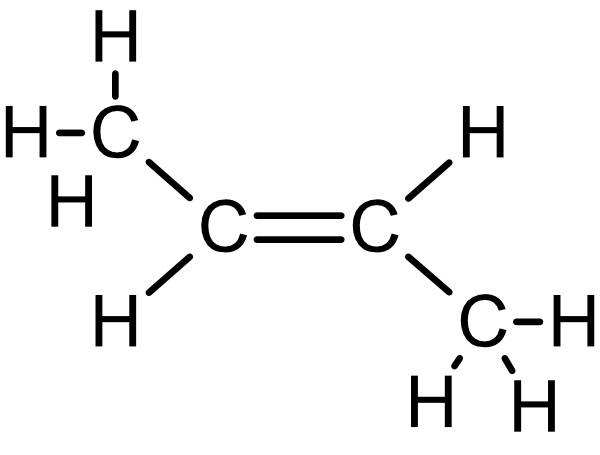
b) Zeichne die Strukturformeln von Propen, 1-Buten, cis-2-Buten, trans-2-Buten und 1,3-Butadien.
{slider title="Lösung" open="false" class="icon"}
Propen:
1-Buten:
cis-2-Buten:
trans-2-Buten:
1,3 Butadien:
{/sliders}
c) Gib die Molekülformel von Propen an.
{slider title="Lösung - Molekülformel von Propen" open="false" class="icon"}
C₃H₆
{/sliders}
d) Benenne die folgende Verbindungen.
I:
II:
{slider title="Lösung" open="false" class="icon"}
I.: Penta-1,3-dien
II. cis-Pent-2-en
{/sliders}
e) Zeichne die Strukturformeln der isomeren Pentene und benenne die Verbindungen.
{slider title="Lösung - Pentene" open="false" class="icon"}
Pent-1-en:
cis-Pent-2-en:
trans-Pent-2-en:
3-Methylbut-1-en:
2-Methylbut-2-en:
2.Methylbut-1-en:
{/sliders}
-
2.4 Vergleich: Ethen – Ethan
2.4 Vergleich: Ethen – Ethan
Aufgabe: vervollständige die Tabelle
Ethan Ethen Strukturformel Bindungswinkel 109,5 °
(= "_________________")
______° C-C-Bindungsabstand 154 pm 135 pm C-Bindungsenergie 348 kJ/mol 614 kJ/mol bevorzugter Reaktionstyp {slider title="Lösung" open="false" class="icon"}
{/sliders}