Atombau/Hundsche Regel
-
2.5 Das Kugelwolkenmodell, KWM
Was du auf dieser Seite lernst
Das Kugelwolkenmodell (KWM) ist eine Weiterentwicklung des Bohr-Modells: Statt fester Elektronenbahnen gibt es nur noch Wahrscheinlichkeitsbereiche – sogenannte Kugelwolken. Du lernst, wie diese dargestellt werden, was das Pauli-Prinzip und die Regel von Hund besagen, und wie das KWM für die ersten 10 Elemente aussieht.
Grundlagen aus der 9. Klasse
Das KWM baut direkt auf dem Bohr-Schalenmodell auf: → 2.4 Bohr-Schalenmodell · → 2.3 Rutherford-Kern-Hülle-Modell
Das Kugelwolkenmodell – eine Weiterentwicklung des Bohr-Modells
Das Bohrsche Atommodell kann schon viel erklären; allerdings gibt es ein weiteres Atommodell, in dem die Elektronen in bestimmten gedachten Aufenthaltswahrscheinlichkeitsräumen betrachtet werden. Das sind keine echten Räume, sondern Bereiche, in denen sich mit hoher Wahrscheinlichkeit gerade ein Elektron – maximal zwei – aufhält. Es könnte sich auch gerade außerhalb dieses Bereichs bewegen, allerdings mit geringerer Wahrscheinlichkeit.
So einfach, wie Niels Bohr sich das vorgestellt hatte, war es allerdings nicht mit der Verteilung der Elektronen innerhalb einer Schale. Es gibt bestimmte Bereiche, in denen sich die Elektronen mit größerer Wahrscheinlichkeit aufhalten – sogenannte Kugelwolken.
🖱️ Interaktives Diagramm → Klicke auf einen Bereich für eine Erläuterung · Mobilgerät: TippenVergleich: Schalenmodell vs. Kugelwolkenmodell am Beispiel Sauerstoff (Z = 8)
Kugelwolke einfach besetzt (1 Elektron) Kugelwolke doppelt besetzt (2 Elektronen) Elektron🔴 Atomkern (Schalenmodell) Der Kern des Sauerstoffs trägt die Ladung 8+ (8 Protonen). Im Schalenmodell nach Bohr umkreisen die Elektronen den Kern auf festen Bahnen – wie Planeten die Sonne. Im Kugelwolkenmodell bleibt der Kern unverändert, aber die Elektronen befinden sich nicht mehr auf Bahnen, sondern in Wahrscheinlichkeitsbereichen.⚪ K-Schale (Schalenmodell) Die K-Schale ist die innerste Elektronenschale. Beim Sauerstoff enthält sie 2 Elektronen. Im Kugelwolkenmodell entspricht ihr eine einzige rote Kugelwolke direkt am Kern (doppelt besetzt). Die K-Schale fasst maximal 2 Elektronen (→ Pauli-Prinzip).⚪ L-Schale (Schalenmodell) Die L-Schale ist die zweite Elektronenschale. Beim Sauerstoff enthält sie 6 Elektronen, gleichmäßig auf der Kreisbahn verteilt. Im Kugelwolkenmodell werden diese 6 Elektronen auf 4 Kugelwolken verteilt: 2 doppelt besetzte (rot) und 2 einfach besetzte (grün).🔴 Atomkern (Kugelwolkenmodell) Auch im Kugelwolkenmodell bleibt der Atomkern mit der Ladung 8+ unveränderter Mittelpunkt. Die Kugelwolken sind um ihn herum angeordnet. Je näher eine Kugelwolke am Kern liegt, desto energieärmer ist sie (K-Schale < L-Schale).● Kugelwolke der K-Schale (doppelt besetzt) Die Kugelwolke der K-Schale liegt direkt am Kern und ist rot = doppelt besetzt – sie enthält beide K-Elektronen (2e). In der K-Schale gibt es nur eine einzige Kugelwolke. Maximal 2 Elektronen passen hinein (→ Pauli-Prinzip).● Kugelwolke der L-Schale – einfach besetzt Grüne Kugelwolken sind einfach besetzt – sie enthalten genau 1 Elektron. Beim Sauerstoff gibt es in der L-Schale 2 einfach besetzte Kugelwolken. Dies folgt aus der Regel von Hund: Energiegleiche Kugelwolken werden zuerst einzeln besetzt.● Kugelwolke der L-Schale – doppelt besetzt Rote Kugelwolken sind doppelt besetzt – sie enthalten 2 Elektronen. Beim Sauerstoff gibt es in der L-Schale 2 doppelt besetzte Kugelwolken. Die Doppelbesetzung tritt erst auf, wenn alle energiegleichen Kugelwolken mindestens 1 Elektron haben (→ Regel von Hund).💡 Nochmals klicken schließt die Erläuterung.
Das Kugelwolkenmodell ähnelt einem Tetraeder
Das Kugelwolkenmodell ist ein stark vereinfachtes Orbitalmodell. Da die Elektronen sich in bestimmten Bereichen aufhalten, den sogenannten Orbitalen, sind diese negativ geladen und stoßen sich somit ab. Um den größtmöglichen Abstand zu erhalten, ergeben diese vier Kugelwolken eine Art Tetraeder. Das soll die folgende Animation eines Sauerstoffmodells zeigen.
Vereinfachte Darstellung der Kugelwolken
Da die räumliche Anordnung der Kugelwolken (Tetraeder-Struktur, 109,47°-Winkel) schwer darstellbar ist, wird im Unterricht eine vereinfachte, ebene Darstellung verwendet. Die Abbildung unten zeigt links die räumliche Ansicht und rechts die vereinfachte Darstellung. Beachte: Die räumliche Anordnung der Orbitale sieht in Wirklichkeit anders aus als die ebene Vereinfachung.
🖱️ Interaktives Diagramm – Vereinfachte Darstellung → Klicke auf eine Kugelwolke für eine ErläuterungSauerstoff (Z = 8): räumliche Darstellung (links) und vereinfachte Darstellung (rechts)
einfach besetztes Orbital (1 Elektron) doppelt besetztes Orbital (2 Elektronen) Elektron🔴 Atomkern (räumliche Darstellung) Der Kern des Sauerstoffs trägt die Ladung 8+. In der räumlichen Darstellung ist gut zu sehen, wie die vier L-Kugelwolken den Kern tetraedrisch umgeben – der Winkel zwischen je zwei Kugelwolken beträgt 109,47° (Tetraeder-Winkel). Dieser maximale Abstand entsteht, weil sich die negativ geladenen Kugelwolken gegenseitig abstoßen.● K-Schalen-Kugelwolke (räumlich, doppelt besetzt) Die kleine rote Kugelwolke direkt am Kern gehört zur K-Schale (1s²). Sie ist doppelt besetzt (2 Elektronen) und liegt energetisch am tiefsten. In der räumlichen Darstellung ist gut zu sehen, wie sie sich vom Kern kaum abhebt – sie ist sehr klein im Vergleich zu den L-Kugelwolken.● Einfach besetztes Orbital (räumlich, 1 Elektron) Grüne Kugelwolken enthalten jeweils 1 Elektron. Beim Sauerstoff gibt es zwei einfach besetzte Kugelwolken in der L-Schale. In der räumlichen Darstellung sieht man ihre tetraedrische Anordnung: Sie stehen im größtmöglichen Winkelabstand zu allen anderen Kugelwolken.● Doppelt besetztes Orbital (räumlich, 2 Elektronen) Rote Kugelwolken enthalten jeweils 2 Elektronen. Beim Sauerstoff gibt es zwei doppelt besetzte Kugelwolken in der L-Schale (2s² und 2px²). In der räumlichen Ansicht sind sie gut von den grünen einfach besetzten Kugelwolken zu unterscheiden.🔴 Atomkern (vereinfachte Darstellung) In der vereinfachten Darstellung liegt der Kern 8+ in der Mitte. Die vier L-Kugelwolken sind hier in einer ebenen Anordnung (oben, unten, links, rechts) dargestellt – in Wirklichkeit sind sie tetraedrisch (räumlich) angeordnet. Die vereinfachte Darstellung erleichtert das Zeichnen im Unterricht.● K-Schalen-Kugelwolke (vereinfacht, doppelt besetzt) Die kleine rote Kugelwolke um den Kern gehört zur K-Schale. Sie ist doppelt besetzt (2 Elektronen, 1s²). In der vereinfachten Darstellung wird sie als kleiner Kreis direkt am Kern gezeigt – wie in der räumlichen Darstellung auch.● Einfach besetztes Orbital (vereinfacht, 1 Elektron) Grüne Kugelwolken = einfach besetzt (1 Elektron). In der vereinfachten Darstellung sind sie oben und links gezeichnet. Achtung: Diese ebene Anordnung ist eine Vereinfachung – räumlich stehen alle vier L-Kugelwolken im Tetraeder-Winkel (109,47°) zueinander!● Doppelt besetztes Orbital (vereinfacht, 2 Elektronen) Rote Kugelwolken = doppelt besetzt (2 Elektronen). In der vereinfachten Darstellung sind sie unten und rechts gezeichnet. Diese Anordnung zeigt die Besetzungsunterschiede (grün vs. rot) auf einen Blick – auch wenn die räumliche Realität eine tetraedrische Anordnung ist.💡 Nochmals klicken schließt die Erläuterung.
2.5.1 Feinstruktur der Elektronenhülle
Im Kugelwolkenmodell gelten drei grundlegende Prinzipien, die erklären, wie Elektronen auf die Kugelwolken verteilt werden:
1. Heisenbergsche Unschärferelation (1927)
Es ist nicht möglich, gleichzeitig den Ort, die Geschwindigkeit und die Bewegungsrichtung eines Elektrons anzugeben. Daher lassen sich für Elektronen der Atomhülle keine festen Bahnen, sondern nur Aufenthaltsbereiche angeben.
2. Pauli-Prinzip
In einer „Kugelwolke" können sich maximal 2 Elektronen aufhalten, die sich in einer bestimmten Eigenschaft (Spin) voneinander unterscheiden.
3. Regel von Hund
Energiegleiche Kugelwolken werden zunächst einzeln mit Elektronen besetzt, bevor eine Doppelbesetzung erfolgt.
Das Kugelwolkenmodell ist ein vereinfachtes Orbitalmodell und gilt nur für Hauptgruppenelemente.
🖱️ Interaktiv – Pauli-Prinzip → Finde den Fehler im rechten Modell und klicke darauf🔍 Aufgabe: Das rechte Modell zeigt eine Verletzung des Pauli-Prinzips. Finde das falsche Orbital und klicke darauf! (Tipp: Eines der Orbitale hat zu viele Elektronen.)✅ Dieses Orbital ist korrekt besetzt Dieses Orbital enthält maximal 2 Elektronen – das entspricht dem Pauli-Prinzip. Suche weiter: Das falsche Orbital befindet sich im rechten Modell (falsch, nach Pauli-Prinzip).✅ Dieses Orbital ist korrekt besetzt Auch dieses Orbital im rechten Modell ist korrekt (max. 2 Elektronen). Der Fehler liegt woanders – schau dir alle Orbitale des rechten Modells genau an!🎉 Du hast den Fehler gefunden! Dieses Orbital enthält 3 Elektronen – das ist nach dem Pauli-Prinzip unmöglich!
Pauli-Prinzip: In einer Kugelwolke (= Orbital) können sich maximal 2 Elektronen aufhalten. Diese müssen sich außerdem in ihrer Quanteneigenschaft (dem Spin) voneinander unterscheiden (+½ und −½). Ein drittes Elektron wird vom Orbital „abgewiesen" – es muss in ein anderes Orbital wechseln.💡 Klicke nochmals auf ein Orbital, um die Erläuterung zu schließen.
🖱️ Interaktiv – Hundsche Regel → Finde den Fehler im rechten Modell und klicke darauf🔍 Aufgabe: Das rechte Modell zeigt eine Verletzung der Regel von Hund. Finde das falsch besetzte Orbital und klicke darauf! (Tipp: Energiegleiche Orbitale sollten zuerst einzeln besetzt werden.)✅ Dieses Orbital ist korrekt besetzt – Regel von Hund eingehalten Im linken Modell sind die Orbitale korrekt nach der Regel von Hund besetzt: Energiegleiche Orbitale werden zunächst einzeln mit Elektronen besetzt, bevor eine Doppelbesetzung stattfindet. Das Suchergebnis liegt im rechten Modell – klicke dort auf ein Orbital!🎉 Du hast den Fehler gefunden! Im rechten Modell sind alle Orbitale doppelt besetzt (rot) – obwohl noch ein viertes Orbital leer wäre. Das verstößt gegen die Regel von Hund!
Regel von Hund: Energiegleiche Orbitale (z. B. die drei 2p-Orbitale der L-Schale) werden zunächst einzeln mit einem Elektron besetzt, bevor ein zweites Elektron hinzukommt. Grund: Zwei Elektronen im selben Orbital stoßen sich durch ihre negative Ladung stärker ab – es ist energetisch günstiger, wenn sie verschiedene Orbitale besetzen.💡 Klicke nochmals, um die Erläuterung zu schließen.
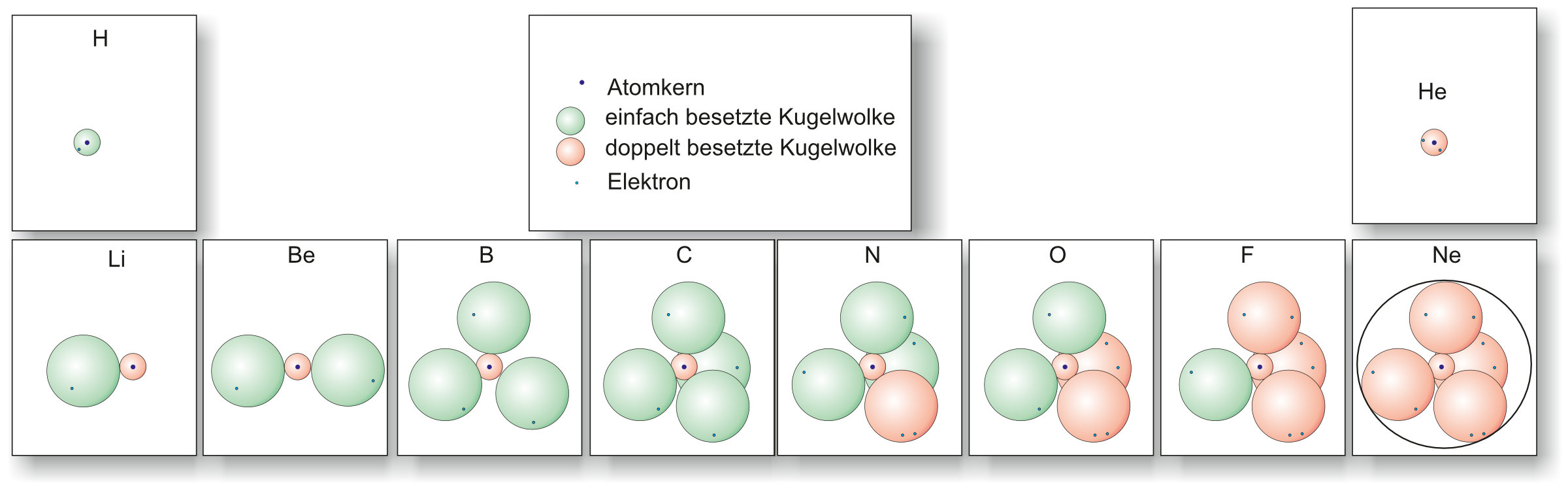
Das KWM der ersten 10 Elemente
Durch Pauli-Prinzip und Regel von Hund ergeben sich folgende Kugelwolkenmodelle für die ersten 10 Elemente. Grün = einfach besetzt · Rot = doppelt besetzt:
↑ Zum Vergrößern klicken
Auf einen Blick – die wichtigsten Aussagen
Kugelwolke
Eine Kugelwolke ist ein Bereich, in dem sich ein Elektron mit ~90 % Wahrscheinlichkeit aufhält. Kein fester Körper – nur ein Wahrscheinlichkeitsbereich.
Pauli-Prinzip
Max. 2 Elektronen pro Kugelwolke, mit entgegengesetztem Spin. Ein drittes Elektron ist ausgeschlossen.
Regel von Hund
Energiegleiche Kugelwolken erst einzeln besetzen, dann doppelt. Gilt für alle Kugelwolken einer Schale.
Farb-Code
Grün = 1 Elektron (einfach besetzt). Rot = 2 Elektronen (doppelt besetzt). Gilt für alle KWM-Darstellungen.
Häufige Fragen – Kugelwolkenmodell
Was ist der Unterschied zwischen dem Bohr-Modell und dem Kugelwolkenmodell?
Im Bohr-Modell bewegen sich Elektronen auf festen Kreisbahnen (Schalen). Das Kugelwolkenmodell ersetzt diese durch Wahrscheinlichkeitsbereiche: Man kann nur angeben, in welchem Bereich sich ein Elektron mit ca. 90 % Wahrscheinlichkeit aufhält – nicht wo es sich genau befindet. → 2.4 Bohr-Schalenmodell
Was ist eine Kugelwolke?
Eine Kugelwolke ist der kugelförmige Bereich, in dem sich ein Elektron mit einer Wahrscheinlichkeit von ca. 90 % aufhält. Wichtig: Kugelwolken sind keine festen Körper, sondern nur Wahrscheinlichkeitsbereiche! In der Kursstufe werden Kugelwolken auch als Orbitale bezeichnet und nach Typ (s, p, d) unterschieden.
Was besagt das Pauli-Prinzip?
Das Pauli-Prinzip (Wolfgang Pauli, 1925): In einer Kugelwolke können sich maximal 2 Elektronen aufhalten, die sich in ihrem Spin (+½ und −½) unterscheiden müssen. Merkhilfe: Die Kugelwolke ist wie ein Zimmer mit 2 Plätzen – beide Bewohner müssen verschieden sein.
Was besagt die Regel von Hund?
Die Regel von Hund (Friedrich Hund, 1925): Energiegleiche Kugelwolken einer Schale werden zunächst einzeln besetzt, bevor eine Doppelbesetzung stattfindet. Grund: Zwei Elektronen in derselben Kugelwolke stoßen sich stärker ab. Merkhilfe: Wie in einem Bus – erst wenn jede Doppelbank einen Fahrgast hat, setzt sich jemand dazu.
Für welche Elemente gilt das Kugelwolkenmodell?
Das vereinfachte Kugelwolkenmodell gilt für Hauptgruppenelemente. Für H bis Ne (Perioden 1 und 2) ist die Darstellung vollständig. Ab der dritten Periode kommen weitere Kugelwolkentypen hinzu. Bei Nebengruppenmetallen reicht das vereinfachte Modell nicht mehr aus. → 2.6 PSE und Atommodelle
Lernkarten – Kugelwolkenmodell
Klicke auf eine Karte, um die Antwort zu sehen.
1Was ist eine Kugelwolke und wie unterscheidet sie sich von einer Elektronenbahn?
Kugelwolke = Wahrscheinlichkeitsbereich (~90 %), kein fester Weg. Bohr: Kreisbahn → KWM: kugelförmige Zone.
2Formuliere das Pauli-Prinzip in einem Satz.
In einer Kugelwolke können sich maximal 2 Elektronen aufhalten – sie unterscheiden sich im Spin.
3Formuliere die Regel von Hund mit einem Beispiel.
Energiegleiche Kugelwolken werden erst einzeln besetzt. Beispiel: N (Z=7) → alle drei L-Kugelwolken je 1e (2px¹ 2py¹ 2pz¹).
4Was bedeuten die Farben Grün und Rot in KWM-Darstellungen?
Grün = 1e (einfach besetzt) · Rot = 2e (doppelt besetzt).
5Wie viele Kugelwolken hat die K-Schale, wie viele die L-Schale?
K-Schale: 1 Kugelwolke (max. 2e). L-Schale: 4 Kugelwolken (max. 8e). Die 3 äußeren L-Kugelwolken sind energiegleich.
Weiter im Kapitel: Atombau und PSE
← 2.4 Bohr-Schalenmodell → 2.6 PSE und Atommodelle → 2.7 Lewis-Formeln
🔁 Grundlagen: Rutherford-Modell · Bohr-Schalenmodell · Periodensystem (PSE)