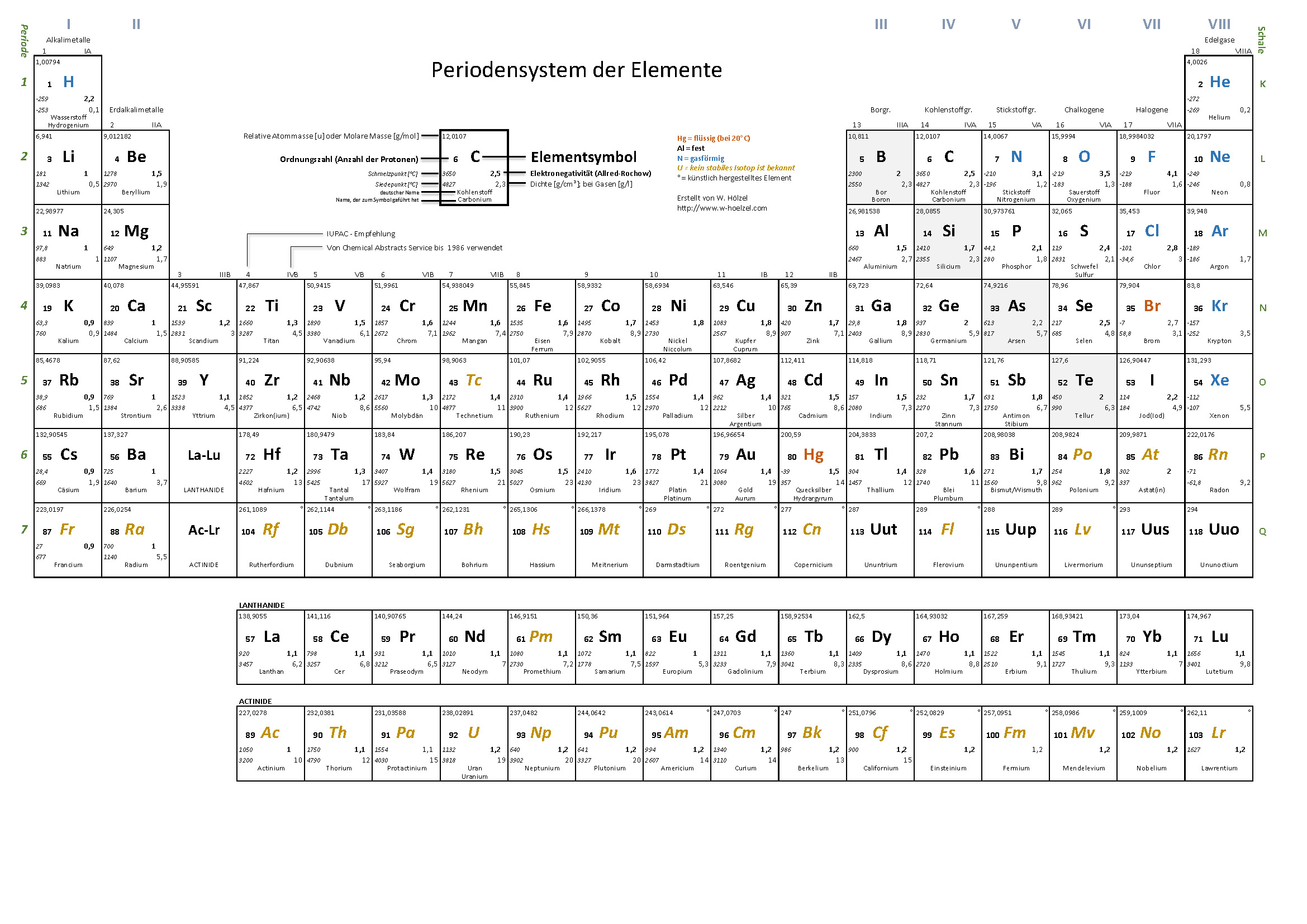
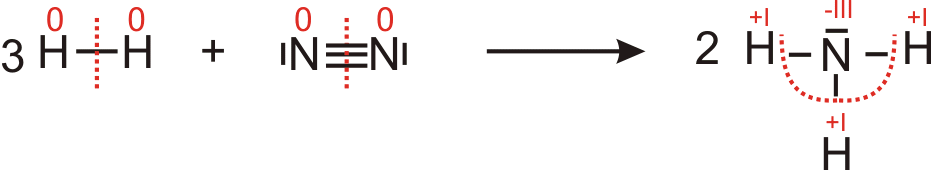Periodensystem der Elemente
-
2.6 Das Periodensystem der Elemente (PSE) und die Atommodelle
Was du auf dieser Seite lernst
Das Periodensystem der Elemente (PSE) ordnet alle bekannten Elemente nach ihrer Ordnungszahl und gibt dir auf einen Blick Auskunft über Atommasse, Elektronenkonfiguration, Schalen und Valenzelektronen. Du lernst, wie das PSE aufgebaut ist, was Gruppen und Perioden bedeuten und wie du Valenzelektronen ablesen kannst.
Grundlagen aus der 9. Klasse
Um das PSE zu verstehen, solltest du Protonen, Elektronen und Neutronen sowie Elektronenschalen kennen: → 2.3 Rutherford-Modell · → 2.4 Bohr-Schalenmodell · → 2.5 Kugelwolkenmodell
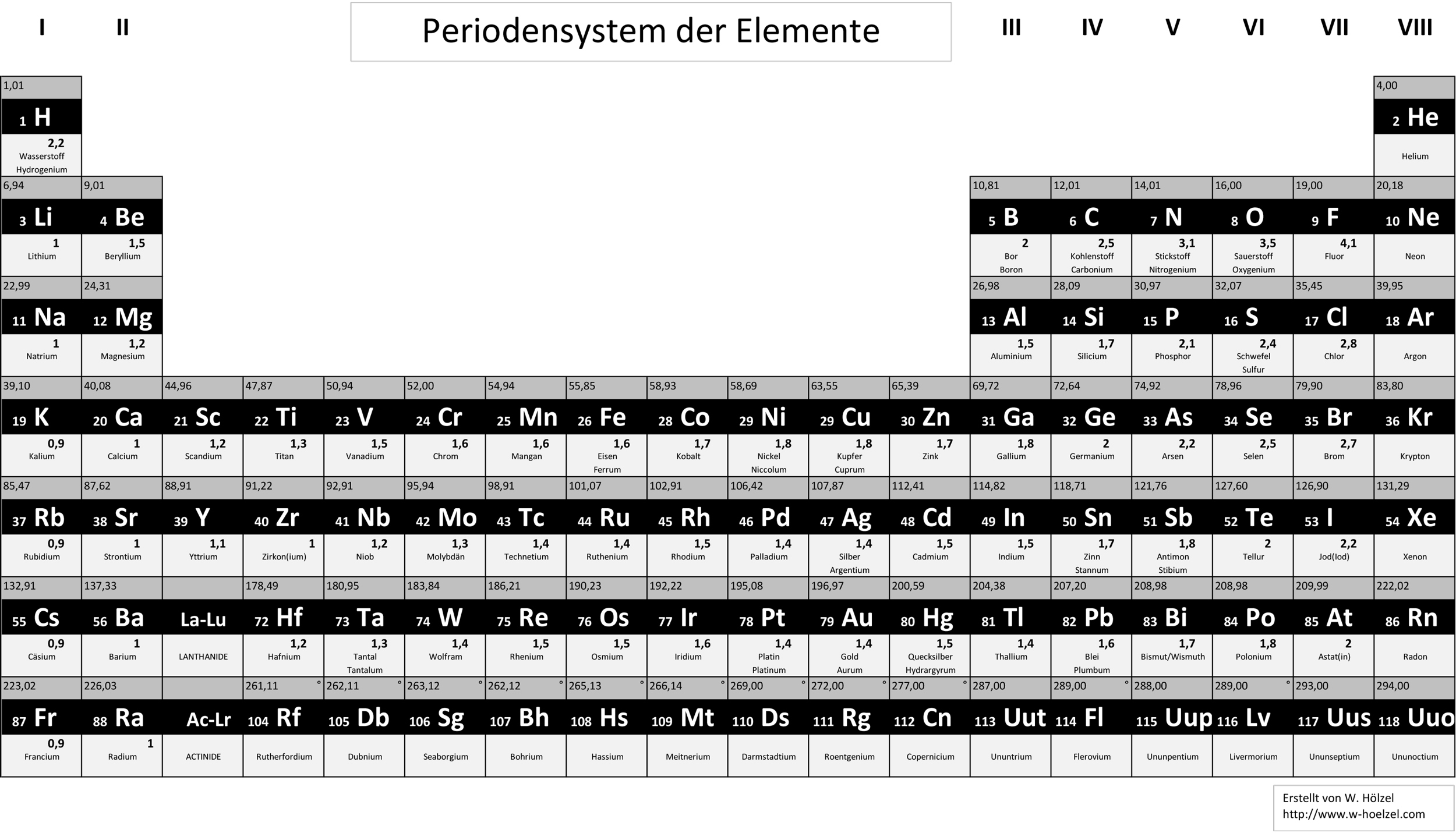
Das Periodensystem der Elemente (PSE)
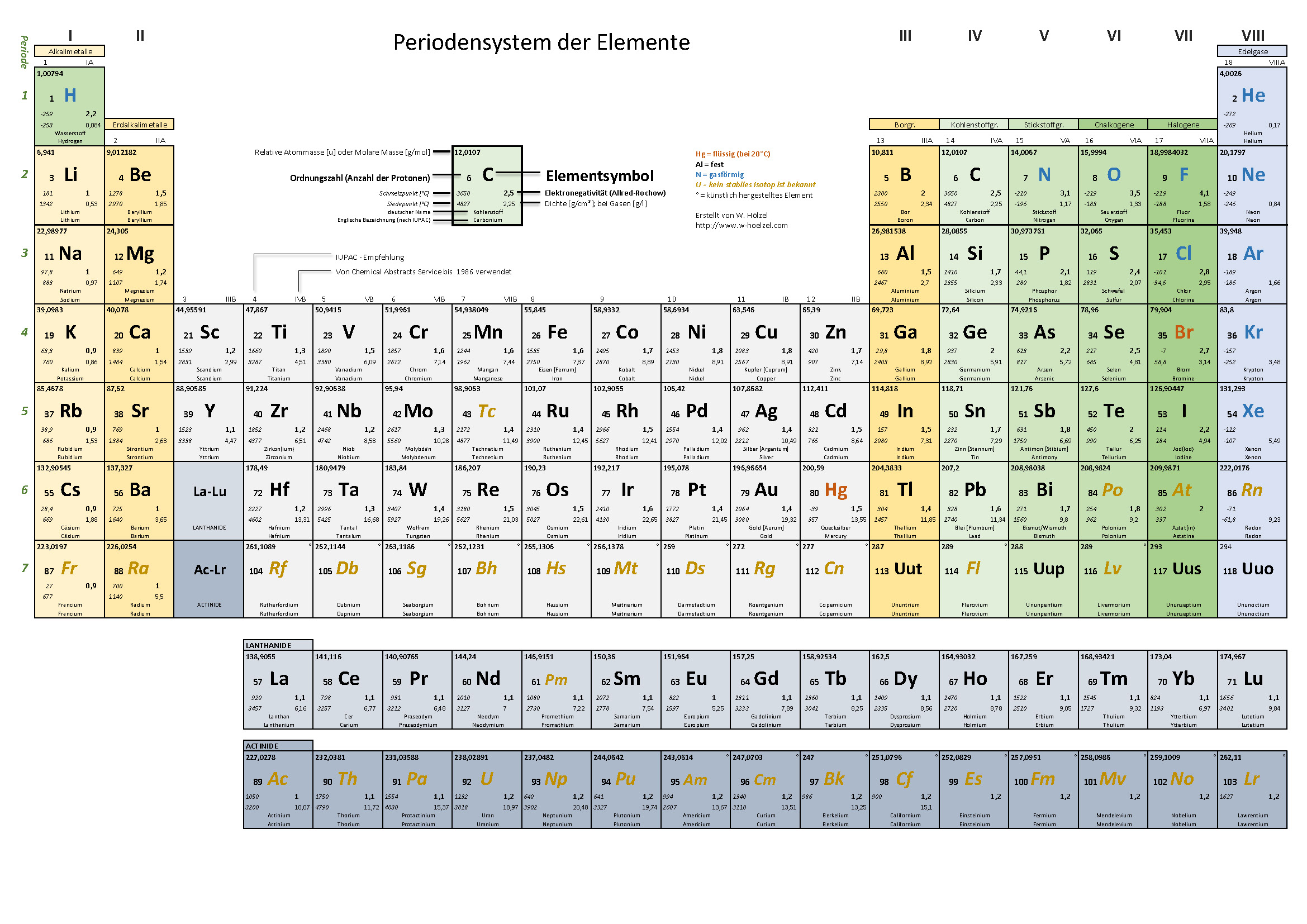
Periodensystem – Nur Hauptgruppenelemente
↑ Zum Vergrößern klicken · Farben: Alkalimetalle Erdalkalimetalle Metalloide Nichtmetalle Halogene Edelgase
Das Periodensystem der Elemente ist eine große Hilfe, um Voraussagen bezüglich chemischer Reaktionen zu treffen und Eigenschaften zu benennen. Man muss es nicht auswendig lernen – wichtig ist, es lesen zu können.
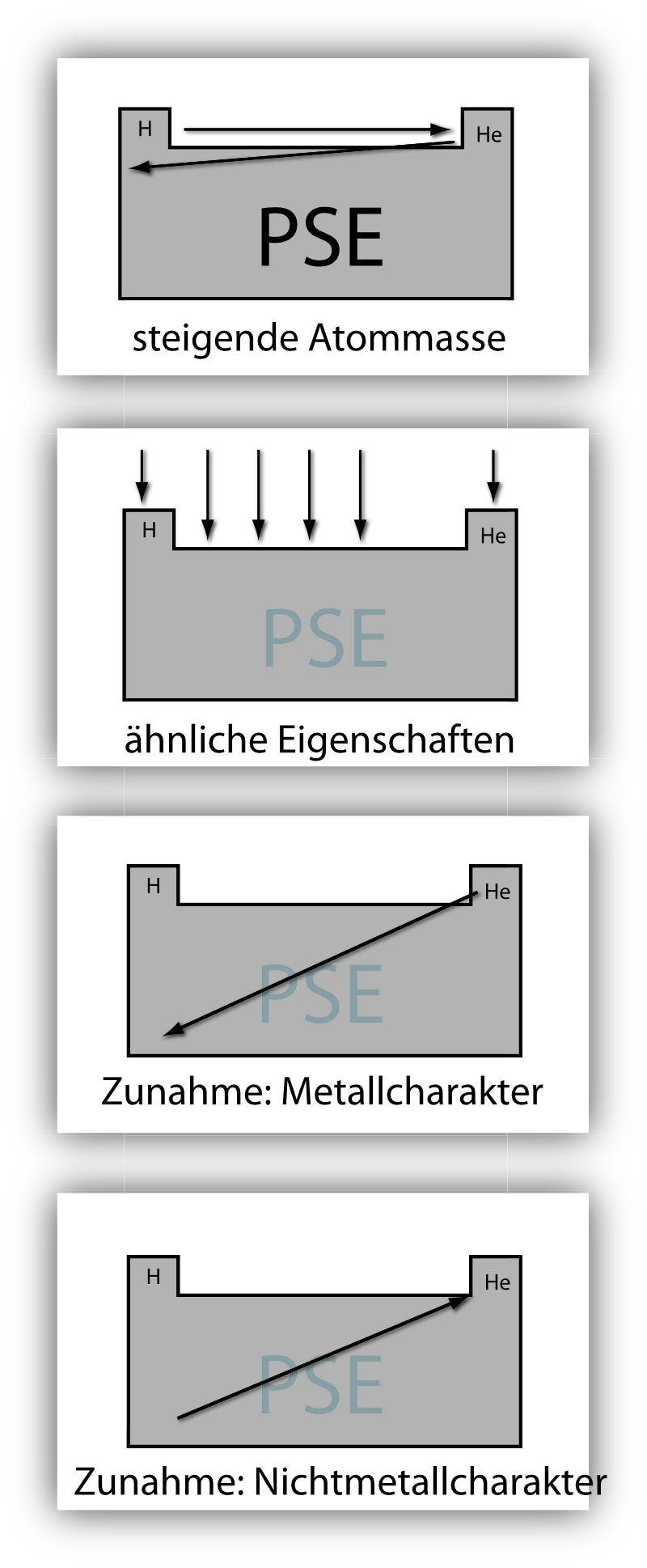
Ursprünglich wurden die Elemente nach steigender Atommasse geordnet. Heute erfolgt die Anordnung nach der Ordnungszahl (= Kernladungszahl = Anzahl der Protonen) und nach periodisch wiederkehrenden Ähnlichkeiten in den Eigenschaften.
Ordnungsprinzipien
- Reihenfolge: Die Elemente sind nach steigender Ordnungszahl (Anzahl der Protonen = Anzahl der Elektronen) angeordnet.
- Periode (= Zeile): Die Periodennummer gibt die Anzahl der Elektronenschalen an.
Beispiel: H, He → 1 Schale · Li…Ne → 2 Schalen · Na…Ar → 3 Schalen - Gruppe (= Spalte): Elemente mit gleicher Anzahl an Außenelektronen (Valenzelektronen) stehen in einer Gruppe.
↑ PSE-Symbol-Erklärung – zum Vergrößern klicken
Bedeutung des PSE
- Voraussage damals unbekannter Elemente (z. B. Germanium – von Mendeleev 1871 vorausgesagt, 1886 entdeckt).
- Ablesen von physikalischen und chemischen Eigenschaften aus der Stellung im PSE.
- Das Kurzperiodensystem enthält nur die Hauptgruppenelemente.
Was bedeuten die Felder eines PSE-Eintrags?
Klicke auf ein farbiges Feld der Elementbox, um zu erfahren, was es bedeutet. Beispiel: Aluminium (Al, Z = 13)
26,981538[Ne]3s²3p¹13 Al6611,5 24676,0Aluminium← Klicke auf ein Feld der Elementbox
🟠 Relative Atommasse (oben) Die relative Atommasse (in u, früher: atomare Masseneinheit) gibt an, wie schwer ein Atom im Verhältnis zu 1/12 des Kohlenstoff-12-Atoms ist. Bei Aluminium: 26,98 u. Sie ist kein ganzzahliger Wert, weil verschiedene Isotope des Elements in der Natur vorkommen und gemittelt werden.⬜ Elektronenkonfiguration Die Elektronenkonfiguration [Ne]3s²3p¹ zeigt, auf welchen Orbitalen die Elektronen des Atoms verteilt sind. [Ne] bedeutet: die Konfiguration des Edelgases Neon ist bereits vollständig besetzt. Dann kommen noch 3s² (2 Elektronen im s-Orbital der 3. Schale) und 3p¹ (1 Elektron im p-Orbital). Das ist Kursstufen-Wissen – in Klasse 9 reicht die Schalen-Angabe.🟢 Elementsymbol und Ordnungszahl Das Elementsymbol (hier: Al) besteht aus 1–2 Buchstaben: 1. Buchstabe immer großgeschrieben, 2. Buchstabe immer klein. Die kleine Zahl links oben (hier: 13) ist die Ordnungszahl (= Kernladungszahl = Anzahl der Protonen = Anzahl der Elektronen im neutralen Atom).🔵 Schmelz-/Siedepunkt und weitere Daten Die vier Zahlen im mittleren Bereich geben (je nach PSE) an:
661 = Schmelzpunkt in °C · 2467 = Siedepunkt in °C
1,5 = Elektronegativität (EN) nach Pauling · 6,0 = weitere Eigenschaft (EN-Skala oder Ionisierungsenergie – je nach PSE-Version). Diese Werte sind für Klasse 9 noch weniger wichtig.🔵 Elementname Der vollständige Name des Elements (hier: Aluminium). Im PSE steht er meist unten. Die Valenzelektronen (Außenelektronen) kannst du aus der Hauptgruppe ablesen: Aluminium steht in der 3. Hauptgruppe → hat 3 Valenzelektronen.Elementarteilchen aus dem PSE ablesen
Mit Hilfe des PSE können wir sehr schnell die Anzahl der einzelnen Elementarteilchen bestimmen. Wichtig ist dabei: Im PSE sind die Elemente immer so notiert, dass sie elektrisch neutral sind.
Beispiel: Natrium 23₁₁Na
Größe Ableitung aus PSE Wert für Na Kernladungszahl (Z) = Ordnungszahl = Anzahl der Protonen = Anzahl der Elektronen 11 Nukleonenzahl (A) = Anzahl der Protonen + Anzahl der Neutronen 23 Neutronen = Nukleonenzahl − Kernladungszahl = 23 − 11 12 Merke: Da das Atom elektrisch neutral ist → Anzahl Protonen (11+) = Anzahl Elektronen (11−) → Ladung = 0
⚠️ Die Nukleonenzahl im PSE ist ein gerundeter Wert (relative Atommasse). Für exakte Berechnungen wird der ganzzahlige Wert des häufigsten Isotops verwendet.Übungen: Elementarteilchen aus dem PSE ablesen
Überlege zunächst selbst, dann klappe die Lösung auf.
Afg. 1 Nenne die Anzahl der Elektronen von Kohlenstoff (C).
Lösung: C hat die Ordnungszahl 6 → 6 Elektronen (= 6 Protonen, da elektrisch neutral).Afg. 2 Nenne die Anzahl der Protonen von Brom (Br).
Lösung: Br hat die Ordnungszahl 35 → 35 Protonen.Afg. 3 Nenne die Anzahl der Neutronen von Schwefel (S, Nukleonenzahl 32).
Lösung: S: Ordnungszahl = 16 (Protonen), Nukleonenzahl ≈ 32 → Neutronen = 32 − 16 = 16 Neutronen.Afg. 4 Wie groß ist die Masse von einem Bor-Atom (B)?
Lösung: Die relative Atommasse von B beträgt ca. 10,81 u (aus dem PSE ablesbar).Afg. 5 Nenne das Symbol und die Anzahl der Protonen von Gallium.
Lösung: Symbol: Ga · Ordnungszahl: 31 Protonen.Perioden = Anzahl der Elektronenschalen
Niels Bohr zeigte, dass sich die Elektronen auf unterschiedliche Energieniveaus (= „Schalen") verteilen. Diese Anzahl der Schalen findest du auch im PSE wieder – nämlich in der Angabe der Zeile (= Reihe = Periode).
H, He → Periode 1 → 1 Schale (K-Schale)Li … Ne → Periode 2 → 2 Schalen (K, L)Na … Ar → Periode 3 → 3 Schalen (K, L, M)Rb, Sr … → Periode 5 → 5 Schalen🔑 Merke: Die Periodennummer im PSE = die Anzahl der besetzten Elektronenschalen des Atoms.
Übungen: Perioden und Elektronenschalen
Afg. 1 Nenne alle Elemente, die nur 1 Energieniveau/Schale besitzen.
Lösung: H (Wasserstoff) und He (Helium) – beide stehen in Periode 1 → 1 Schale (K-Schale).Afg. 2 Wie viele „Schalen" besitzt Phosphor (P)?
Lösung: P steht in Periode 3 → 3 Schalen (K, L, M-Schale).Afg. 3 Wie viele Energieniveaus besitzt Xenon (Xe)?
Lösung: Xe steht in Periode 5 → 5 Energieniveaus.Afg. 4 Wie viele Elektronenschalen besitzt Sauerstoff (O)?
Lösung: O steht in Periode 2 → 2 Schalen (K- und L-Schale).Haupt- und Nebengruppenelemente
Im PSE unterscheidet man zwei Typen von Elementen:
Hauptgruppenelemente (grün)
Die Elemente der 1., 2. und 13.–18. Gruppe. Sie unterscheiden sich stärker voneinander. Ihre Anzahl an Valenzelektronen ist direkt aus der Hauptgruppennummer ablesbar. Im Kurzperiodensystem sind nur Hauptgruppenelemente enthalten.
Nebengruppenelemente (grau)
Die Elemente der 3.–12. Gruppe (Übergangsmetalle). Sie besitzen entweder 1 oder 2 Außenelektronen und sind sich chemisch recht ähnlich. Auf den folgenden Seiten werden sie zunächst „weggeschnitten", um mehr Platz zu haben.
Hauptgruppen-Namen: I. HG: Alkalimetalle · II. HG: Erdalkalimetalle · III. HG: Borgruppe · IV. HG: Kohlenstoffgruppe · V. HG: Stickstoffgruppe · VI. HG: Chalkogene (Erzbildner) · VII. HG: Halogene (Salzbildner) · VIII. HG: Edelgase
⚠️ Metallischer vs. nichtmetallischer Charakter: Metallischer Charakter nimmt nach links unten zu · Nichtmetallischer Charakter nimmt nach rechts oben zu · Halbmetalle stehen diagonal dazwischen.
Valenzelektronen und Hauptgruppennummer
Innerhalb einer Hauptgruppe stehen häufig chemisch sich ähnelnde Elemente. Für die chemischen Eigenschaften sind vor allem die Außenelektronen (= Valenzelektronen) verantwortlich.
Die Hauptgruppennummer (gelb unterlegt im PSE) gibt die Anzahl der Valenzelektronen wieder. „Chemie ist die Physik der Valenzelektronen!"
1. HauptgruppeH, Li, Na, K, Rb, Cs, Fr1Valenzelektron2. HauptgruppeBe, Mg, Ca, Sr, Ba, Ra2Valenzelektronen3. HauptgruppeB, Al, Ga, In, Tl3Valenzelektronen7. HauptgruppeF, Cl, Br, I, At7Valenzelektronen8. HauptgruppeHe, Ne, Ar, Kr, Xe, Rn8Valenzelektronen (Edelgase)🔑 Merke: H ist in der 1. HG → 1 Valenzelektron · O ist in der 6. HG (VIA) → 6 Außenelektronen · Edelgase haben 8 Valenzelektronen (He: 2) → besonders stabil (→ Edelgasregel)
Übungen: Valenzelektronen und Hauptgruppenelemente
Für diese Übungen benötigst du das PSE. Bei Klassenarbeiten (und im Abitur) darf es verwendet werden.
Afg. 1 Wie viele Außenelektronen besitzt Rubidium (Rb)?
Lösung: Rb steht in der 1. Hauptgruppe → 1 Außenelektron.Afg. 2 Wie viele Valenzelektronen hat Stickstoff (N)?
Lösung: N steht in der 5. Hauptgruppe (VA) → 5 Valenzelektronen.Afg. 3 Wie viele Valenzelektronen hat Aluminium (Al)?
Lösung: Al steht in der 3. Hauptgruppe → 3 Valenzelektronen.Afg. 4 Wie viele Außenelektronen besitzt die 4. Hauptgruppe?
Lösung: Alle Elemente der 4. HG (C, Si, Ge, Sn, Pb, Fl) haben 4 Außenelektronen.Afg. 5 Wie viele Außenelektronen besitzt Calcium (Ca)?
Lösung: Ca steht in der 2. Hauptgruppe → 2 Außenelektronen.Afg. 6 Wie viele Valenzelektronen hat Chlor (Cl)?
Lösung: Cl steht in der 7. Hauptgruppe (VIIA / Halogene) → 7 Valenzelektronen.Afg. 7 Wie viele Valenzelektronen hat Helium (He)?
Lösung: He ist ein Edelgas (8. HG) – aber eine Ausnahme: es hat nur 2 Valenzelektronen (K-Schale voll mit 2e).Afg. 8 Wie viele Außenelektronen besitzt die 8. Hauptgruppe (Edelgase)?
Lösung: Alle Edelgase (außer He) haben 8 Außenelektronen → vollständig besetzte Außenschale → besonders stabil → kaum Reaktionen.📥 PSE zum Downloaden: Periodensysteme (PSE) herunterladen → (Bei Klassenarbeiten und im Abitur darf das PSE verwendet werden.)
Auf einen Blick – die wichtigsten Aussagen
Ordnungszahl
Die Ordnungszahl = Kernladungszahl = Anzahl der Protonen = Anzahl der Elektronen (neutral).
Periode
Die Periodennummer = Anzahl der besetzten Elektronenschalen (Energieniveaus).
Hauptgruppe
Die Hauptgruppennummer = Anzahl der Valenzelektronen (Außenelektronen). Entscheidet über chemische Eigenschaften.
Nukleonenzahl
Nukleonenzahl = Protonen + Neutronen. Neutronen = Nukleonenzahl − Ordnungszahl.
Häufige Fragen – PSE und Atombau
Wie lese ich die Ordnungszahl, Atommasse und Valenzelektronen aus dem PSE ab?
Die Ordnungszahl steht oben links beim Elementsymbol (= Anzahl der Protonen). Die relative Atommasse steht meist oben im Feld. Die Valenzelektronen (Außenelektronen) entsprechen direkt der Hauptgruppennummer. Beispiel: Chlor (Cl) steht in der 7. Hauptgruppe → 7 Valenzelektronen, Ordnungszahl 17 → 17 Protonen, 17 Elektronen.
Was ist der Unterschied zwischen Gruppe und Periode im PSE?
Eine Periode ist eine waagerechte Zeile. Die Periodennummer gibt an, wie viele Elektronenschalen das Atom hat. Eine Gruppe (= Spalte) fasst Elemente mit gleicher Anzahl an Valenzelektronen zusammen – sie haben daher ähnliche chemische Eigenschaften. Beispiel: Alle Alkalimetalle (1. HG) haben 1 Valenzelektron und reagieren ähnlich mit Wasser.
Was sind Valenzelektronen und warum sind sie wichtig?
Valenzelektronen (= Außenelektronen) befinden sich auf der äußersten besetzten Elektronenschale. Sie sind entscheidend für alle chemischen Reaktionen, weil Atome bevorzugt ihre äußere Schale vollständig besetzen wollen (→ Edelgasregel). Die Anzahl der Valenzelektronen ist direkt aus der Hauptgruppennummer ablesbar.
Wie berechne ich die Anzahl der Neutronen eines Atoms?
Neutronen = Nukleonenzahl − Ordnungszahl (= Nukleonenzahl − Protonenzahl). Beispiel: Natrium ²³Na → Nukleonenzahl 23, Ordnungszahl 11 → 23 − 11 = 12 Neutronen. Achtung: Die im PSE angegebene Atommasse ist ein Mittelwert über alle Isotope – für die Neutronenberechnung nimmt man den gerundeten ganzzahligen Wert.
Was ist der Unterschied zwischen Haupt- und Nebengruppenelemente?
Hauptgruppenelemente stehen in Gruppe 1–2 und 13–18. Die Hauptgruppennummer entspricht direkt der Anzahl der Valenzelektronen. Nebengruppenelemente (Gruppen 3–12, Übergangsmetalle wie Eisen, Kupfer, Zink) haben meistens 1–2 Valenzelektronen. Im Kurzperiodensystem werden Nebengruppen oft weggelassen. → 2.7 Lewis-Formeln
Lernkarten – PSE und Atombau
Klicke auf eine Karte, um die Antwort zu sehen.
1Was gibt die Ordnungszahl im PSE an?
Ordnungszahl = Anzahl der Protonen = Anzahl der Elektronen (im neutralen Atom) = Kernladungszahl.
2Was sagt die Periode (Zeile) im PSE aus?
Die Periodennummer = Anzahl der besetzten Elektronenschalen (Energieniveaus) des Atoms.
3Wie viele Valenzelektronen hat Chlor? Wie liest du das ab?
Cl steht in der 7. Hauptgruppe → 7 Valenzelektronen. Hauptgruppennummer = Anzahl der Valenzelektronen.
4Wie berechnet man die Anzahl der Neutronen?
Neutronen = Nukleonenzahl − Ordnungszahl. Beispiel: Na ²³Na → 23 − 11 = 12 Neutronen.
5Wie viele Valenzelektronen haben Edelgase und warum sind sie so stabil?
Edelgase haben 8 Valenzelektronen (He: 2) → vollständig besetzte Außenschale → energetisch sehr stabil → kaum Reaktionen (→ Edelgasregel).
Weiter im Kapitel: Atombau und PSE
← 2.5 Kugelwolkenmodell → 2.7 Lewis-Formeln → 3. Edelgasregel
🔁 Grundlagen: Rutherford · Bohr-Schalenmodell · Kugelwolkenmodell · PSE herunterladen
-
3 Redoxreaktionen mit Molekülen - Oxidationszahlen
3 Redoxreaktionen mit Molekülen
Bei der Verbrennung von Stoffen bilden sich Oxide, ohne dass es zur Bildung von Ionen kommt. Beispiele dafür sind die Verbrennung von Wasserstoff, Kohlenstoff, Schwefel und Phosphor.
Um diese Reaktion als Redoxreaktion erfassen zu können, hat man als Hilfsgröße die Oxidationszahl eingeführt.
3.1 Oxidationszahl
Def.: Die Oxidationszahl gibt an, welche Ladung ein Atom in einem Molekül oder in einem anderen Teilchen hätte, wenn alle am Aufbau des Teilchens beteiligten Atome in Form von Ionen vorlägen.
Die sich für die Atome in der Verbindung ergebenden formalen Ladungszahlen nennt man Oxidationszahlen. Zur Unterscheidung von Ionenladungen werden sie als römische Zahlen an die Elementsymbole geschrieben.
Vorgehensweise: Vgl. dazu die zwei Beispiele 3.2 und 3.3 um die Schritte nachvollziehen zu können.
1. Schritt: Strukturformel erstellen.
2. Schritt: Ermittlung der Elektronegativität aller Elemente (siehe PSE) :
3. Schritt: Bindungselektronen werden formal dem elektronegativeren Bindungspartner zugeteilt. Besitzen die Bindungspartner die gleiche Elektronegativität erhalten sie je die Hälfte der Bindungselektronen.Faustregel: (Hinweis: Wann immer eindeutige Strukturformeln möglich sind, würde ich keine Faustregeln nutzen)
- Fluor immer: –I
- Wasserstoff: +I
- Sauerstoff: -II
- Halogene: -I (sofern nicht mit Sauerstoff oder einem elektronegativeren Halogen verbunden sind)
4. Schritt: Man bestimmt die Hauptgruppennummer des Elements und zählt dann die Elektronen, welche das Element jetzt "formal" hätte (vgl. 3. Schritt). Dann berechnet man entsprechend folgender Formel:
Oxidationszahl = Hauptgruppennummer des Elements – Elektronenanzahl im Molekül
Bsp. Sauerstoff im Wassermolekül: Oxidationszahl(O) = steht in der 6. Hauptgruppe = VI - 8 = -2 (bzw. - II)
Bsp. Wasserstoff im Wassermolekül: Oxidationszahl(H) = I - 0 = +1
5. Schritt: Kontrolle: Summe der Oxidationszahlen muss 0 sein (bei elektr. Neutralen Molekülen).
Mit Hilfe der Oxidationszahl lassen sich die Begriffe Oxidation und Reduktion neu fassen:Oxidation: Elektronenabgabe) bedeutet eine Erhöhung der Oxidationszahl.
Reduktion: (Elektronenaufnahme) bedeutet eine Erniedrigung der Oxidationszahl.
Redoxreaktionen: sind Vorgänge bei denen sich die Oxidationszahlen der beteiligten Atomarten ändern.3.2 Vollständige Verbrennung von Kohlenstoff
Kohlenstoff Sauerstoff Kohlenstoff(IV)-oxid
Atom Molekül Molekül

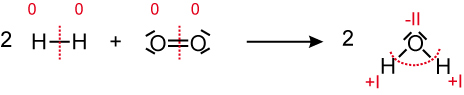
→ Kohlenstoff wird oxidiert, Sauerstoff wird reduziert.3.3 Reaktion von Wasserstoff mit Sauerstoff
Wasserstoff Sauerstoff Wasser
Oxidationszahlen von Wasserstoff wird positiver → Wasserstoff wird oxidiert
Oxidationszahlen von Sauerstoff wird negativer → Sauerstoff wird reduziert3.5 Reaktion von Wasserstoff mit Stickstoff zu Ammoniak (Ammoniaksynthese)
Oxidationszahlen von Wasserstoff wird positiver → Wasserstoff wurde oxidiert
Oxidationszahlen von Stickestoff wurde negativer → Stickstoff wurde reduziert3.6 Reaktion von Schwefel mit Sauerstoff zu Schwefeldioxid
Man muss nicht immer die Lewis-Formeln (Strukturformeln) zeichnen. Manchmal genügt es, nach den Faustregeln zu arbeiten.
Oxidationszahlen von Schwefel wird positiver → Schwefel wurde oxidiert
Oxidationszahlen von Sauerstoff wurde negativer → Sauerstoff wurde reduziert3.7 Synthese von Chlorwasserstoff aus den Elementen
Oxidationszahlen von Wasserstoff wird positiver → Wasserstoff wurde oxidiert
Oxidationszahlen von Chor wurde negativer → Chlor wurde reduziert3.8 Synthese von Schwefelwasserstoff aus den Elementen
Oxidationszahlen von Wasserstoff wird positiver → Wasserstoff wurde oxidiert
Oxidationszahlen von Schwefel wurde negativer → Schwefel wurde reduziert -
Periodensystem der Elemente - PSE
Ich habe für meine Schüler Periodensysteme erstellt, die jederzeit ausgedruckt werden können. Das Ziel: je nach Aufgabenstellung nur die wesentlichen Informationen. Die Werte stammen aus verschiedenen Quellen (www.wikipedia.de, www.internetchemie.info, Mortimer „Chemie", Holleman-Wiberg „Lehrbuch der anorganischen Chemie").
Falls gravierende Fehler vorhanden sind, würde ich mich über eine Nachricht freuen. Diese Periodensysteme können heruntergeladen und ausgedruckt werden.
Kurze Einführung in das Periodensystem der Elemente
Eine kurze Einführung in das PSE mit einfachen Übungen findest du auf meiner Basischemie-Seite. Allerdings ist das empfohlene PSE nicht mehr online (weshalb ich selber welche erstellte; vgl. unten).
Periodensysteme

1. Einfaches PSE für die Schule
Beschränkt sich auf die wesentlichen Informationen. Auch die Halbmetalle sind sehr einfach wiedergegeben.
- Elektronegativität
- Namen (deutsch und englisch)
- Ordnungsnummer · Masse · Symbol
- Halbmetalle (vereinfacht; vgl. Wikipedia)
- Metalle · Nichtmetalle · Edelgase
- Aggregatzustand bei 20 °C
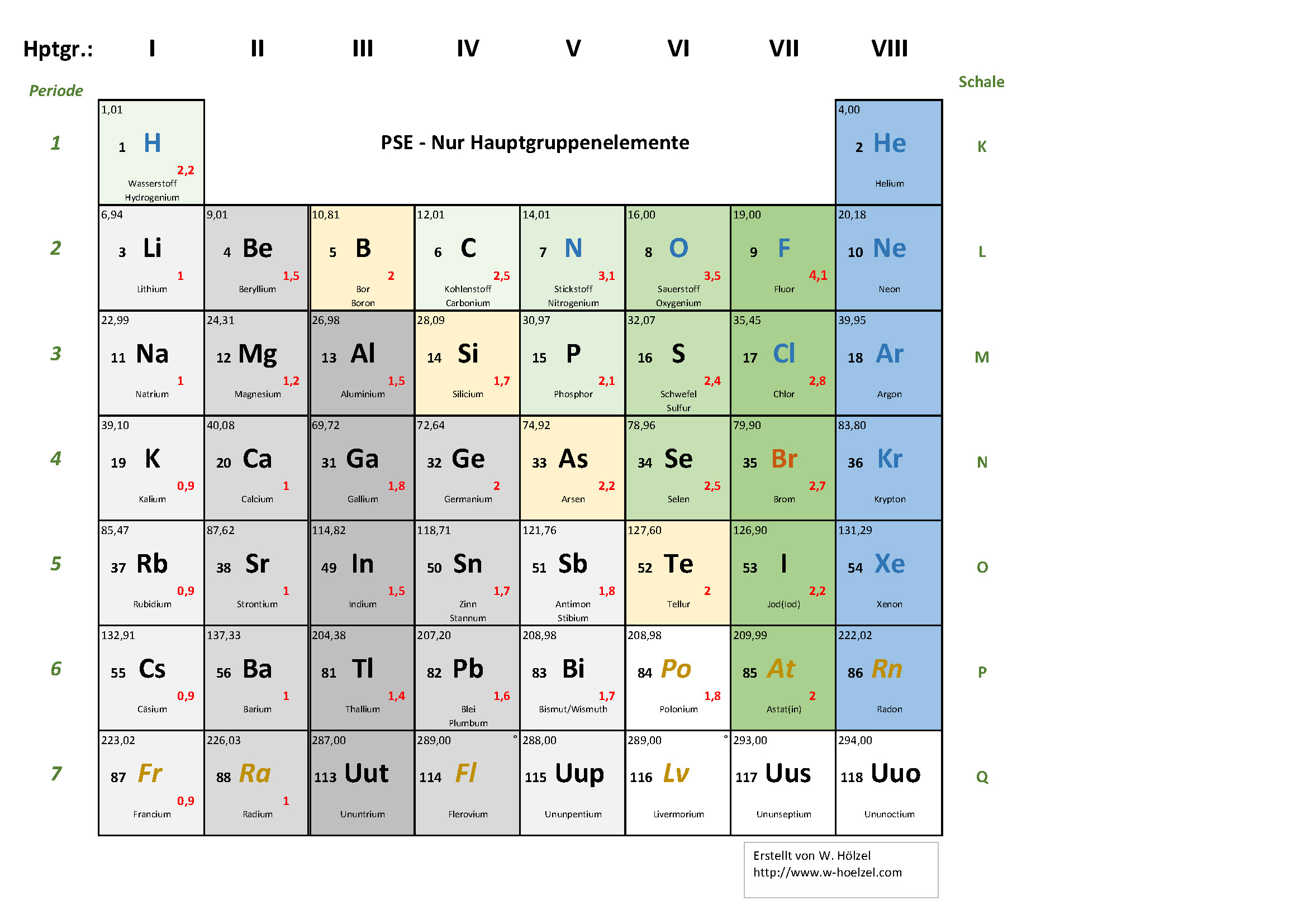
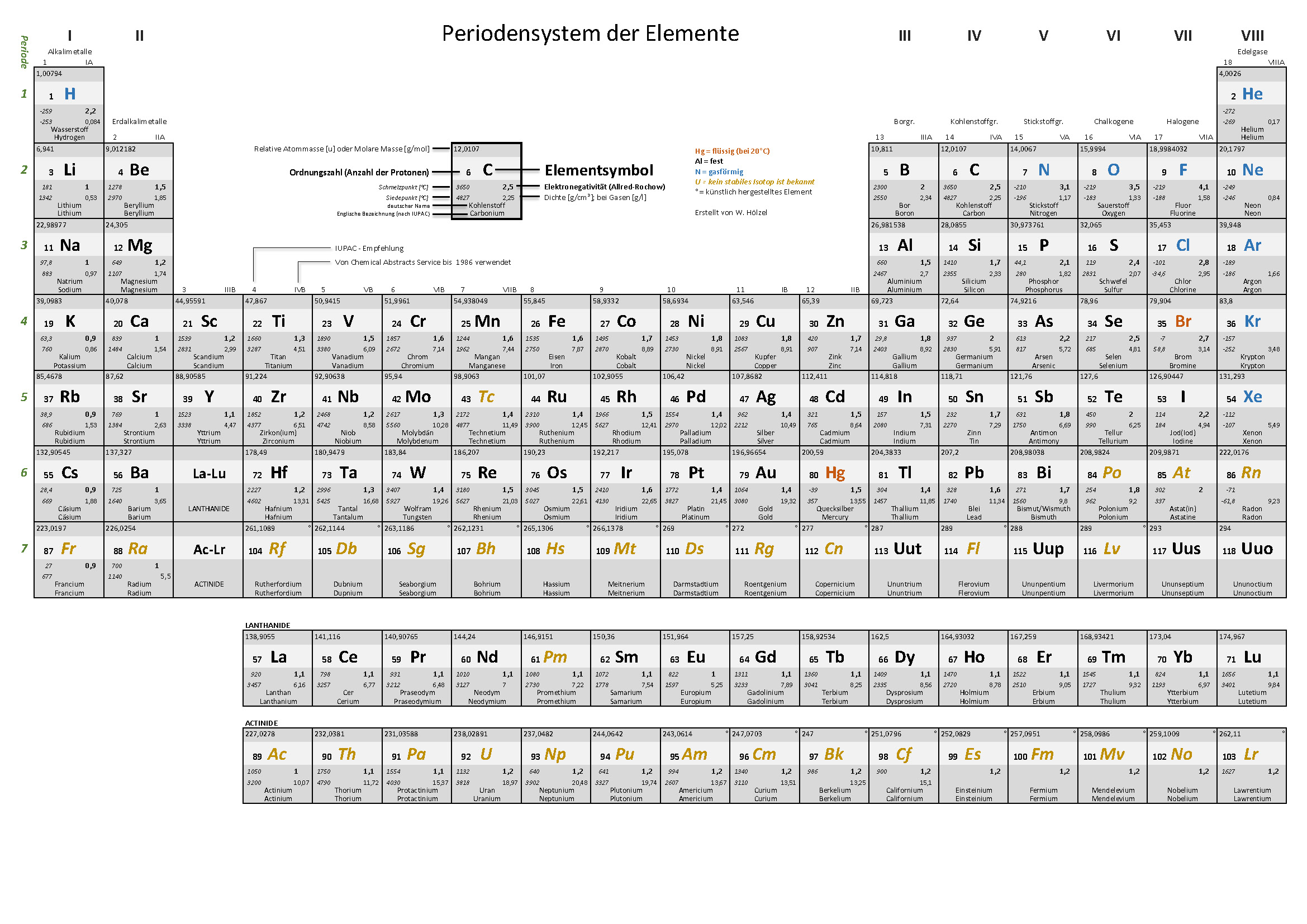
3. PSE – Nur Hauptgruppenelemente
Für Edelgasregel, Atombindungen und erste Salze — ohne Nebengruppen.
- Elektronegativität
- Namen (deutsch und englisch)
- Ordnungsnummer · Masse · Symbol
- Halbmetalle (vgl. Wikipedia)
- Metalle · Nichtmetalle · Edelgase
- KEINE Nebengruppen, Lanthanide, Actinide
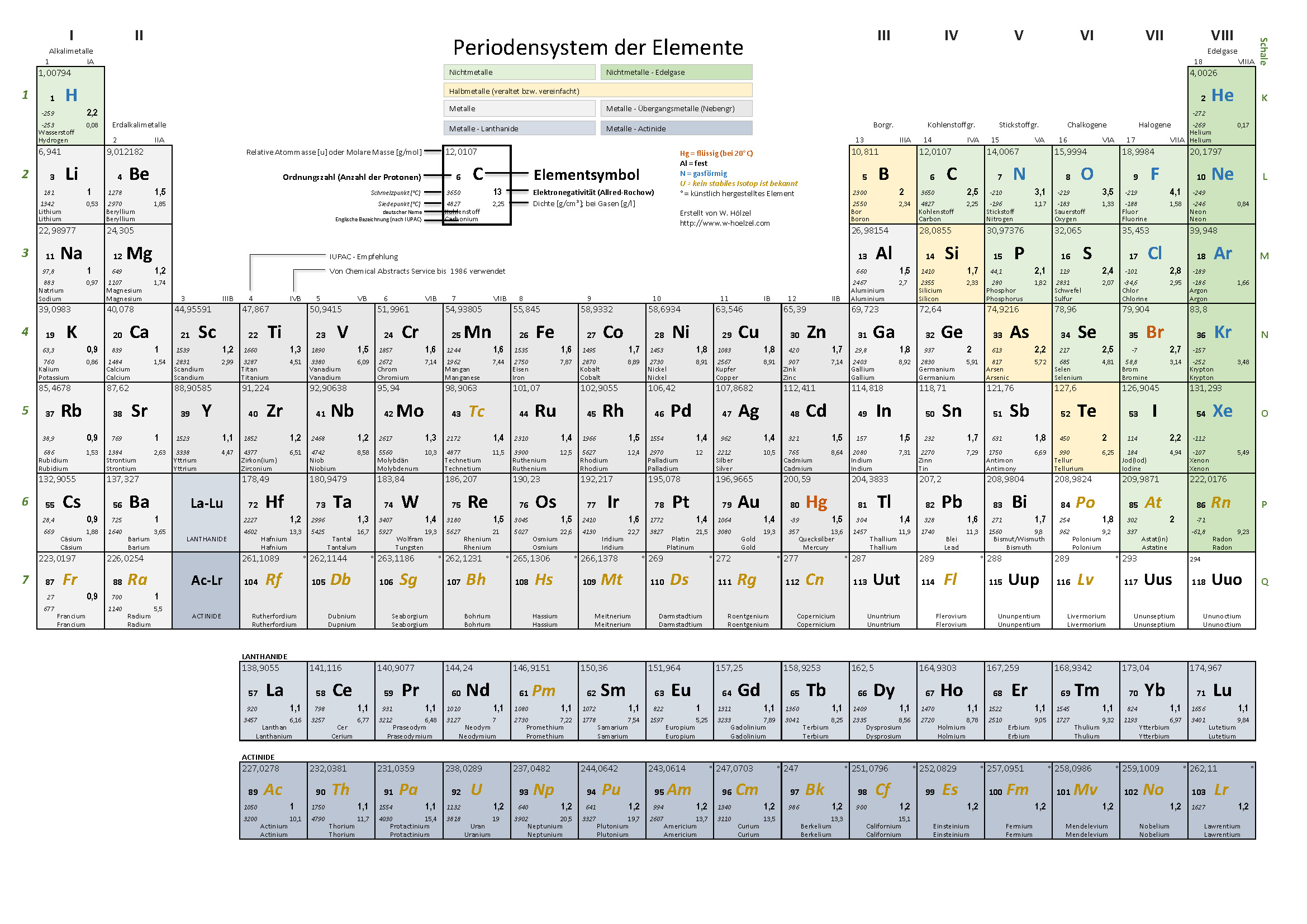
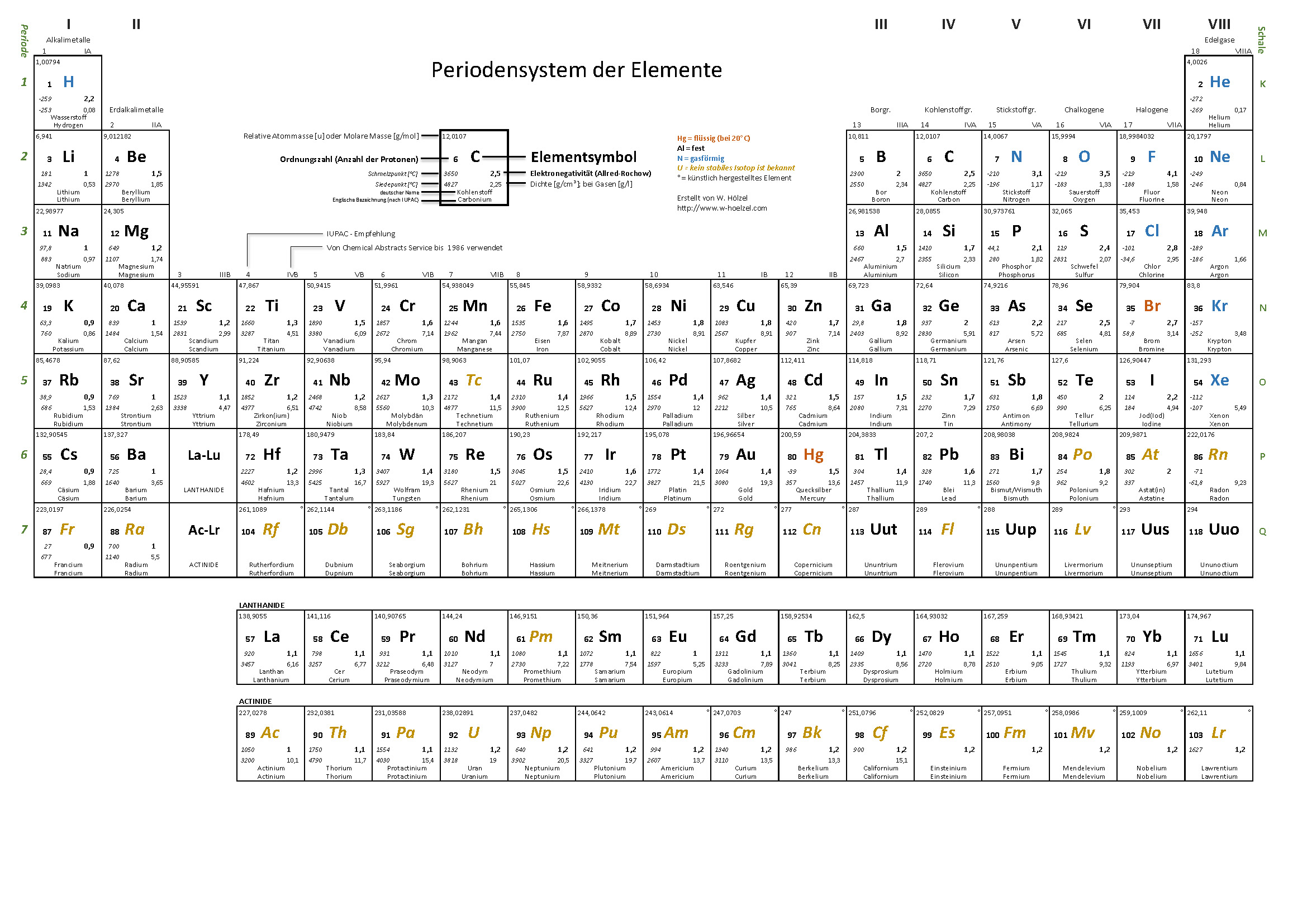
6. PSE – Einteilung Metalle / Nichtmetalle
Farbige Einteilung der Metalle, Halbmetalle, Nichtmetalle und Edelgase.
- Elektronegativität
- Namen (deutsch und englisch)
- Ordnungsnummer · Masse · Symbol
- Halbmetalle (vgl. Wikipedia)
- Metalle · Nichtmetalle · Edelgase
- Aggregatzustand · Dichte · Schmelz- und Siedetemperatur
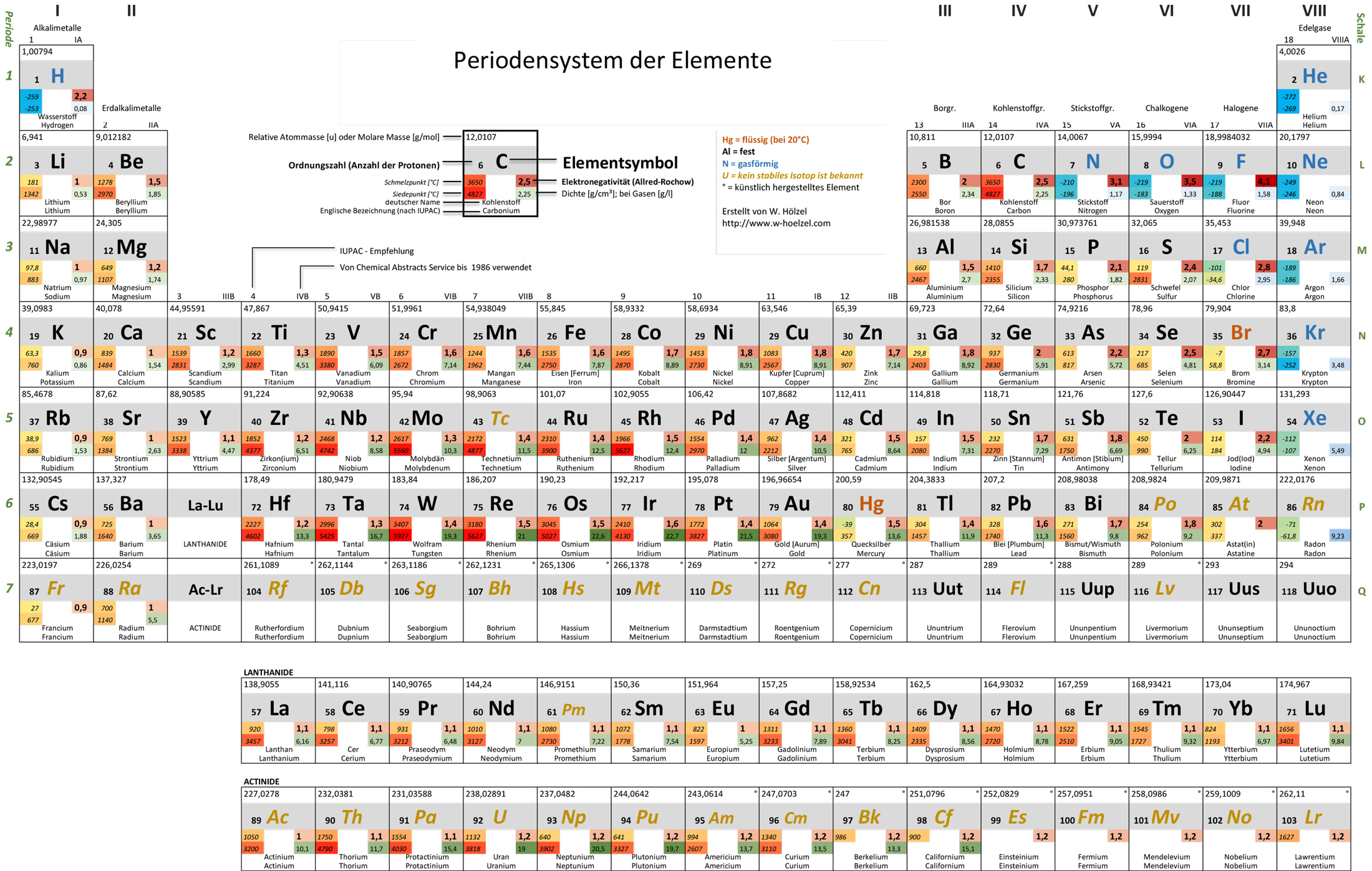
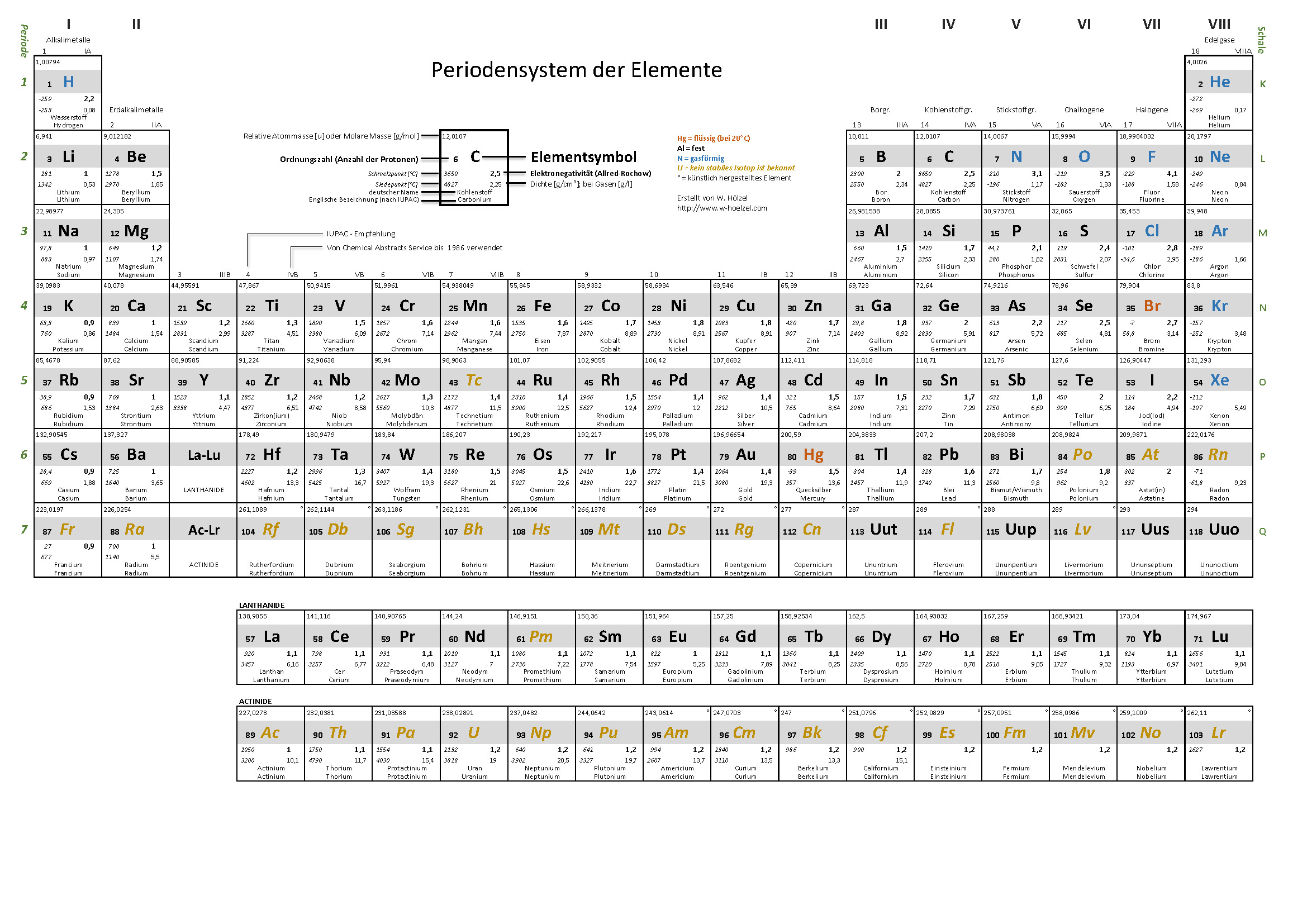
10. PSE – Farbkodierung für Eigenschaften
Visualisiert Schmelztemperatur, Siedetemperatur, Dichte und Elektronegativität mittels Farbkodierung.
- Elektronegativität [farbig]
- Namen (deutsch und englisch)
- Ordnungsnummer · Masse · Symbol
- Aggregatzustand · Dichte [farbig]
- Schmelztemperatur [farbig] · Siedetemperatur [farbig]
Einige Beispiele weiterer Periodensysteme im Internet
- Zentrale Übersicht: https://de.wikipedia.org/wiki/Periodensystem
- Hervorragende Datensammlung: www.internetchemie.info
- Interaktives PSE mit Elektronenverteilung und Wikipedia-Links: www.ptable.com
- Interaktives PSE mit PSE-Ansichten: www.uniterra.de