Redoxreaktion/Redoxpaar
-
1 Freiwillig ablaufende Reaktionen
Was du auf dieser Seite lernst
Du wiederholst die Grundbegriffe der Redoxchemie und lernst sie neu zu durchdenken: Was bedeuten Oxidation und Reduktion im Sinne der Elektronenübertragung? Was ist ein korrespondierendes Redoxpaar? Am Beispiel Magnesium + Sauerstoff werden Reaktionsgleichung, Redoxschema und Elektronenbilanz erarbeitet.
Grundlagen aus der 9. Klasse
Den Versuch Magnesium + Sauerstoff und die erste Einführung in Oxidation und Reduktion kennst du bereits aus der 9. Klasse: → Magnesium und Sauerstoff (Kl. 9) · → Neue Definitionen: Oxidation / Reduktion (Kl. 9)
1.1 Wiederholung bekannter Begriffe und Definitionen
Versuch 1: Magnesium + Sauerstoff
Magnesium verbrennt mit stark leuchtender Flamme. Ein weißer Feststoff bleibt übrig.
Formuliere die Reaktionsgleichungen und ein Redoxschema:
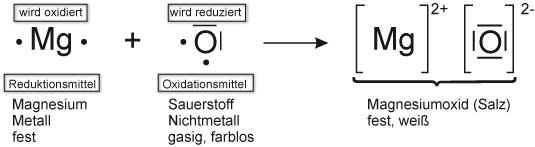
✕Lösung: Reaktionsgleichung und Redoxschema Mg + O₂
Zunächst vereinfacht atomar (natürlich liegt Sauerstoff molekular vor):
↑ Zum Vergrößern klicken
Vollständiger:
Reaktionsgleichung: 2 Mg + O2 → 2 MgO ΔH < 0
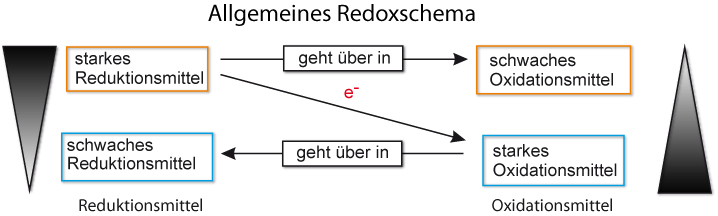
Redoxschema (allgemein):
↑ Zum Vergrößern klicken
↑ Zum Vergrößern klicken
 ✕
✕
 ✕
✕
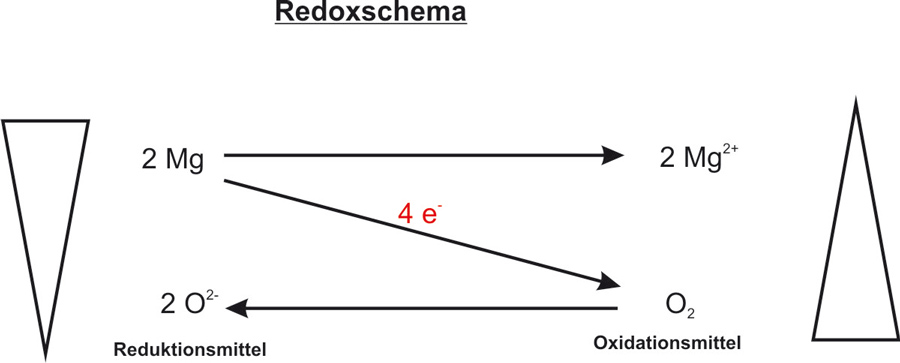
Einfach ist es, wenn man die Teilreaktionen (Oxidation und Reduktion) erstellt und dann erst die Redoxreaktion. Versucht mal diese zu formulieren:
Lösung: Teilreaktionen und Elektronenbilanz Mg + O₂
Oxidation: Mg → Mg2+ + 2 e− | · 2
Reduktion: O2 + 4 e− → 2 O2− | · 1
————————————————————————
Redoxreaktion: 2 Mg + O2 → 2 Mg2+ + 2 O2−Begriffe und Definitionen
Oxidation = Elektronenabgabe; Erhöhung der Oxidationszahlen
Reduktion = Elektronenaufnahme; Erniedrigung der OxidationszahlenOxidationsmittel: Elektronenakzeptor („Elektronenräuber"); wird bei der Reaktion selbst reduziert. [Eselsbrücke: Putzmittel]
Reduktionsmittel: Elektronendonator („Elektronenspender"); wird bei der Reaktion selbst oxidiert.Redoxreaktionen: Reaktionen mit Elektronenübertragung.
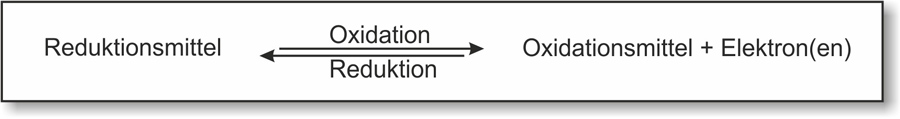
Oxidation und Reduktion laufen gleichzeitig ab.Ein Reduktionsmittel gibt Elektronen ab, die es später wieder aufnehmen kann. Es wird also zu einem Oxidationsmittel.
↑ Zum Vergrößern klicken
✕
↑ Zum Vergrößern klicken
✕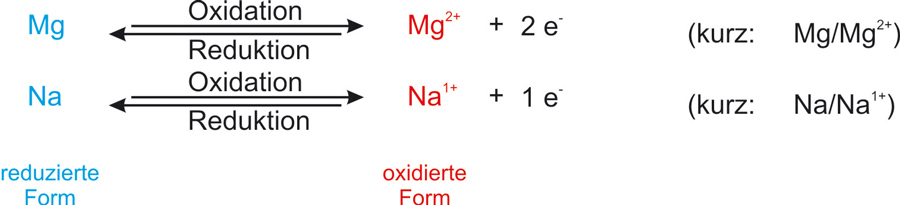
Reduktionsmittel und Oxidationsmittel bilden ein korrespondierendes Redoxpaar:
↑ Zum Vergrößern klicken
✕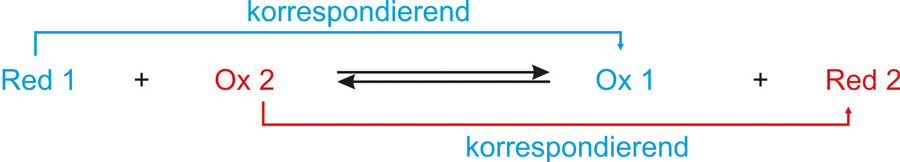
Die übliche Kurzschreibweise für ein Redoxpaar:
Reduzierte Form / oxidierte Form
Me / Men+Bei jeder Redoxreaktion sind zwei korrespondierende Redoxpaare beteiligt (analog: Protolysereaktion).
Wichtig – Elektronenbilanz
Die Zahl der abgegebenen und aufgenommenen Elektronen muss gleich sein – die Elektronenbilanz muss stimmen. Dazu multipliziert man die Teilreaktionen mit dem geeigneten gemeinsamen Vielfachen.
Auf einen Blick – die wichtigsten Aussagen
Oxidation
Oxidation = Elektronenabgabe. Die Oxidationszahl steigt. Das abgebende Teilchen heißt Reduktionsmittel und wird dabei selbst oxidiert.
Reduktion
Reduktion = Elektronenaufnahme. Die Oxidationszahl sinkt. Das aufnehmende Teilchen heißt Oxidationsmittel und wird dabei selbst reduziert.
Korrespondierendes Redoxpaar
Ox/Red-Form bilden ein Redoxpaar (Kurzschreibweise: Men+/Me). Bei jeder Redoxreaktion sind stets zwei korrespondierende Paare beteiligt.
Elektronenbilanz
Abgegebene Elektronen = aufgenommene Elektronen. Teilreaktionen mit dem gemeinsamen Vielfachen multiplizieren, bis die Bilanz stimmt.
Häufige Fragen – Freiwillig ablaufende Redoxreaktionen
Was ist der Unterschied zwischen Oxidation und Reduktion?
Oxidation ist die Abgabe von Elektronen – die Oxidationszahl des betroffenen Atoms steigt. Reduktion ist die Aufnahme von Elektronen – die Oxidationszahl sinkt. Beide Prozesse laufen immer gleichzeitig ab: Kein Teilchen gibt Elektronen ab, ohne dass ein anderes sie sofort aufnimmt. Man spricht daher von einer Redoxreaktion. Grundlagen: → Neue Definitionen Kl. 9
Was versteht man unter einem korrespondierenden Redoxpaar?
Ein korrespondierendes Redoxpaar besteht aus der oxidierten und der reduzierten Form eines Teilchens, z. B. Mg2+/Mg oder O/O2−. Kurzschreibweise: Ox-Form / Red-Form bzw. Men+/Me. Bei jeder Redoxreaktion sind genau zwei solcher Paare beteiligt – analog zu den zwei korrespondierenden Säure-Base-Paaren bei der Protolyse.
Wie unterscheiden sich Oxidationsmittel und Reduktionsmittel?
Das Oxidationsmittel ist der Elektronenakzeptor: Es nimmt Elektronen auf und wird dabei selbst reduziert (Eselsbrücke: „Putzmittel oxidiert = nimmt auf"). Das Reduktionsmittel ist der Elektronendonator: Es gibt Elektronen ab und wird dabei selbst oxidiert. Im Beispiel Mg + O₂ ist Mg das Reduktionsmittel, O₂ das Oxidationsmittel.
Wie muss die Elektronenbilanz bei einer Redoxreaktion aussehen?
Die Anzahl der abgegebenen Elektronen (Oxidation) muss exakt gleich der Anzahl der aufgenommenen Elektronen (Reduktion) sein. Um das zu erreichen, multipliziert man die Teilreaktionen mit geeigneten ganzzahligen Faktoren (kleinstes gemeinsames Vielfaches). Beispiel Mg + O₂: Die Oxidation (2 e− pro Mg) wird mit 2 multipliziert, die Reduktion (4 e− pro O₂) bleibt 1× → 4 e− auf beiden Seiten.
Was ist der Unterschied zwischen der atomaren und der molekularen Schreibweise der Reaktionsgleichung?
Die atomare Schreibweise (vereinfacht) betrachtet nur einzelne Atome und ist gut für das Verständnis der Elektronenübertragung. Die molekulare Schreibweise berücksichtigt den tatsächlichen Aggregatzustand der Stoffe (O₂ liegt molekular vor) und liefert die vollständige, ausbalancierte Reaktionsgleichung: 2 Mg + O2 → 2 MgO (ΔH < 0).
Lernkarten – Freiwillig ablaufende Redoxreaktionen
Klicke auf eine Karte, um die Antwort zu sehen.
1Was bedeutet Oxidation im Sinne der Elektronenübertragung?
Oxidation = Elektronenabgabe
→ Oxidationszahl steigt
→ Das abgebende Teilchen heißt Reduktionsmittel
(wird selbst oxidiert)2Was bedeutet Reduktion im Sinne der Elektronenübertragung?
Reduktion = Elektronenaufnahme
→ Oxidationszahl sinkt
→ Das aufnehmende Teilchen heißt Oxidationsmittel
(wird selbst reduziert)3Was versteht man unter einem korrespondierenden Redoxpaar? Gib die Kurzschreibweise an.
Ox-Form und Red-Form eines Teilchens bilden ein Paar.
Kurzschreibweise: Men+/Me
(erst oxidierte, dann reduzierte Form)
Bei jeder Redoxreaktion: 2 Paare4Woran erkennt man das Oxidationsmittel und das Reduktionsmittel in einer Reaktion?
Oxidationsmittel:
nimmt e− auf → wird reduziert
Reduktionsmittel:
gibt e− ab → wird oxidiert
Merke: Jedes Oxidationsmittel wird selbst reduziert.5Stelle die Teilreaktionen für 2 Na + Cl₂ → 2 NaCl auf und prüfe die Elektronenbilanz.
Oxidation: Na → Na+ + e− | ·2
Reduktion: Cl2 + 2 e− → 2 Cl− | ·1
————————————
2 Na + Cl2 → 2 Na+ + 2 Cl−
Bilanz: 2 e− abg. = 2 e− aufg. ✓Weiter im Kapitel Elektrochemie
← Elektrochemie – Übersicht → 1 Freiwillig ablaufende Reaktionen – Teil B → 1.2 Erstellung einer Redoxreihe
🔁 Grundlagen (Kl. 9): Magnesium + Sauerstoff · Neue Definitionen Oxidation / Reduktion · Oxidationszahlen
